| 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火... | 您所在的位置:网站首页 › 肼又称联氨是一种可燃性的液体对不对 › 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火... |
肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火...
|
(12分) 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。 (1)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。该电池放电时,通入肼的一极为________极,该极的电极反应式是________,电池工作一段时间后,电解质溶液的pH将________(填“增大”、“减小”、“不变”)。 (2)肼用亚硝酸氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977。写出肼与亚硝酸反应的化学方程式________。 (3)肼和四氧化二氮作火箭推进剂,两者反应产物是氮气和水。当反应生成28.0kg还原产物时,计算参加反应的肼的质量 (写出计算过程) 。 高三化学填空题简单题查看答案及解析 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。 (1)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。该电池放电时,通入肼的一极为 极,该极的电极反应式是 。电池工作一段时间后,电解质溶液的pH将 (填“增大”、“ (2)肼用亚硝酸(HNO2)氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977。写出肼与亚硝酸反应的化学方程式 (3)肼和四氧化二氮作火箭推进剂,两者反应产物是氮气和水。当反应生成28.0kg还原产物时,计算参加反应的肼的质量 (写出计算过程) 。 高三化学填空题困难题查看答案及解析 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料.(1)已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol,2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=一1135.7kJ/mol.则肼完全燃烧的热化学方程式为______.(2)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,正极的电极反应式是______,电池工作一段时间后,电解质溶液的pH将______(填“增大”、“减小”、“不变”).(3)如图是一个电化学装置示意图.用肼--空气燃料电池做此装置的电源.①如果A为含有锌、银、金三种杂质的粗铜,B为纯铜,C为CuSO4.该装置的实际意义是______.②如果A是铂电极,B是石墨电极,C是AgNO3溶液,若B极增重10.8g,该燃料电池理论上消耗______molN2H4.(4)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因______.(5)常温下将0.2mol/L HCl溶液与0.2mol/L N2H4•H2O溶液等体积混合(忽略混合后溶液体积的变化),若测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)______0.1mol/LHCl溶液中由水电离出的c(H+)(填“大于”、“小于”、或“等于”).(6)已知:在相同条件下N2H4•H2O的电离程度大于N2H5C1的水解程度.常温下,若将0.2mol/L N2H4•H2O溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H-5、Cl-、OH-、H+离子浓度南大到小的顺序为______. 高三化学解答题中等难度题查看答案及解析 (15分) 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。 (1)已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/tool 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=一1135.7kJ/mol 则肼完全燃烧的热化学方程式为________。 (2)肼——空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。该电池放电时,正极的电极反应式是________,电池工作一段时间后,电解质溶液的pH将________(填“增大”、“减小”、“不变”)。 (3)右图是一个电化学装置示意图。用肼——空气燃料电池做此装置的电源。
①如果A为含有锌、银、金三种杂质的粗铜,B为纯铜,C为CuSO4。该装置的实际意义是________。 ②如果A是铂电极,B是石墨电极,C是AgNO3溶液,若B极增重10.8g,该燃料电池理论上消耗________molN2H4。 (4)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因________。 (5)常温下将0.2mol/L HCl溶液与0.2mol/L N2H4·H2O溶液等体积混合(忽略混合后溶液体积的变化),若测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)________0.1mol/LHCl溶液中由水电离出的c(H+)(填“大于”、“小于”、或“等于”)。 (6)已知:在相同条件下N2H4·H2O的电离程度大于N2H5C1的水解程度。常温下,若将0.2mol/L N2H4·H2O溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H-5、Cl-、OH-、H+离子浓度南大到小的顺序为________。 高三化学填空题简单题查看答案及解析 [s1] 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。 (1)已知:N2(g)+2O2(g)=2NO2(g) △H= +67.7 kJ/mol 2N2H4(l)+2NO2(g)=3N2(g)+4H2O(g) △H= -1135.7 kJ/mol 则肼完全燃烧的热化学方程式为_______________________________________。 (2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。该电池放电时,正极的电极反应式是______________________________________,电池工作一段时间后,电解质溶液的pH将_________(填“增大”、“减小”、“不变”)。
做此装置的电源。如果A是铂电极,B是石墨电极,C 是AgNO3溶液, 若B极增重10.8 g,该燃料电池理 论上消耗_____mol N2H4。 (4)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示 肼的水溶液显碱性的原因_________________________。 [s1]24. 高三化学填空题极难题查看答案及解析 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料.(1)已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7kJ/mol则32g肼完全燃烧得到气态产物时放出热量______kJ.(2)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,正极的电极反应式是______,电池工作一段时间后,电解质溶液的pH将______(填“增大”、“减小”、“不变”).(3)如图是一个电化学装置示意图.用肼--空气燃料电池做此装置的电源.①如果A为含有锌、银、金三种杂质的粗铜,B为纯铜,C为CuSO4.该装置的实际意义是______.②如果A是铂电极,B是石墨电极,C是AgNO3溶液,电解的离子方程式为______ 4Ag+4HNO3+O2↑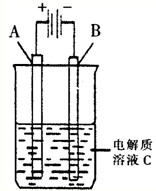 高三化学解答题中等难度题查看答案及解析 肼(N2H4)又称联氨,其液体可燃,燃烧热较大且燃烧产物对环境无污染,可以用作火箭燃料。肼溶于水是一种二元碱。 完成下列填空: (1)写出肼的电子式 ,肼的晶体类型 。 (2)工业上可用次氯酸钠和氨反应制肼,若只有一种氧化产物。写出该方法制备肼的化学方程式 。 (3)0.2mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出128.3kJ的热量。 写出该反应的热化学方程式 。 (4)室温下,N2H5Cl的水溶液显 (填酸、碱、中)性。 其原因是。 已知:H2O N2H4 + H2O [N2H5]+ + H2O (5)肼可以和氧气反应N2H4+O2→N2+2H2O。为除去高压锅炉用水中溶解的O2,常用N2H4或Na2SO3。除去等物质的量的O2,所消耗的N2H4和Na2SO3的质量之比为 。 与N2H4相比较,使用Na2SO3会对锅炉造成不良的影响,其原因是 。 高三化学填空题困难题查看答案及解析 肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均可生成氮气和水,用作火箭燃料.(1)写出肼与一氧化氮反应的化学方程式______.(2)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,电极反应式:负极______.(3)如图是一个电化学装置示意图.用肼--空气燃料电池做此装置的电源.①如果A为含有铁、银、金、碳等杂质的粗铜,B为纯铜,C为CuSO4溶液.通电一段时间后,______极的质量增大.(填“阴极”、“阳极”).②如果A是铂电极,B是石墨电极,C是CuSO4溶液,阳极的电极反应式是______.若产生1mol气体则消耗肼为______g.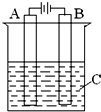 高三化学解答题中等难度题查看答案及解析 (10分)(1)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在101kPa,320g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是:________ (2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。肼—空气燃料电池放电时,正极的电极反应式是________;负极的电极反应式是 ________。 (3)如图是一个电化学过程示意图。假设使用肼—空气燃料电池作为本过程的电源,铜片质量变化128g,则肼—空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气的体积含量为20%)。
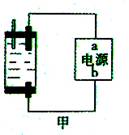
(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是________。 高三化学填空题简单题查看答案及解析 (10分)、Ⅰ:(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是________。 (2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%一30%的KOH溶液。肼—空气燃料电池放电时:正极的电极反应式是________。 Ⅱ:探究家庭制备次氯酸钠溶液的发生器如右图,原理是用石墨做电极电解饱和食盐水。
(1)若通电后,为使氯气被全部吸收,则电源的a极的名称是________。 (2)电解饱和食盐水的离子方程式为________,所得的次氯酸钠溶液中加入几滴石蕊试液,观察到的现象是 ________ , 用离子方程式和简要文字说明理由________。 高三化学填空题中等难度题查看答案及解析 |
【本文地址】