| 中美双报安全性数据报告Gateway,你"get way"了吗? | 您所在的位置:网站首页 › gateway和getway › 中美双报安全性数据报告Gateway,你"get way"了吗? |
中美双报安全性数据报告Gateway,你"get way"了吗?
|
谷科林自研了支持中美双报的药物警戒系统,并已分别与CDE和FDA Gateway传输测试成功。 一、报告CDE的电子传输方式 药品审评中心(CDE)目前仅接受以下两种个例不良反应电子传输方式,两种方式可任选其一: 1.GATEWAY方式提交 申请人申请GATEWAY账号并进行电子传输测试,测试成功后,进行正式提交。 2.XML文件方式提交 申请人登陆国家药品审评中心官方网站(www.cde.org.cn),在“申请人之窗”注册账号,在左侧菜单栏下的“药物警戒提交”提交XML格式文件。 Gateway方式较XML文件方式来讲,递交报告更加便捷高效。因此,若申办方已使用PV系统,一般优选Gateway方式速报,仅在系统或端口对接等出现故障、无法实现Gateway方式递交时,才选择在“申请人之窗”提交XML格式文件。 与CDE进行Gateway对接的具体要求和步骤详见 《药物临床试验期间安全性数据快速报告标准和程序》 。现将简单步骤描述如下: 1.提交测试报告: (1)填写《ICSR电子传输账号申请表》,发送至[email protected],注册用于个例安全性报告的电子传输测试账号。 (2)CDE工作人员收到邮件申请后,将配置用户提供的配置信息和AS2证书到测试环境,并回复邮件提供CDE的AS2证书和配置信息。 (3)用户配置CDE的AS2证书和配置信息到PV系统的测试环境。 (4)用户发送一份测试的ICSR报告,验证模块间的对接有效且可以传输符合E2B(R3)要求的电子文档,当收到药品审评中心确认测试报告有效的电子回执后,即成功建立测试传输ICSR的数据连接。 2.提交正式报告: (5)填写《ICSR电子传输账号申请表》,发送至[email protected],注册用于个例安全性报告的电子传输的正式账号。详见附表。 (6)CDE工作人员收到邮件申请后,将配置用户提供的配置信息和AS2证书到正式环境,并回复邮件提供CDE的AS2证书和配置信息。 (7)用户配置CDE的AS2证书和配置信息到PV系统的正式环境。 (8)用户收到邮件后发送一份正式的ICSR报告,验证模块间的对接有效且可以传输符合E2B(R3)要求的电子文档,当收到药品审评中心确认正式报告有效的电子回执后,即成功建立正式传输ICSR的数据连接。
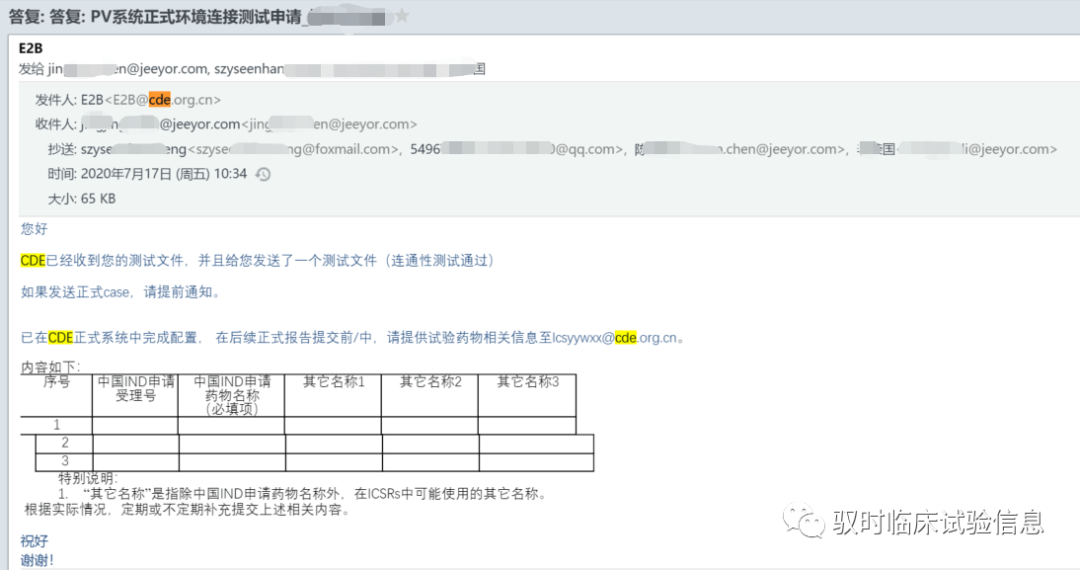
图1.与CDE Gateway对接测试成功的通知邮件 二、报告FDA的电子传输方式 FDA ESG(Electronic submission gateway)提供两种电子传输的方式:WebTrader和AS2。 1.WebTrader:WebTrader是一个基于网页的界面,用于发送报告文档和接收来自FDA的回执和确认。每个用户都必需注册他们自己唯一的WebTrader帐户。 2.AS2(System-to-System):用户可以选择通过系统与系统通信访问网关的方式递交报告。系统与系统之间的通信(通常称为AS2)为提交、收据和确认提供了与FDA的自动连接,需要配置服务器和软件。提交可以自动或手动发送,回执和确认可以异步或同步接收。 与FDA目标中心(如CDER)进行Gateway对接的步骤: 1.申请AS2账号: (1)发送邮件至[email protected]申请AS2测试账号,并按照网页要求提供相关配置信息。 2.准备工作: (2)寄送纸质版Letter of Non-Repudiation(官网提供模板)给FDA。 (3)获取个人电子证书及密钥。 (4)按指南准备电子传输测试文件。 (5)准备负载测试文件(大文件)。 (6)阅读FDA ESG网站上的用户指南和教程。 3.注册测试账号 (7)收到受理邮件后,根据邮件提供的网址、账号和密码填写配置信息和上传AS2证书。 4.设置AS2参数 (8)收到账号激活通知后(大约48小时内),双方互换配置信息和证书,配置到各自的测试环境中。 5.发送测试文件 (10)发送符合各中心指南要求的负载测试文件到目标中心。 6.正式环境账号批准 (11)递交测试通过后,ESG helpdesk将发送邮件指导如何注册正式环境AS2账号。 (12)根据指导互换配置信息和证书并配置到正式环境中,约48小时内可收到账号激活通知,即可正式发送报告。
图2.与FDA Gateway对接测试成功的通知邮件 欢迎留言,有言必复~返回搜狐,查看更多 |
【本文地址】
| 今日新闻 |
| 推荐新闻 |
| 专题文章 |