| 信立泰国产共晶S086申请上市:药 | 您所在的位置:网站首页 › exp3174代谢 › 信立泰国产共晶S086申请上市:药 |
信立泰国产共晶S086申请上市:药
|
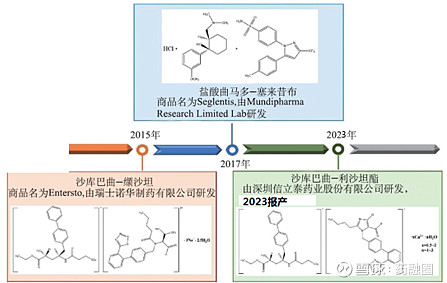
来源:雪球App,作者: 药融圈,(https://xueqiu.com/1923373626/260738141) 引言 2023年7月7日CDE官网显示,信立泰S086(沙库巴曲阿利沙坦钙共晶)申请上市获受理。业内普遍认为S086是国产商业化的第一个药-药共晶,借助信立泰热点,本文从产业化的角度浅述药物-药物共晶相关的技术问题。 1 药-药共晶是first-in-class的新药吗? 药-药共晶也称为多药共晶,即两个或者两个以上的药物活性物质(API)按照特定的化学计量比存在于同一个晶胞结构中。药-药共晶是药物共晶的一个”子集”,可以理解为特殊的共晶。我们接下来从已上市多药共晶和行业指南两个维度分析药-药共晶法规监管问题: 维度1:商业化的药药共晶 依据“晶体工程设计”并成功产业化的药-药共晶有3个(如图1所示):
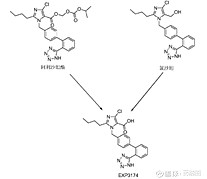
图1商业化的药-药共晶 诺欣妥(Entresto) –诺华 LCZ696是沙库巴曲和缬沙坦钠的药-药共晶,2015年FDA和欧盟先后通过快速审评通道批准上市,监管分类是First-in-class的一类新药。药物活性组分1-缬沙坦是已上市药物API,2001年获批;药物活性组分2-沙库巴曲是新API,沙库巴曲在共晶申报前未上市,其游离酸形态为油状物,成盐后吸湿性极强,制剂成药性差,这可能是沙库巴曲进一步开发共晶的动机,但意料之外的是共晶的效果,专家共识表明:LCZ696共晶是影响药代动力学的经典案例,两种API在同一晶格中,形成协同效应,实现了1+1>2临床作用。 有观点认为,因为沙库巴曲为新活性API,LCZ696共晶被认定是“新分子实体”,所以按1类新药监管申报。这观点不能说他是错的,但也不全对。为什么呢?咱们接着往下看看第二个获批上市的药-药共晶。 Seglentis –西班牙埃斯蒂文公司 E58425盐酸曲马多-塞来昔布共晶,2017年在欧洲按First-in-class共晶新药获批, 2018年我国按1类进口新药引进,2021年FDA按1类新药批准该多药共晶上市。但组成多药共晶的两个API均是获批20年之久的老药:共晶组分1-盐酸曲马多商品名Ultram,1995年获FDA批准上市;共晶组分2-塞来昔布商品名Celebrx, 1998年FDA批准上市。 E58425盐酸曲马多-塞来昔布共晶专家共识:独特的药-药共晶结构赋予两种API 差异化的内在溶出曲线,共晶中的曲马多溶出变慢(比单药溶出慢7倍),塞来昔布溶出变快(比单药塞来昔布快3倍,塞来昔布为BCSII类),溶出的改变可以转化为临床获益,与参考产品相比具有更高的效益风险比,且剂量降低。与LCZ696一样,E58425药-药共晶,通过晶体工程设计,同样实现了1+1>2的药物-药物协同作用。 信立泰S086 沙库巴曲-阿利沙坦酯共晶,CDE按1类新药注册申报。从专利推测其API—API共晶组分:活性组分1-沙库巴曲,共晶活性组分2-阿利沙坦酯活性代谢物EXP3174(新活性分子)。下图2是代谢物EXP3174与阿利沙坦结构关系示意图,可以判断S086是LCZ696的一个“me-too”产品,但信立泰另辟蹊径,走出了国产药-药共晶新药申报成功的第一步,笔者认为非常值得业内学习。
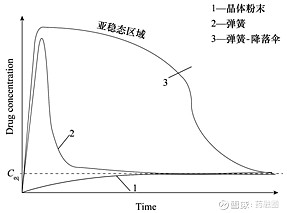
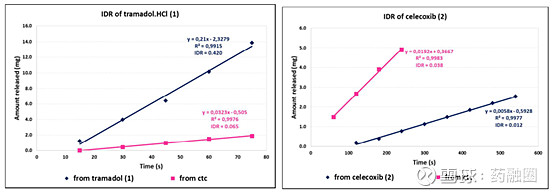
图2代谢物EXP3174结构图 维度2:共晶行业指南 共晶行业指南有2个:EMA在2015年发布“共晶使用文件”《Reflection paper on the use of cocrystals of active substances in medicinal product》和FDA在2018年发布的《guidance for industry – regulatory classification of pharmaceutical co-crystals. 2018》。FDA指南中未涉及到具体药-药共晶的监管说明。EMA“共晶使用文件”相对来说态度更“开放”,其根本理念是“根据共晶对药物安全性/有效性的影响大小来确定是否将共晶作为“新分子实体”。曲马多-塞来昔布两个老药的共晶,2017年率先在欧洲作为First-in-class的新药获批,2021年FDA也作为1类新药批准,以此来看,市场走在“文件”的前面。 总体来讲,抛开监管的不太完善的问题,已上市的药-药共晶,均实现了药-药协同作用,且均按1类新药申报注册。 笔者认为,药-药共晶产业化研究,其意义不仅仅在于改善溶解度、稳定性等方面,其更重要的意义在于:发现已有药物之间、或者已有药物与创新活性分子之间的协同临床价值作用,实现1+1>2的临床应用。 2 药-药共晶“特性”是什么? 药-药共晶与复方制剂特性比较 药-药共晶与复方制剂同属于联合用药范畴。复方制剂是两种或多种活性药物成分(APIs)组成的物理混合,复方的底色是“物理混合”,溶解溶出特性是物理叠加。复方制剂的“物理混合过程”会存在如下问题:物理混合后稳定性会下降、API-API溶解度差异大造成不相容问题、API之间理化差异导致开发过程中控制多组分API的比例和分散性存在困难等。 药-药共晶是“超分子复合物”,API-API之间通过“氢键、π-π堆积”等弱相互作用存在同一个晶胞参数中。药-药共晶属于纯物质范畴,不会存在上述“复方开发中物理混合”导致的问题。最重要的是,药-药共晶的溶解特性符合“弹跳-伞降模型”(图3),可显著调控两组API药物溶解度、溶出速率,进而可能影响药代动力学曲线,达到“预想不到”的临床效果。如图4曲马多-塞来昔布,溶出显著改变,易溶组分曲马多API溶出变慢,难溶BCS II类组分塞来昔布溶出显著提高。(专利保护的共晶协同作用)
图3 弹跳-伞降模型示意图
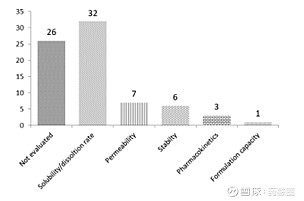
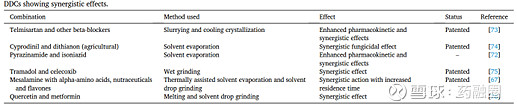
图4 盐酸曲马多-塞来昔布共晶(CTC-红色线)与单药溶出对比图 3 药-药共晶开发的技术挑战点有哪些? 选择大于努力:API-API组合的选择 选择合适的药物组合开发共晶,本身就是巨大的挑战。茶碱-苯巴比妥2:1的药-药共晶(theophylline-phenobarbitalin)学术界研究的非常火热,二者分子中存在典型的氢键链接位点,容易设计形成共晶。但茶碱是哮喘用药,苯巴比妥是神经系统用药,二者的设计组合无任何临床治疗应用支持,更有甚者,茶碱通过肝酶代谢,苯巴比妥作为CYP诱导剂,使得共晶中茶碱的药物浓度低于治疗窗口。 从实际治疗角度出发,药企的小伙伴们,肯定会明智想到,选择已上市和在研的复方制剂中的API组合,或者已有临床实践的联合用药中API组合来设计共晶。但常常这类限定的组合,形成共晶的难度会非常大。矛盾就是:从分子层面设计的共晶,实际应用堪忧,而实际应用有数据支持的分子,往往很难有形成共晶典型“位点”。 运气加成:剂量相容性问题 药-药共晶API-API是以特定化学计量比分布在晶胞结构,即API-API间具有特定的化学计量比如1:1,1:2或2:1等。但多药治疗方案中,存在一个治疗有效的合适比例范围。共晶中API-API的化学计量比,可能与临床应用的比例不一致。如抗病毒药物拉米定和齐多夫定都是抗病毒药物,二者联合用药口服剂量质量比是1:2,但拉米夫定-齐多夫定只开发出化学计量比为1:1的共晶(转化为质量比为1:1.2),这个药-药共晶进一步临床开发评估可能无比的脑壳疼。 不可预测性:1+1>2的药-药协同作用 据统计,见报道的药物共晶有几千个,但药-药共晶相对稀少。药-药共晶制备、表征、纯化放大、质控以及共晶解离控制,难度均远高于普通共晶。药-药共晶的效果本身不可预测,文献中统计了近十年报道的63个药-药共晶,多达26个药-药共晶相较于单药无任何改善效果。前面强调过,单纯改善药物溶解度、稳定性可以用的手段很多,药物-药物共晶开发重点是实现1+1>2的临床应用,获取低风险、低投入但高回报的新药申报途径,文献报道的有协同作用的药物如下图5。挑战和机遇总是伴生:LCZ696重磅炸弹药,共晶专利到期2026年11月;盐酸曲马多-塞来昔布,共晶专利到期2030年4月;国产S086沙库巴曲- EXP3174共晶专利到期2036年,药-药共晶大大延长了老药的生命周期。
图5 文献统计药-药共晶效果(来源文献4)
图6 文献报道的具有协同作用的药-药共晶((来源文献3) 药-药共晶能不能火?在晶体工程领域,药物共晶的研究一直非常火热,虽然上市的普通共晶和药-药共晶都是个位数。但笔者认为,产业应用中,药-药共晶的关注度会高于普通共晶。因为普通共晶主要是改善理化性质,只要最终固态形式满足要求,从业人员是不太关注其到底是按盐还是共晶申报,但药-药共晶则被寄予了“拓展全新的疾病治疗领域”的厚望。 只能说挑战机遇共存,期待更多药-药共晶被设计和开发吧。 本文中代表个人个人观点,如有纰漏,还望不吝赐教哈。 参考文献: [1] FDA, Guidance for industry – regulatory classification of pharmaceutical co-crystals. 2018. [2] EMA. Reflection paper on the use of cocrystals of active substances in medicinal products. 2015 (网页链接 Accessed on: 5 Jan 2018) [3] Banerjee M, Nimkar K, Naik S, et al. Unlocking the potential of drug-drug cocrystals–a comprehensive review[J]. Journal of Controlled Release, 2022, 348: 456-469. [4] Wang X, Du S, Zhang R, et al. Drug-drug cocrystals: opportunities and challenges[J]. Asian journal of pharmaceutical sciences, 2021, 16(3): 307-317. [5] Co-crystal of tramadol-celecoxib: preclinical and clinical evaluation of a novel analgesic $信立泰(SZ002294)$ #新药研发# |
【本文地址】