| 高中化学原电池与电解池知识点总结(可下载,打印) | 您所在的位置:网站首页 › 高考化学常见知识点归纳 › 高中化学原电池与电解池知识点总结(可下载,打印) |
高中化学原电池与电解池知识点总结(可下载,打印)
|
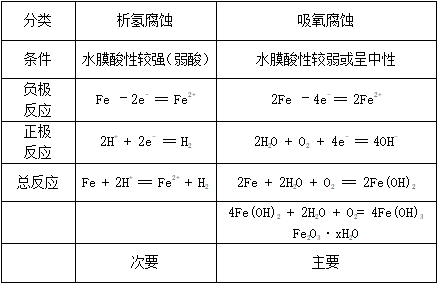
总反应: Zn+Cu2+== Zn2++ Cu ☆ 写电池符号应注意事项: • 正、负极:(-) 左, (+) 右 • 界面“|”: 单质与“极棒”写在一起,写在“|”外面。 • 注明离子浓度(c),气态时用分压(p),物质状态:固态(s), 液态(l) 等 • 盐桥: “||” 三、金属腐蚀与防护: 1.金属腐蚀:金属(或合金)跟周围接触到的气体(或液体)反应而腐蚀损耗的过程。 ⑴ 本质:金属原子失电子而被氧化 M – ne- ====Mn+ (2) 分类: ①化学腐蚀: 金属与其他物质 直接氧化反应 金属被氧化 (不是电解质溶液)(无电流产生) ②电化腐蚀: 不纯金属或合金发生原电池反应 活泼金属被氧化 电解质溶液 (有电流产生) ⑶钢铁腐蚀:
2.金属腐蚀的防护 ⑴ 金属腐蚀的原因:金属本身的组成和结构是锈蚀的根据;外界条件(如:温度、湿度、与金属接触的物质)是促使金属锈蚀的客观因素。 ⑵ 防护: ①改变金属内部组成结构,可以增强金属耐腐蚀的能力。如:不锈钢。 ② 在金属表面覆盖一层保护层,以断绝金属与外界物质接触,达到耐腐蚀的效果。(油脂、油漆、搪瓷、塑料、电镀金属、氧化成致密的氧化膜) ③电化学保护法:牺牲阳极阴极保护法、外加电流阴极保护法。 四、电解及其应用 1.电解的原理: 使电流通过电解质溶液而在阴、阳两极上引起氧化还原反应的过程叫做电解。 电解质在溶解或熔化状态下电离出自由离子,通电时,自由移动的离子定向移动,阳离子移向阴极,在阴极获得电子发生还原反应;阴离子移向阳极,在阳极失去电子发生氧化反应。电解质导电过程就是电解过程。 2.电解反应离子放电顺序(不考虑浓度等其他因素) 放电:阳离子得电子而阴离子失电的过程。 上述顺序基本上与金属活动顺序一致,即越活泼的金属,其阳离子越难结合电子,但Fe3+氧化性较强,排在Cu2+之前。 ⑵阴离子放电顺序 (注明:若阳极材料是金属(除Pt、Au外),电极首先发生氧化反应而进入溶液。) 3.电镀:利用电解原理在某些金属表面镀上一层金属或合金的过程,金属叫镀件,薄层镀层。 阴极:镀件→待镀金属 阳极:镀层金属 电镀液:含有镀层金属离子的溶液。 五、几种常见新型原电池 1.铅蓄电池 (-)Pb|PbSO4(s)|H2SO4(aq)| PbSO4(s)|PbO2(+) Pb + PbO2+ 2H2SO42PbSO4+ 2H2O 2. 燃料电池 新型电池中,电极的导电材料一般多孔的金属板,负极是通入还原剂的一方,正极是通入氧化剂的一方. 如:氢氧燃料电池,电解质溶液为30%的氢氧化钾溶液: 正极:O2+ 4e- + 2H2O=== 4OH- 负极:2H2–4e-+ 4OH-===4H2O 又如:甲烷燃料电池;电解质溶液为氢氧化钾溶液: 正极:2O2+ 8e-+ 4H2O ==8OH- 负极:CH4+ 10OH--8e- ==CO2- 3 + 7H2O 总反应:CH4+ 2O2+ 2OH-== CO2- 3 + 3H2O 铅蓄电池(充电) 阳极:PbSO4- 2e- + 2H2O == PbO2+ SO42-+ 4H+ 阴极:PbSO4+ 2e-== Pb + SO42- 总反应式:2PbSO4+ 2H2O Pb + PbO2+ 4H++ 2SO42- 铅蓄电池(放电) 正极 (PbO2) :PbO2+ 2e-+ SO42-+ 4H+== PbSO4↓ + 2H2O 负极 (Pb) :Pb - 2e-+ SO42-== PbSO4↓ 总反应式:Pb + PbO2+ 4H++ 2SO42-== 2PbSO4↓ + 2H2O 银锌纽扣电池(碱性介质) 正极 (Ag2O) :Ag2O + H2O + 2e-== 2Ag + 2OH- 负极 (Zn) :Zn + 2OH--2e-== ZnO + H2O 总反应式:Zn + Ag2O == ZnO + 2Ag Al─NaOH─Mg原电池 正极:6H2O + 6e-== 3H2↑ + 6OH- 负极:2Al - 6e-+ 8OH-== 2AlO2-+ 4H2O 总反应式:2Al + 2OH-+ 2H2O == 2AlO2-+ 3H2↑ ▍来源:本文来源网络,版权归相关权利人所有,如侵权,请联系删除返回搜狐,查看更多 |
【本文地址】