| 醋酸解离常数的测定实验报告(八篇) | 您所在的位置:网站首页 › 酸度计的使用及ph的测定 › 醋酸解离常数的测定实验报告(八篇) |
醋酸解离常数的测定实验报告(八篇)
|
实验六 醋酸电离度和电离常数的测定―pH法 一、实验目的 1.测定醋酸的电离度和电离常数; 2.学习pH计的使用。 [教学重点] 醋酸的电离度、电离常数的测定 [教学难点] pH计的使用 [实验用品] 仪器:滴定管、吸量管(5mL)、容量瓶(50 mL)、pH计、玻璃电极、甘汞电极 药品:0.200 mol·L-1HAc标准溶液、0.200 mol·L-1NaOH标准溶液、酚酞指示剂、标准缓冲溶液(pH=6.86、pH=4.00) 二、基本原理 HAc → H++ Ac- C:HAc的起始浓度;[H+]、[Ac-]、[HAc]:分别为平衡浓度; α:电离数;K:平衡常数 α = Ka = 当α小于5时,C - [H+]≈C,所以Ka≈ 根据以上关系,通过测定已知浓度HAc溶液的pH值,就可算出[H+],从而可以计算该HAc溶液的电离度和平衡常数。(pH=-lg[H+],[H+]=10-pH) 三、实验内容 1.HAc溶液浓度的测定(碱式滴定管) 以酚酞为指示剂,用已知浓度的NaOH溶液测定HAc的浓度。 
2.配制不同浓度的HAc溶液 用移液管或吸量管分别取2.50 mL、5.00 mL、25.00 mL已测得准确浓度的HAc溶液,分别加入3只50 mL容量瓶中,用去离子水稀释至刻度,摇匀,并计算出三个容量瓶中HAc溶液的准确浓度。将溶液从稀到浓排序编号为:1、2、3,原溶液为4号。 3.测定HAc溶液的pH值,并计算HAc的电离度、电离常数 把以上四种不同浓度的HAc溶液分别加入四只洁净干燥的50 L杯中,按由稀到浓的顺序在pH计上分别测定它们的pH值,并记录数据和室温。将数据填入下表(p.129.),计算HAc电离度和电离常数。 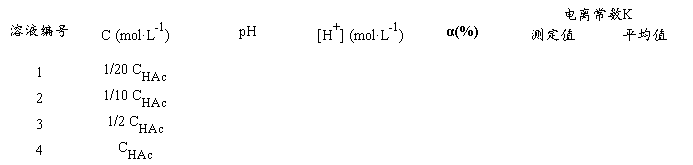
K值在1.0×10-5~2.0×10-5范围内合格(文献值25℃1.76×10-5) …… …… 余下全文 |
【本文地址】
 × 100%
× 100%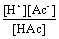 =
=