| 分析化学实验 过氧化氢含量的测定 实验报告 | 您所在的位置:网站首页 › 过氧化氢含量的测定实验计算题 › 分析化学实验 过氧化氢含量的测定 实验报告 |
分析化学实验 过氧化氢含量的测定 实验报告
|
分析化学实验 过氧化氢含量的测定 实验报告
时间:2024.7.5
实 验 报 告 姓名: 班级: 同组人: 项目 过氧化氢含量的测定 课程: 分析化学 学号: 一、实验目的 1. 了解高锰酸钾标准溶液的配制方法和保存条件。 2. 掌握以Na2C2O4为基准物标定高锰酸钾溶液浓度的方法原理及滴定条件。 3. 掌握用高锰酸钾法测定过氧化氢含量的原理和方法。 二、实验原理 标定高锰酸钾溶液的基准物质有H2C2O4·2H2O、Na2C2O4、FeSO4·7H2O、(NH4)2SO4·6H2O、As2O3和纯铁丝等。由于前两者较易纯化,所以在标定高锰酸钾时经常采用。 本实验采用Na2C2O4标定预先配好的浓度近0.02mol/L的高锰酸钾溶液,两者反应方程式如下:2KMnO4+5Na2C2O4+8H2SO4===2MnSO4+8H2O+10CO2↑+5Na2SO4+K2SO4 H2O2是一种常用的消毒剂,在医药上使用较为广泛。在酸性条件下,可用KMnO4标准溶液直接测定H2O2,其反应如下:2MnO4-+5H2O2+6H+=2Mn2++5O2+8H2O 此反应可在室温下进行。开始时反应速度较慢,随着Mn2+的产生反应速度会逐渐加快。因为H2O2不稳定,反应不能加热,滴定时的速度仍不能太快。测定时,移取一定体积H2O2的稀释液,用KMnO4标准溶液滴定至终点,根据KMnO4溶液的浓度和所消耗的体积,计算H2O2的含量。 注:1.用KMnO4溶液滴定H2O2时,不能用HNO3或HCl来控制溶液酸度。 2.H2O2样品若系工业产品,常加入少量乙酰苯胺等稳定剂,这时会造成误差,可改用碘量法测定。 三、仪器和药品 仪器:电子天平、称量瓶、50mL酸式滴定管、10、25、50mL移液管、 50mL量筒、电炉、2 mL刻度吸管、250mL容量瓶 试剂: 3mol·L-1 H2SO4 、0.02 mol·L-1 KMnO4 标准溶液、Na2C2O4、 过氧化氢样品(质量分数约为30%) 四、内容及步骤 1、0.02 mo·L-1 KMnO4溶液的配制 用台秤称取约1.7g KMnO4溶于500 mL水中,盖上表面皿,加热煮沸1h,煮时及时补充水。静置一周后,用玻璃砂芯漏斗过滤,保存于棕色瓶中待标定。 2、KMnO4溶液浓度的标定 准确称取0.15~0.20g Na2C2O4基准物质于250mL锥形瓶中,加水约20mL使之溶解,再加10mL3mol·L-1的H2SO4溶液,并加热至75~85℃,立即用待标定的KMnO4溶液滴定,滴至溶液呈淡红色并经30s不褪色,即为终点。平行测定3次,根据滴定所消耗KMnO4溶液体积和基准物的质量,计算KMnO4溶液的浓度。 3、样品的测定 用移液管吸取市售的过氧化氢样品(质量分数约为30%)2 mL,置于250mL容量瓶中,加水稀释至标线,充分混合均匀。 再吸取稀释液25.00mL,置于250mL锥形瓶中,20~30mL水和3 mol·L-1H2SO410mL,用KMnO4标准溶液滴定至溶液呈粉红色并经30s不褪色,即为终点。根据KMnO4标准溶液用量,计算未经稀释的样品中H2O2的质量浓度(用g·mL-1表示) 五、实验结果记录与计算 1、KMnO4溶液浓度的标定 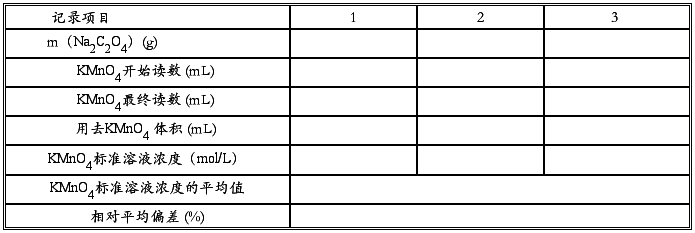
2、过氧化氢的含量的测定 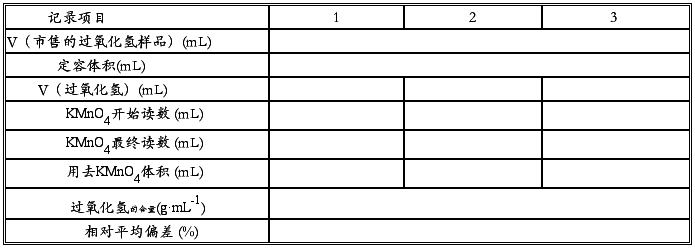
六、思考题: 1.用Na2C2O4标定KMnO4溶液浓度时,酸度过高或过低有无影响?溶液的温度过高或过低有什么影响? 2.用KMnO4法测定H2O2时,为什么不能用HNO3或HCl来控制溶液的酸度? 教师评语: 年 月 日 第二篇:过氧化氢含量的测定_实验报告实验一 过氧化氢含量的测定(高锰酸钾法) 一、 实验目的 (1) 掌握高锰酸钾法测定过氧化氢含量的原理、滴定条件和操作步骤; (2) 掌握移液管及容量瓶的正确使用方法,熟悉液体样品的取样和稀释操作。 二、 实验原理 由于在酸性溶液中,KMnO4的氧化性比H2O2的氧化性强,所以,测定H2O2的含量时,常采用在稀硫酸溶液中,室温条件下用高锰酸钾法测定。其反应为: 5H2O2+2MnO4-+6H+=2Mn2++8H2O+5O2 开始反应缓慢,第1滴溶液滴入后不易褪色,待产生Mn2+后,由于Mn2+的催化作用,加快了反应速率,故滴定速度也应加快,直至溶液呈微红色且半分钟内不退色,即为终点。根据高锰酸钾浓度和滴定中消耗KMnO4的体积, WH2O2= C1/5KMnO4(VKMnO4-V空)×10-3×M1/2 H2O2×100%/M样品×0.1 ρH2O2= C1/5KMnO4(VKMnO4-V空)×10-3×M1/2 H2O2×1000/V样品×0.1 式中p(H2O2)――H2O2的质量浓度,g/L。 三、 仪器与试剂 仪器:移液管(25ml),吸量管(10ml),洗耳球,容量瓶(250ml),酸式滴定管(50ml). 试剂:工业H2O2样品,C1/5KMnO4=0.3mol/L标准溶液,H2SO4(3mol/L)溶液。 四、 实验步骤
2.H2O2的含量测定 用吸量管吸取2mlH2O2样品(约为2g),置于250ml容量瓶中,加水稀释至标线,混合物均匀。用移液管准确移取25.00ml过氧化氢稀释液三份,分别置于三个250ml锥形瓶中,各加20mlH2SO4(3mol/L),用高锰酸钾标准溶液滴定。开始反应缓慢,待第一滴高锰酸钾溶液完全褪色后,再加入第二滴,随着反应速度的加快,可逐渐增加滴定速度,直到溶液呈为微红色且半分钟内不退色,即为终点。计算未经稀释样品中的含量。 五、实验记录与处理 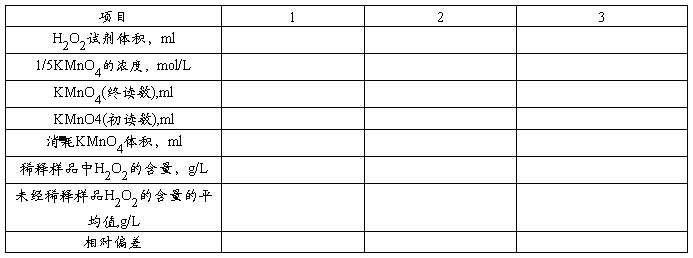 更多相关推荐:
高锰酸钾法测定过氧化氢含量实验报告
更多相关推荐:
高锰酸钾法测定过氧化氢含量实验报告
高锰酸钾法测定过氧化氢含量实验报告一实验目的1了解高锰酸钾标准溶液的配制方法和保存条件2掌握以Na2C2O4为基准物的标定高锰酸钾溶液浓度的方法原理及滴定条件3掌握用高锰酸钾法测定H2O2含量的原理和方法二实验... 过氧化氢含量的测定 实验报告实验一过氧化氢含量的测定高锰酸钾法一实验目的1掌握高锰酸钾法测定过氧化氢含量的原理滴定条件和操作步骤2掌握移液管及容量瓶的正确使用方法熟悉液体样品的取样和稀释操作二实验原理过氧化氢H2O2在工业生物医药等方面应... 过氧化氢含量的测定过氧化氢含量的测定一实验目的1掌握用KMnO4法直接滴定H2O2的基本原理和方法2掌握用吸量管移取试液的操作二实验原理在强酸性条件下KMnO4与H2O2进行如下反应2KMnO45H2O23H2SO42MnSO4... 实验报告格式-过氧化氢含量的测定实验报告格式实验日期实验地点指导教师实验名称过氧化氢含量的测定一实验目的1掌握高锰酸钾标准溶液的配制和标定方法2掌握用高锰酸钾法测定过氧化氢含量的原理和方法二实验原理写有关反应及计算公式22MnHCO标定反应5... 过氧化氢含量的测定_实验报告实验一过氧化氢含量的测定高锰酸钾法一实验目的1掌握高锰酸钾法测定过氧化氢含量的原理滴定条件和操作步骤2掌握移液管及容量瓶的正确使用方法熟悉液体样品的取样和稀释操作二实验原理1由于在酸性溶液中KMnO4的氧化性比... 3%过氧化氢含量测定实验方案H2O2含量的测定一、实验目的1.理解用KMnO4法测定H2O2的原理。2.掌握用KMnO4法测定H2O2的方法。二、仪器与试剂仪器:刻度吸管(2ml)、酸式滴定管、锥形瓶。试剂:KMnO4滴定液(0.lmol… 化学实验报告 实验__过氧化氢含量的测定实验报告姓名班级同组人自评成绩项目过氧化氢含量的测定课程分析化学学号一实验目的1了解高锰酸钾标准溶液的配制方法和保存条件2掌握以Na2C2O4为基准物标定高锰酸钾溶液浓度的方法原理及滴定条件3掌握用高锰酸钾法测... 过氧化氢的催化分解实验报告过氧化氢的催化分解一、实验目的:1.用静态法测定H2O2分解反应的速度常数和半衰期。2.熟悉一级反应特点,了解反应物浓度、温度、催化剂等因素对一级反应速度的影响。3.掌握量气技术和体积校正,学会用图解计算法求出… 实验报告探究不同条件下过氧化氢的分解实验比较过氧化氢在不同条件下的分解目的要求通过比较过氧化氢在不同条件下分解的快慢了解过氧化氢酶的作用和意义实验材料新鲜的质量分数为20的肝脏如猪肝鸡肝研磨液新配制的体积分数为3的过氧化氢溶液质量分数为35的Fe... 实验14 过氧化氢催化分解反应速率常数的测定第次课4学时实验14过氧化氢催化分解反应速率常数的测定一、实验目的1.测定过氧化氢催化分解反应速率常数;2.掌握通过测量反应系统的体积跟踪反应系统浓度从而研究反应速率的方法。二、实验原理过氧化氢在没有催化剂存在… 实验二 过氧化氢的测定实验二植物组织过氧化氢含量的测定一实验目的1掌握植物组织中过氧化氢含量的定量测定原理2了解H2O2对植物大分子物质的损害机理二实验原理植物组织内积累的H2O2是由一些氧化酶主要是超氧化物歧化酶SOD催化超阳阴离... 水中氯的测定实验报告技能实训2水中氯化物的测定沉淀滴定法一实训目的1掌握AgNO3溶液的配制和标定2掌握用莫尔法测定水中氯化物的原理和方法二原理此法实在中性和弱碱性PH为65105溶液中以铬酸钾为指示剂以硝酸银标准溶液滴定水样中氯... 过氧化氢含量的测定实验报告(22篇) |
【本文地址】