| 贺普拉肽最新动态丨一文了解乙肝、丁肝在研创新药贺普拉肽! | 您所在的位置:网站首页 › 贺普拉肽最新消息 › 贺普拉肽最新动态丨一文了解乙肝、丁肝在研创新药贺普拉肽! |
贺普拉肽最新动态丨一文了解乙肝、丁肝在研创新药贺普拉肽!
|
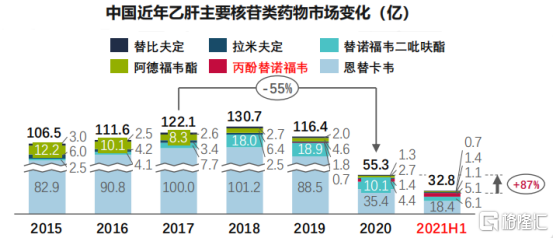
在全球范围内,慢性乙型肝炎(CHB)因乙型肝炎病毒(HBV)感染而备受关注,该病毒主要影响肝脏,引发严重的乙类传染病。据最新统计,全球范围内约有2.4亿慢性乙肝患者,其中中国患者的数量尤为显著,高达2000-3000万,每年新增的乙肝患者数量也高达100万,其中700万人因肝脏疾病严重性和罹患癌症的风险而急需治疗。 若未能及时采取有效的抗病毒治疗措施,慢性乙肝患者的病情可能会逐步恶化,从肝硬化到肝衰竭,甚至最终发展为肝癌。在中国,原发性肝癌和肝硬化患者中,由乙肝病毒引发的比例分别高达80%和60%,这一数据进一步凸显了乙肝的严重性和对中国公共卫生构成的巨大挑战。 慢性乙型肝炎药物治疗市场潜力巨大目前,干扰素和核苷(酸)类药物是临床上批准用于治疗慢性乙肝的药物。药融数据显示,核苷类似物药物市场规模从2016年的111.6亿人民币下降至2020年的55.3亿人民币,预计随着诊断率的进一步提升,核苷(酸)类药物市场将从2025年的123.3亿增长到2030年的183.7亿;随着更多创新型乙型肝炎病毒药物陆续上市,市场将开始大幅增长。
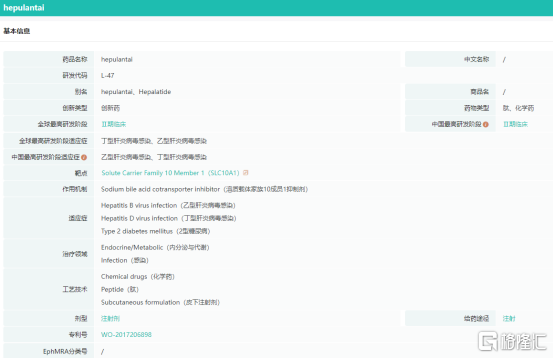
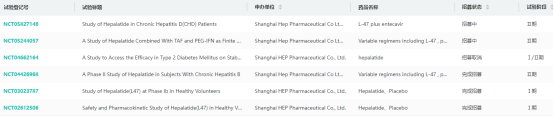
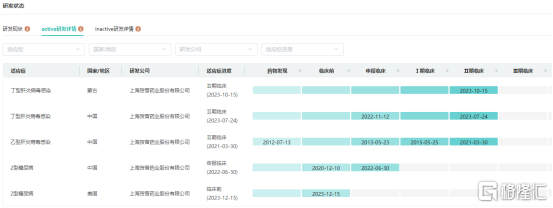
数据来源:药融云数据库 与核苷(酸)类药物单药治疗相比,序贯/联合长效干扰素的治疗策略可以提高慢性乙肝患者HBsAg的清除率,特别是部分优势患者治疗效果更显著。2021年我国长效干扰素市场容量为18.92亿元,预计到2024年增长至25.91亿元,2019-2024年CAGR为11.52%。 然而,大量的临床数据显示,干扰素在治疗48周后的标准治疗后达到程度性治愈率仅为约7%,而核苷(酸)类药物基本无法实现程度性治愈。因此,临床治疗迫切需要能够高效实现乙肝治愈的创新药物,以改善患者的治疗结局和生活质量。 在研乙肝药物主要药物类型除抑制乙肝病毒已经上市的核苷(酸)类药物及干扰素类药物外,目前尚未有全新作用机制药物获得批准上市。乙肝治疗药物在研主要药物类型包括核苷(酸)类似物、RNA干扰类药物、病毒进入抑制剂、衣壳抑制剂、HBsAg 抑制剂、反义分子、治疗性乙肝疫苗、靶向先天免疫防御途径药物、宿主靶向途径(Host Acting Pathway)药物、基因编辑等。 国产在研全新机理乙肝新药——贺普拉肽贺普拉肽作为一款有望实现慢性乙肝的程度性治愈的国产治疗药物,其研发进展一直备受关注。贺普拉肽(L47,Hepalatide)是上海贺普药业自主研发的1.1类创新化学药品,是一种来自乙肝病毒(HBV)Pre-S1衍生的47aa合成肽,可通过与肝细胞表面的HBV进入受体牛磺酸胆酸钠共转运多肽(NTCP)竞争性地结合以阻断HBV进入肝细胞。 贺普拉肽基本信息 图片来源:药融云全球药物研发数据库 贺普拉肽是全新机理的抗乙肝多肽药物,通过与HBV肝细胞感染受体钠-胆酸转运蛋白NTCP特异性结合,阻断HBV感染肝细胞,打断了乙肝现有治疗中病毒清除-再感染的反复循环,保护新生健康肝细胞,提高慢性乙肝的治疗效率。其已先后获得2项“重大新药创制”国家科技重大专项支持。 贺普拉肽有望实现乙肝功能性治愈吗?乙肝病毒(HBV)感染需要病毒进入人体后与细胞表面受体分子结合,随后渗入肝细胞内并在DNA中造成损伤。目前市场上的一些抗病毒药物主要通过抑制病毒复制来清除病毒,这些药物仅对已感染肝细胞内的HBV发挥作用,而无法保护健康的肝细胞免受HBV再次感染。 而贺普拉肽是一种新型的病毒进入抑制剂类药物,它通过抑制肝细胞表面的乙肝病毒受体,模拟健康肝细胞的受感染状态,从而限制HBV的感染能力。这就像是为病毒提供了一个“位置”,当病毒试图与肝细胞表面的受体结合并不断复制和感染新的肝细胞时,发现这个“位置”已经被贺普拉肽占据。由于“位置”已被新药占据,病毒无法找到寄生的场所,这就打破了病毒不断循环感染的过程,从而实现治愈的可能性。 贺普拉肽的疗效如何?有何优势?据药融云全球临床试验数据库收录的公开信息显示,贺普拉肽体内阻断HBV感染评价方面,显示高、中剂量组治疗9天后HBV-DNA水平均降至检测限以下,高、中、低剂量组治疗21天血清ALT(IU/ml)水平均降至检测限以下。药代研究显示贺普拉肽具有显著的肝靶向性。 注射用贺普拉肽随机、双盲、空白对照剂量递增I期临床试验,针对单纯抗HBVPre-S1抗体阳性患者,按4:1双盲、随机进入试验和对照组。PhaseIa入组患者45例,PhaseIb入组患者35例。临床试验结果显示,药物安全性优异,获得了临床推荐剂量并验证了胆汁酸升高(TBA)呈剂量依赖关系。 据I期研究公布的数据显示,贺普拉肽联合干扰素可迅速降低HBVDNA,同时降低HBsAg、ALT和HBcrAg,临床安全性优异。在2023欧洲肝病学会年会(EASL2023)上,研究人员公布了其PhaseII期临床(NCT-04426968)数据,该项研究旨在评估贺普拉肽(Hepalatide)在未经治慢乙肝患者中的安全性和有效性。 贺普拉肽全球临床试验信息查询(部分) 图片来源:药融云全球临床试验数据库 其II期临床初步数据显示,贺普拉肽(Hepalatide)与Peg-IFN联合治疗的安全性和耐受性良好。重要的是,HBVDNA水平以贺普拉肽(Hepalatide)剂量依赖的方式迅速下降,突出了其在抗HBV治疗中的治疗潜力。 贺普拉肽研发到什么进度了?2020年11月,注射用贺普拉肽(L47)联合聚乙二醇干扰素治疗HBeAg阳性慢性乙型病毒性肝炎随机、双盲安慰剂对照、多中心、量效关系Ⅱ期临床试验正式启动。 2023年5月,贺普药业顺利完成了贺普拉肽治疗慢性乙肝的II期临床试验(NCT04426968)最后1例受试者入组(lastpatientin,LPI)。该研究为一项包含96例受试者的随机双盲、安慰剂对照的临床研究,旨在探索贺普拉肽联合聚乙二醇干扰素α治疗HBeAg阳性慢性乙型肝炎的量效关系以及安全性。该临床研究预计在2023年第四季度完成,揭盲后确定贺普拉肽联合干扰素治疗乙肝的有效性。 其另一项随机双盲、安慰剂对照、多中心II期研究(NCT05244057)旨在评估三联疗法Hepalatide+聚乙二醇干扰素α +TAF对核苷经治≥ 2年的慢性乙型肝炎患者的有效性,目前正在进行受试者招募。 后续贺普拉肽将开展关键性国际多中心临床试验,根据与药监部门沟通确定的临床方案,以达到程度性治愈(HBVDNA在用药结束后6个月检测不到)为临床评价终点,达到临床终点后将有望在全球多个国家或地区进行上市注册。 贺普拉肽还在开发什么适应症?除了乙型肝炎适应症之外,2023年2月,国家药监局药品审评中心(CDE)信息显示,注射用贺普拉肽获临床试验静默许可,拟申请用于慢性丁型病毒性肝炎。这是国内企业获得的首个丁肝适应症临床批件,具有突破性的意义。丁肝在我国尚无有效治疗药物。 贺普拉肽在研适应症全球研发现状 图片来源:药融云全球药物研发数据库 目前,经中国国家药品监督管理局和蒙古国卫生部批准,贺普拉肽正在中蒙联合开展治疗丁型肝炎II期临床研究,并于2023年10月15日在蒙古国家临床研究机构完成首批7名丁肝患者临床研究入组。预期于2025年完成III期临床试验,提交中蒙首个丁型肝炎治疗药物的上市申请。 另外,贺普药业还在开发贺普拉肽的糖尿病等适应症。其治疗糖尿病已收到美国FDA糖尿病Ic/IIa临床试验申请pre-INDmeeting回复,同意提交IND申请,正在准备美国IND申报;在国内,针对其2型糖尿病适应症目前正处于申报临床阶段。 |
【本文地址】