| 病例讨论:肾穿病理电镜与光镜不符合,诊断是什么? | 您所在的位置:网站首页 › 肾病综合征病例讨论 › 病例讨论:肾穿病理电镜与光镜不符合,诊断是什么? |
病例讨论:肾穿病理电镜与光镜不符合,诊断是什么?
|
停雷公藤多苷,予强的松 50 mg qd+茴三硫片 25 mg tid+羟氯喹 0.2 g bid+骨化三醇+碳酸钙+瑞舒伐他汀钙片 10 mg qd,口干改善,强的松逐渐减量,2021-12 停强的松。 2022-7-4 日出现肺部感染、眼睑水肿,血压 182/100 mmHg,当地医院查 CT 示双肺肺部感染,抗 ANA 抗体 1:320、补体 C3 0.468 g/L、C4 0.0107 g/L、RF 678IU/ml、BNP>3500pg/ml,尿常规蛋白 2+、BLD 2+、尿蛋白定量 3.37-9.78 g/24 h。 当地予茴三硫片 25 mg tid+羟氯喹 0.2 g bid+骨化三醇+碳酸钙+瑞舒伐他汀钙片 10 mg qd+抗感染+汤药+雷贝拉唑、米格来宁、头痛宁胶囊+胆石颗粒+利速尿,浮肿加重蔓延全身,尿量减少,体重 1 周内增加 10 Kg,出现夜间胸闷憋气不能平卧,2022-7-14 日入我院免疫风湿科。 入院查体:体温 38.1℃,血压 160/90 mmHg,体重 61.5 Kg,身高 1.55m,BMI 25.6。半卧位,贫血貌,双眼睑水肿明显。听诊两肺呼吸音粗, 可闻及明显湿性啰音,右肺明显。心脏各瓣膜未闻及病理性杂音,腹部移动性浊音阴性,双下肢重度对称凹陷性浮肿。尿量 2600 ml/日。未见眼底出血及渗出。 入院化验:WBC15.15x109/L、Hb98 g/L、PLT239x109/L,ALB 28.8 g/L、Scr248.1umol/L、sCRP152.11 mg/L、CO2CP18.1 mmol/L,抗 ANA 抗体 1:80、抗 SSA/52KD 抗体 3+,抗 dsDNA 抗体及抗 Sm 抗体阴性、抗 SSA/60KD、抗体抗 SSB 抗体、抗 U1RNP 抗体阴性,抗 ANCA 抗体阴性、抗 MPO 抗体 5.84、抗 PR3 7.41,抗 GBM 抗体阴性。RF 27.8IU/ml、补体 C3 0.6 g/L、C4 0.01 g/L、IgG 1.96 g/L。 甲功正常。乙肝丙肝抗原及 HIV、梅毒抗体阴性、HBeAb 及 HBcAb 阳性,肿瘤全套阴性。 血气:pH 7.392、二氧化碳分压 28.7 mmHg、氧分压 56.2 mmHg、氧饱和度 88.5%、血 Hb 10.0 g/dL、乳酸 0.5 mmol/L、细胞外剩余碱 -7.4 mmol/L、血渗透压 262.7mosm/kg。 尿常规 PH5.0、蛋白 3+、尿潜血 3+、尿糖 2+、尿蛋白定量 4.73-7.72 g/24 h。 入院检查: B 超:胸腔、腹腔、心包积液,甲状腺结节(良性)。 胸部 CT: 1. 双肺轻度间质性改变,双肺多发支气管轻度扩张。 2. 双肺多发斑片状实变影,双肺肺部感染。 3. 胸腔积液。 4. 心包积液。 入院诊断: 1、急性肾损伤 3 期; 2、肾病综合症; 3、原发性干燥综合征; 4、急性心功能不全; 5、肺部感染; 6、呼吸衰竭; 7、高血压病 3 级(很高危); 8、高脂血症; 9、缺铁性贫血; 10、胆囊结石 胆囊炎 诊疗经过 2022-7-14 日入院后予莫西沙星+ 头孢哌酮钠舒巴坦钠抗感染+ 呋塞米40-80 mg qd+螺内酯 40 mg qd+拜新同 30 mg bid+茴三硫片 25 mg tid+羟氯喹 0.2 g bid,尿量逐步增多,浮肿消退。 2022-7-16 日体温正常,36.5℃,2022-7-24 日复查胸片肺部感染炎症吸收,予停莫西沙星及 头孢哌酮钠舒巴坦钠。 2022-7-24 日予甲泼尼龙 40 mg qd 静滴,2022-7-27 日予甲泼尼龙 24 mg qd 静滴,2022-8-2 日改为 24 mg qd 口服。 2022-8-10 日血 WBC 8.0x109/L、Hb 97 g/L、PLT 227x109/L TP 41.9 g/L、ALB 26.5 g/L、Scr 134umol/L、GLU 3.66 mmol/L、CO2CP 25.5 mmol/L、S-CRP 13.7 mg/L、RF 15.2IU/ml、Fe 4.75umol/L↓、血清未饱和铁结合力 19.3umol/L↓、总铁结合力 24.09 umol/L↓、铁饱和度 19.9%↓,尿常规:尿糖 1+、尿蛋白 2+、RBC 865.90/ul、WBC 5.90/ul、尿蛋白定量 9.78 g/d。尿量 2500 ml/日左右。 2022-8-11 日肾穿活检。 2022-8-11 予蔗糖铁注射液+甲泼尼龙 24 mg/日+呋塞米片 40 mg qd+螺内酯 40 mg qd+硫酸羟氯喹 0.2 g bid+硝苯地平控释片 30 mg bid,尿量 2600-3000 ml/日。 2022-8-11 肾穿刺病理: 光镜诊断:1. 膜增生性肾小球肾炎(免疫复合物介导),冷球蛋白血症肾损害等继发性肾炎待除外;2. 血栓性微血管病肾损伤。 考虑光镜切片偏厚, 重新切片染色。第一次切片 PAS 染色及 PASM 图片和重新切片相比,同一肾小球图片可以看出第一次切片厚 ,染色也偏深,尤其是 PAS 染色显示切片厚。 光镜描述:7 个肾小球,其中 1 个球性硬化,其余肾小球系膜细胞和基质中至重度弥漫增生,小球呈结节分叶状改变,节段毛细血管内细胞增多伴少量中性粒细胞浸润,基底膜弥漫增厚伴双轨症,Masson 染色可见内皮下及系膜区嗜复红蛋白沉积;肾小管上皮空泡及颗粒变性,灶状刷毛缘脱落,管腔扩张、腔内见多数红细胞及少数蛋白管型;肾间质水肿,多灶状淋巴细胞和单核细胞浸润;小动脉管壁增厚,内膜黏液样变性及节段纤维素样坏死,管腔狭窄及闭塞。 重新切片光镜诊断: 1、膜增生性肾小球肾炎(免疫复合物介导),冷球蛋白血症肾损害等继发性肾炎待除外;2、TMA 样肾损伤。 向下滑动查看
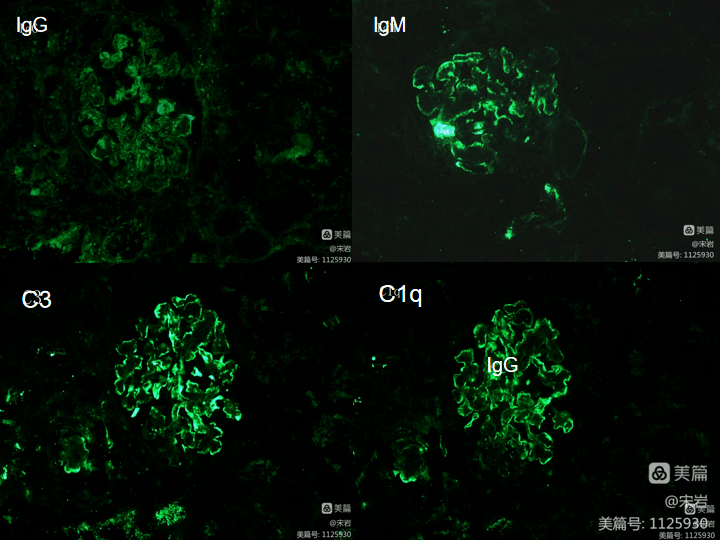
光镜:可见 12 个肾小球,其中 1 个球性硬化,余肾小球系膜细胞和基质轻到重度弥漫性增生,有 8 个小球呈结节分叶状改变,节段毛细血管内细胞增多伴少量中性粒细胞浸润,基底膜弥漫增厚伴双轨征,有 3 个小球轻度系膜细胞和基质增生,无结节分叶状改变,部分小球基底膜缺血皱缩,其中 1 个小球血管袢内可见微血栓形成,Masson 染色可见内皮下及系膜区嗜复红蛋白沉积。 肾小管上皮空泡及颗粒样变性,灶状刷毛缘脱落,管腔扩张,部分小管上皮细胞崩解,可见裸基底膜,肾小管腔内见较多红细胞管型及少数蛋白管型。肾间质水肿,多灶状淋巴单核细胞浸润。小动脉内膜粘液样变性及节段纤维素样坏死,管腔狭窄及闭塞。 病例特点 1. 52 岁女性,口干 2 年眼睑水肿伴血压升高 10 天,临床为干燥综合征+AKI+肾综,无光敏感及口腔溃疡,雷诺氏征阴性,无皮疹。 2. 抗 ANA 抗体 1:320-80、抗 SSA 抗体阳性,补体 C3、C4 均低,抗 dsDNA 抗体及抗 SM 抗体阴性,RF441-217-144-678-33.8-27.8IU/ml。 3. 血压最高 182/100 mmHg,无视物模糊,入院眼底检查未见出血渗出。 4. 免疫荧光:IgG 1+、IgM 3+、C3 3+、IgA -、C1q 2+,系膜区团块状、毛细血管袢颗粒样沉积。 向下滑动查看 可见 3 个肾小球,IgG 1+、IgM 3+、C3 3+、IgA -、C1q 2+,阳性物质系膜区团块状及毛细血管袢颗粒样沉积。
5. 光镜:12 个肾小球可见一个小球血管袢见微血栓形成,11 个肾小球病变不均一,有 3 个小球未见系膜插入形成的双轨。诊断: MPGN(免疫复合物介导),冷球蛋白血症肾损害等继发性肾炎待除外; 血栓性微血管病肾损伤。电镜:系膜增生性肾小球肾炎,伴内皮细胞损伤改变,未见到冷球栓子及亚结构、系膜插入形成的 双轨。 MPGN(免疫复合物介导),冷球蛋白血症肾损害等继发性肾炎待除外; 血栓性微血管病肾损伤。电镜:系膜增生性肾小球肾炎,伴内皮细胞损伤改变,未见到冷球栓子及亚结构、系膜插入形成的 双轨。 6. 电镜与光镜诊断不符合。 这例的小球病变不均一,基底内疏松层大部分轻度增宽可能是高血压和血管病变引起的内皮细胞损伤所致。可见 MPGN 是一组类似于肾病综合征样的病理上描述的综合征,按发病机制分为免疫复合物介导型、补体介导和 TMA 样病变引起的,并不是一个病,诊断 MPGN 首先要除外 lgAN 和 LN 等继发的 MPGN 样病变。 光镜诊断 MPGN 样病变更合理。 向下滑动查看
PAS 染色下 11 个没有硬化的肾小球的病变,有的肾小球系膜细胞和基质增生不明显,没有系膜插入和双轨。
小球分叶样改变,系膜细胞和基质中-重度系膜增生,系膜细胞和基质插入形成双轨,也可见没有系膜细胞和基质插入的双轨征。
系膜细胞和基质明显增生,系膜细胞和基质插入形成双轨。
肾小球呈分叶状,弥漫性重度系膜细胞增生伴内皮细胞增生,系膜细胞和基质增生插入形成双轨征,可见微血栓形成。
7 点钟位置见微血栓形成。
无明显系膜细胞和基质增生的肾小球。
无明显系膜细胞和基质增生的小球,未见双轨征。
有基底膜增厚和假双轨征,但无明显系膜插入形成的双轨征。
无明显系膜细胞和基质增生的小球。
小动脉内膜粘液样变性水肿,左侧小动脉纤维素样坏死。
部分小管腔内可见红细胞管型,小管上皮细胞空泡颗粒变性,可见裸基底膜,间质水肿。
右边的两个肾小球有系膜细胞和基质轻度增生,但未见系膜插入及双轨征形成。
PASM 染色的 11 个没有硬化的小球,第五张的肾小球未见系膜插入及双轨征形成。 电镜诊断:符合系膜增生性肾小球肾炎,伴内皮细胞损伤改变,请结合光镜分析。 向下滑动查看 电镜:半薄切片,2 块肾组织,可见 3 个肾小球。肾小球系膜细胞和系膜基质轻至中度增生,节段内皮细胞增生,系膜区及节段内皮下块状电子致密物沉积,基底膜内疏松层大部分轻度增宽,上皮足突大部分融合。肾小管上皮细胞空泡变性伴溶醇体增多,部分微绒毛脱落,部分萎缩。肾间质淋巴单核细胞浸润伴胶原纤维增生。 节段内皮下团块状电子致密物沉积。
足突大部分融合,内疏松层轻度增宽,提示有内皮细胞损伤。
CD68 阳性
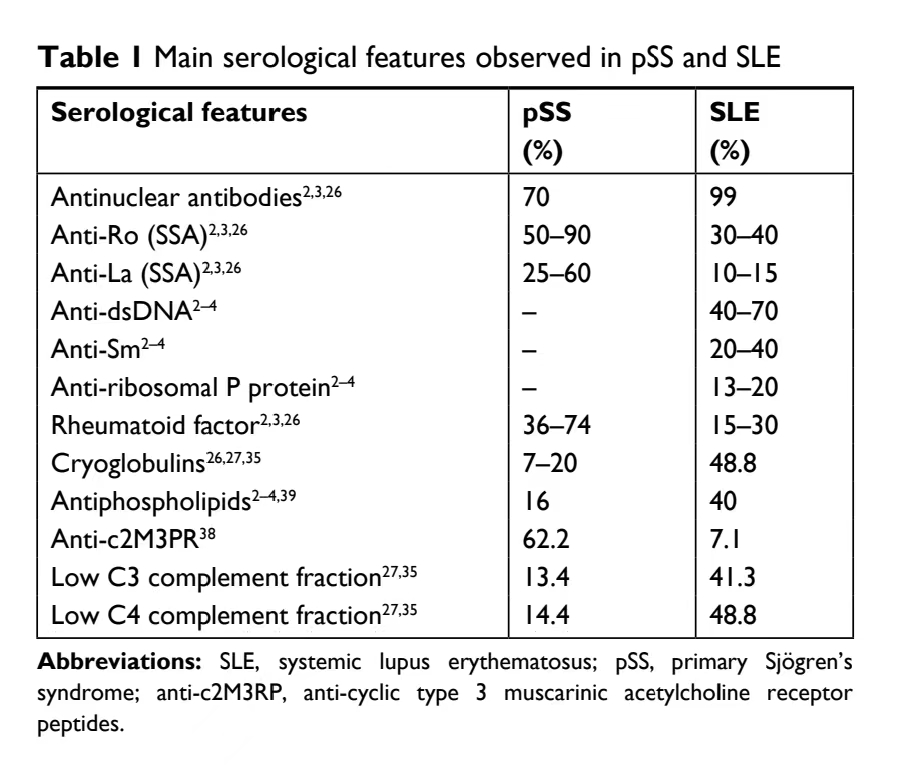
病例思考与讨论 患者的 AKI 的病因是什么? 光镜可见肾小管上皮空泡及颗粒样变性,灶状刷毛缘脱落,管腔扩张,部分小管上皮细胞崩解,可见裸基底膜,肾小管腔内见较多红细胞管型及少数蛋白管型。肾间质水肿,多灶状淋巴单核细胞浸润。 患者的 AKI 是 AIN 所致,,患者入院前曾在当地医院予服用中药汤药和解热镇痛药 10 天,考虑为药物引起的 AIN 可能性大, 光镜可见小动脉内膜粘液样变性及节段纤维素样坏死,管腔狭窄及闭塞,AIN 不能除外 TMA 样病变参与其中。 干燥综合征肾损害的病理特点有哪些? 干燥综合征的诊断标准及其肾损害的临床病理特征 2016 年 ACR/EULAR)pSS 诊断标准: 唾液腺组织中淋巴细胞灶数量 ≥1/4 mm2 3 分 √ 抗 RO(SSA)3 分 √ 眼睛染色 ≥5(至少 1 只眼睛)1 分 Schirmer 试验(≤5 mm / 5 分钟,至少 1 只眼睛)1 分 未刺激的唾液流速(≤0.1 ml/min)1 分 √ 唾液腺组织中淋巴细胞灶数量 ≥1/4 mm2 3 分 √ 抗 RO(SSA)3 分 √ 眼睛染色 ≥5(至少 1 只眼睛)1 分 Schirmer 试验(≤5 mm / 5 分钟,至少 1 只眼睛)1 分 未刺激的唾液流速(≤0.1 ml/min)1 分 √ 诊断:≥4 分即可确诊 pSS。 患者有眼干口干,抗 SSA 阳性,Schirmer 试验 0 mm/5 分钟,唾液腺组织中淋巴细胞灶数量 ≥1/4 mm2,3+1+3 = 6 分,pSS 诊断成立。 pSS 的肾脏损害以间质性肾炎常见,肾小球受累比间质性肾炎少见,pSS 肾脏受累国外报道为 5-14%,协和医院报道为 33-41.8%,肾小球病变占比国外数据为 22.3-35.9%,协和医院数据为 48.5% [1,3-5] 。 国外文献 pSS 肾小球受累以 MPGN(冷球蛋白血症所致)和 MN 为主,其它病理类型包括 MCD、IgA 肾病以及 MsPGN、FSGS 等 [1,2] 。协和医院报道 MN35.9%、MsPGN5.9%、MCD3.9%、lgAV 2.9%、FSGS 2.9% [2,3] 。 pSS 的肾脏损害以间质性肾炎常见,肾小球受累比间质性肾炎少见。患者光镜见肾间质水肿,多灶状淋巴单核细胞浸润。 干燥综合征间质性肾炎浸润的是 B 淋巴(CD20),而常见的间质性肾炎浸润的是 T 淋巴细胞(CD3)≥B 淋巴(CD20),患者多灶状的浸润细胞 B 淋巴细胞还是 T 淋巴细胞。染了肾组织的 CD20(B 淋巴细胞)和 CD3(T 淋巴细胞),患者 CD20 染色 ≥CD3,但 CD20 染色局灶阳性。考虑难以诊断干燥综合征所致慢性间质型肾炎。 怎么解释患者的光镜和电镜的病理类型不同? MPGN 是一组病理上表现相似的一组综合症,病理上可见弥漫性系膜细胞和基质增生和系膜细胞和基质插入形成双轨征的一组病理上表现相同的疾病,由于系膜细胞和基质增生造成肾小球分叶状改变,典型的 MPGN 荧光多以 lgG、C3 沉积为主。 此例光镜 12 个肾小球,除 1 个球性硬化外,有 8 个肾小球系膜细胞和基质增生明显,有系膜插入形成双轨征,肾小球呈分叶状改变,但有 3 个肾小球未见系膜细胞和基质明显增生和系膜插入的双轨征,仅 1 个小球见一个微血栓,光镜为 MPGN。 电镜小球系膜细胞和系膜基质增生,节段内皮细胞增生,内疏松层轻度弥漫性增宽,未见特殊亚结构形成,电镜符合 MsPGN,伴内皮细胞损伤改变。 光镜和电镜结果不一致考虑为肾小球病变不均一所致,即电镜通常只能看到 1 个小球,此例电镜所见肾小球病变轻所致。 患者能除外 SLE 吗?最后诊断是什么? 2019 年 EULAR/ACR SLE 诊断标准主要特点是: 进入标准:ANA ≥ 1:80(HEp-2 细胞方法); 评分标准:SLE 分类标准要求至少包括 1 条临床分类标准以及总分 ≥ 10 分可诊断。 具有更高的诊断敏感性(98%)和诊断特异性(96%)。 可以单凭肾穿诊断 SLE:肾活检病理首先明确为狼疮肾炎,其中 III 或 IV 型,特点是弥漫增殖型、可有新月体形成,分值为 10 分,可以独立诊断为 SLE,即使没有其它临床症状或/和血抗体均阴性 [6] 。 进入标准:ANA ≥ 1:80(HEp-2 细胞方法); 评分标准:SLE 分类标准要求至少包括 1 条临床分类标准以及总分 ≥ 10 分可诊断。 具有更高的诊断敏感性(98%)和诊断特异性(96%)。 可以单凭肾穿诊断 SLE:肾活检病理首先明确为狼疮肾炎,其中 III 或 IV 型,特点是弥漫增殖型、可有新月体形成,分值为 10 分,可以独立诊断为 SLE,即使没有其它临床症状或/和血抗体均阴性 [6] 。 患者抗 ANA 抗体 1:320,有胸腔积液和心包积液(5 分),但未抽胸水定性,肾穿刺病理为 MPGN,如果把 MPGN 归类为 SLE-LN,则为 IV 型 LN(10 分),补体 C3、C4 均低(4 分),总计 = 5+10+4+= 19 分,可以诊断 SLE 了。那么这例是 SLE 的 sSS 还是 pSS 呢? SLE 的抗 dsDNA 抗体和抗 Sm 抗体、抗核糖体(Po)抗体的阳性率分别为 40-70% 和 20-40%、13-20%,而 pSS 三个抗体均阴性,这也是 SLE 和 pSS 血清学的主要鉴别点。pSS 可以出现病理类型为 MPGN 病变,可以引起补体 C3、C4 降低 [7-9] 。 患者 2020-9 月至 2020-12-11 日 RF 441-217-144IU/ml,Scr 正常、尿常规及尿蛋白定量正常,2022-7 月出现肺部感染后,RF678 IU/ml,pSS 病情加重,出现肾损害:尿蛋白定量 3.37-9.78 g/d、潜血 2+,Scr 248.1,pSS 可以引起 MPGN 样病变,结合临床及病理考虑为 pSS,SLE 可以除外。 虽然 2019 年 EULAR/ACR 诊断 SLE 敏感性达 98%,诊断特异性达 96%,在诊断 pSS-冷球蛋白血症-MPGN 时需要注意假阳性。文献报道 pSS 的 MPGN 都是冷球蛋白血症所致,那么这例是冷球蛋白血症吗?
来源:参考文献 7 患者最后诊断是什么? 患者 pSS 诊断明确,临床表现为 pSS+高血压+肾综+AKI+低补体 C3、C4 血症+RF 阳性,血抗 ANA 抗体 1:320-80、抗 SSA 抗体阳性,抗 dsDNA 抗体及抗 SM 抗体阴性,RF 441-217-144-678IU/ml。 入院前出现严重肺部感染和急性心功能不全、RF 由 144 升高到 678IU/ml,提示 pSS 病情波动加重,抗感染治疗后入院查 RF33.8-27.8IU/ml。 血压最高 182/100 mmHg,眼底无出血渗出。入院后控制血压抗感染治疗后心衰及呼吸衰竭好转,Scr 即下降至 106umol/L。 病理免疫荧光以 IgM、C3、C1q 阳性为主,光镜为 pSS-MPGN,小球病变不均一,仅见一个小球血管袢见微血栓形成,均提示为冷球蛋白所致,但电镜未见到冷球栓子及亚结构。 光镜见 1 个小球血管袢有 1 个微血栓,肾组织 CD68 阳性提示冷球蛋白所致,2022-9-21 日血冷球蛋白定性试验阳性,为 II 型冷球蛋白,诊断可以明确为 pSS→ 冷球蛋白血症 →MPGN,所以临床冷球蛋白检测非常重要。 病情演变过程:2020-9 月 PSS+冷球蛋白血症(无肾脏受累)→2022-7-4 日肺部感染造成 pSS 病情反复和加重 → 冷球蛋白血症加重、RF 升高 → 引起肾脏病损害,出现表现为 MPGN 的肾病综合征。文献报道 pSS-均为冷球蛋白血症所致,冷球蛋白所致 MPGN 可以小球病变不均一 [10] ,因此,遇到小球病变不均一的 MPGN 和 pSS-MPGN 时应注意冷球蛋白血症。 2019 年 EULAR/ACR 诊断 SLE 敏感性达 98%,特异性达 96%,但对 pSS-冷球蛋白血症-MPGN 时需要注意假阳性,这例如果机械按照 EULAR/ACR 诊断标准易误诊为 SLE-LN-IV 型。 患者的 MPGN 诊断成立吗? 《肾活检病理学》上 MPGN 描述为光镜肾小球弥漫性分布,肾小球弥漫性系膜细胞和基质中重度增生沿内皮下广泛插入,PASM 基底膜呈双轨或多轨 [11] 。 Fogo《肾脏病理诊断图谱》上 MPGN 病变特征为球性和弥漫性系膜和毛细血管内增生,伴炎细胞渗出、系膜基质增生以及银 染所见的 GBM「双轨征」,肾小球血管袢呈分叶状,在原发性 MPGN 肾小球细胞增生弥漫一致,与 LN 的不规则增生有明显区别,在继发性 MPGN 中,损伤更加不规则[12] 。 这例 MPGN 样病变小球 8/12 = 67%,不够原发性 MPGN 弥漫性(≥90%)诊断标准,但文献报道冷球蛋白血症所致的 MPGN 可以出现肾小球病变不均一[10] ,患者为 pSS-冷球蛋白血症-MPGN,符合继发性冷球蛋白血症所致的继发性 MPGN 诊断标准。 MPGN 并不是一个独立疾病,而是一组病理上表现相同的一组疾病,用 MPGN 样病变比用 MPGN 更合理和准确。 最终诊断:AKI;肾病综合征;原发性干燥综合征(pSS) ,冷球蛋白血症,II 型 MPGN((冷球蛋白 GN);AIN;肺部感染;急性心功能不全;呼吸衰竭 II 型;高血压病 3 级(很高危);高脂血症;缺铁性贫血;胆囊结石;胆囊炎。 小结 患者临床为 pSS+高血压+肾综+AKI+低补体 C3、C4 血症+RF 阳性,血抗 ANA 抗体 1:320、抗 SSA 抗体阳性,抗 dsDNA 及抗 SM、抗核糖体抗体阴性,RF 441-217-144-678-27.8IU/ml。 入院前 10 天肺部感染,RF 由 144 升高到 678IU/ml,提示 pSS 病情加重,冷球蛋白血症加重,出现肾脏损害。血压 182/100 mmHg,眼底无出血渗出。 免疫荧光以 IgM、C3、C1q 阳性为主,光镜小球病变不均一,仅 1 个血管袢见微血栓形成,诊断 MPGN(免疫复合物介导),电镜未见冷球亚结构及未见系膜插入形成的双规,诊断 MsPGN,电镜与光镜诊断不符合,电镜未见 MPGN 样病变及冷球蛋白栓子和亚结构为小球病变不均一所致。 患者血冷球蛋白定性试验阳性,分型为 II 型冷球蛋白,最后诊断明确为 pSS-冷球蛋白血症-MPGN。 文献报道 pSS-均为冷球蛋白血症所致,冷球蛋白所致 MPGN 可以小球病变不均一,因此,遇到小球病变不均一的 MPGN 和 pSS-MPGN 时应注意冷球蛋白血症。 2019 年 EULAR/ACR 诊断 SLE 敏感性达 98%,特异性达 96%,但对 pSS-冷球蛋白血症-MPGN 时需要注意假阳性,这例如果机械按照 EULAR/ACR 诊断标准易误诊为 SLE-LN-IV 型。 患者弥漫增生插入双轨征的小球 8 个/12(小球总数)= 67%,不到弥漫性,但文献报道冷球蛋白血症所致 MPGN 小球病变不均一,显然符合继发性 MPGN 标准。 MPGN 不是一个独立疾病,而是一组病理上表现相同的一组疾病,用 MPGN 样病变比用 MPGN 更合理和准确。AKI 是药物引起的 AIN 可能性大,但有小动脉内膜粘液变性和节段性纤维素样坏死,不除外有冷球蛋白血管炎和高血压因素。 感谢北大一院王素霞教授、任雅丽老师、张旭老师在病理诊断上的帮助!感谢浙江中医药大学附属杭州市中医院肾脏科汤绚丽主任在病理诊断上的帮助! ✩ 本文仅供医疗卫生等专业人士参考 策划 | 静姝 投稿 | [email protected] 题图 | 站酷海洛 配图 | 作者提供 参考文献: 1.Renal involvement in primary Sjögren』 syndrome.Rev Nephrol. 2016 Feb;12(2):82-93. 2.Renal involvement in primary Sjögren』 syndrome:Aretrospective study of 103 biopsy-proven cases from asingle center in China.International Journal of Rheumatic Diseases 2017:1-7. 3.Kidney biopsy findings in primary Sjögren syndrome.Nephrol Dial Transplant. 2015 Aug;30(8):1363-9. 4.Preliminary criteria for the classification of Sjögren's syndrome. Results of a prospective concerted action supported by the European Community.Arthritis Rheum. 1993;36(3):340. 5.Renal involvement in primary Sjögren's syndrome: a clinicopathologic study.Clin J Am Soc Nephrol. 2009 Sep;4(9):1423-31. 6.2019 European League Against Rheumatism/American College of Rheumatology classification criteria for systemic lupus erythematosusAnn Rheum Dis 2019;78:1151–1159. 7.Sjögren’s syndrome and systemic lupus erythematosus: links and risks.Research and Reviews 2019:11 33–45. 8.Clinical and morphological features of kidney involvement in primary Sjögren's syndrome.Nephrol Dial Transplant. 2001;16(12):23-28. 9.Renal involvement in primary Sjögren's syndrome: a clinicopathologic study.Clin J Am Soc Nephrol. 2009 Sep;4(9):1423-31. 10.Cryoglobulinemic vasculitis and glomerulonephritis: concerns in clinical practice.Chinese Medical Journal 2019;132(14). 11. 肾活检病理诊断学: 第 6 章第 7 节. 膜增生性肾小球肾炎:116-120. 12. 肾脏病理诊断图谱: 膜增生性肾小球肾炎.75:75-86. (▲▼上下滑动查看)返回搜狐,查看更多 |
【本文地址】