| 某化学小组向一定量AgNO3 和Cu(NO3)2的混合溶液中加入一定量的Zn粉.充分反应后过滤得溶液A和固体B.滤液A中所含的溶质不可能的情况是A. Zn2 .Cu(NO3)2 .AgNO3C. Zn2 D. Zn(NO3)2 .AgNO3 D [解析]向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn粉.Zn在铜和银的前面.故Zn能与硝酸银反应生成硝酸锌 题目和参考答案 | 您所在的位置:网站首页 › 稀硫酸溶液中的溶质是什么 › 某化学小组向一定量AgNO3 和Cu(NO3)2的混合溶液中加入一定量的Zn粉.充分反应后过滤得溶液A和固体B.滤液A中所含的溶质不可能的情况是A. Zn2 .Cu(NO3)2 .AgNO3C. Zn2 D. Zn(NO3)2 .AgNO3 D [解析]向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn粉.Zn在铜和银的前面.故Zn能与硝酸银反应生成硝酸锌 题目和参考答案 |
某化学小组向一定量AgNO3 和Cu(NO3)2的混合溶液中加入一定量的Zn粉.充分反应后过滤得溶液A和固体B.滤液A中所含的溶质不可能的情况是A. Zn2 .Cu(NO3)2 .AgNO3C. Zn2 D. Zn(NO3)2 .AgNO3 D [解析]向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn粉.Zn在铜和银的前面.故Zn能与硝酸银反应生成硝酸锌 题目和参考答案
|
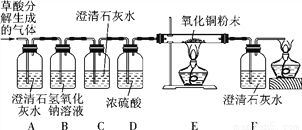
在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水。某化学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究: 【提出问题】 生成物中有哪几种碳的氧化物? 【猜想】 猜想1 猜想2 猜想3 只有CO 只有________ 含有CO和CO2 【设计实验】 基于猜想3,依据CO和CO2的性质,兴趣小组同学设计了如下实验:
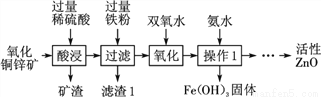
【实验探究】 (1) 观察到________(填序号)装置中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成。 (2) 有两种实验现象都能分别证明草酸分解的气体中含有CO: ① C装置中澄清石灰水不变浑浊,F装置中___________________________; ② E装置中出现_____________________________________的现象。 【实验结论】 通过实验探究证明:猜想3成立。 草酸分解的化学方程式是____________________________________________。 【问题讨论】 (1) B装置的作用是________________________;D装置的作用是__________________。 (2) 装置末端酒精灯的作用是________________________________。 (3)对装置E中玻璃管内的产物成分探究 【查阅资料】 Ⅰ. 一氧化碳还原氧化铜。除生成铜外还可能生成氧化亚铜(Cu2O); Ⅱ. Cu2O为不溶于水的红色固体; Ⅲ. Cu2O+H2SO4===CuSO4+Cu+H2O。 【提出问题】 红色固体含有什么物质? 【猜想假设】 假设一:红色固体只含Cu。 假设二:红色固体只含Cu2O。 假设三:________________________。 【实验验证】 该小组为验证上述假设,取少量红色固体,加到足量稀硫酸中,观察到溶液变为蓝色,红色固体部分溶解。 【实验结论】 根据上述实验结果,可知红色固体中一定含有________。 【数据处理】 为进一步确定红色固体的成分,甲、乙两同学分别称取各自实验后的一定质量的红色固体,加到足量稀硫酸中使其充分反应,经过滤、洗涤、干燥后,称量剩余红色固体质量如表,请完善表中内容。 实验 人员 红色 固体/g 剩余红色 固体/g 实验结论 甲 7.2 3.2 ① __________________ 乙 4.08 2.48 ② __________________ CO2 A 石灰水变浑浊 黑色粉末变红 H2C2O4CO↑+CO2↑+H2O 吸收二氧化碳 吸收水分 点燃CO,防止对空气的污染 红色固体含Cu和Cu2O Cu2O 红色固体只含Cu2O (或假设二成立) 红色固体含Cu和Cu2O(或假设三成立) 【解析】【猜想】碳的氧化物可能是一氧化碳,也可能是二氧化碳,也可能是一氧化碳和二氧化碳;【设计实验】(1)二氧化碳遇澄清石灰水,可使石灰水变浑浊...某科研小组设计利用稀硫酸浸取某废弃的氧化铜锌矿(主要成分为CuO和ZnO,其余成分既不与酸反应,也不溶解于水)的方案,实现废物综合利用。部分实验流程如图:
请根据上述实验流程回答下列问题: (1) 操作1的名称是________。 (2) 在氧化铜锌矿中加入过量稀硫酸,主要成分发生反应的化学方程式为__________________________(任写一个) (3) 加过量铁粉后,发生反应的基本反应类型是______,得到滤渣1的成分为_______(填化学式)。 (4) 在实验过程中,双氧水会与Fe2+反应生成Fe3+和水,以便在后续的操作中将溶液中铁元素除去。高锰酸钾溶液也能将Fe2+氧化成Fe3+,选用双氧水的优点是____________________________。 查看答案根据下列装置,结合所学化学知识回答下列问题:
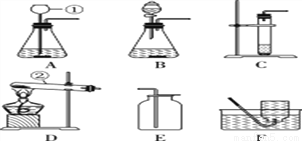
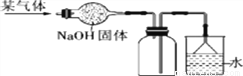
(1) 写出图中标号仪器的名称:① _______。 (2) 实验室用高锰酸钾制取氧气时,发生装置应选用________(填字母);其反应的化学方程式为__________________________。如果改用氯酸钾和二氧化锰制取氧气,反应前后二氧化锰的质量分数________(填“增大”、“减小”或“不变”)。 (3) 实验室制取少量二氧化碳时,发生装置最好选用________(填字母,下同),收集装置选用________,常用此收集方法的原因是____________________,某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能的原因______________________________________________ (4) 化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、改进装置等途径来达到控制反应的目的。常温下块状电石(CaC2)与水反应生成乙炔(C2H2)气体和氢氧化钙,该反应的化学方程式是______________________________,实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂。图中适合制取乙炔气体的发生装置有________(填装置序号)。 (5)下图是干燥、收集某气体的装置。由实验装置可以推测该气体的有关性质,请你在表中找出相对应的选项(____)
序号 气体性质 A B C D 溶于水中所得溶液的pH >7 <7 >7 <7 其密度(ρ1)与空气密度(ρ2 )的比较 ρ1>ρ2 ρ1>ρ2 ρ1<ρ2 ρ1<ρ2 在水中的溶解性 极易溶 难 溶 极易溶 难 溶 查看答案(1)化学与人类生活、生产息息相关,请回答下列问题: ①家用净水器是利用活性炭的___________性,除去有色有味的杂质; ②炒菜时油锅中的油不慎着火,可以采取的灭火方法是___________________________; ③2017年5月,我国在南海进行了天然气水合物(可燃冰)的试开采,天然气的主要成分是_________ ④胃液里含有适量盐酸,服用含氢氧化铝[Al(OH)3]药物可治疗胃酸过多症,反应的化学方程式为______________ (2)根据图文回答下列问题。
① 金刚石的________(填“硬度”或“密度”)大; ② 钠元素是人体必需的________(填“常量”或“微量”)元素; ③ 面包中淀粉属于________(填字母序号); A. 糖类 B. 蛋白质 C. 油脂 ④ 100 g该硫酸溶液中溶质的质量为________g。 查看答案某无色气体可能含有甲烷、一氧化碳、氢气中的一种或几种,依次进行下列实验(假设每步反应或吸收均完全):①无色气体在足量氧气中燃烧;②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6克;③再将剩余气体通过盛有氢氧化钠溶液的洗气瓶,装置增重4.4克。下列推断正确的是 A. 该气体可能只含有一氧化碳、氢气 B. 该气体可能只含有甲烷、一氧化碳 C. 该气体一定只含有甲烷 D. 该气体一定只含有甲烷、氢气 查看答案某化学小组向一定量AgNO3 和Cu(NO3)2的混合溶液中加入一定量的Zn粉,充分反应后过滤得溶液A和固体B,滤液A中所含的溶质不可能的情况是 A. Zn(NO3)2 B. Zn(NO3)2 、Cu(NO3)2 、AgNO3 C. Zn(NO3)2 、Cu(NO3)2 D. Zn(NO3)2 、AgNO3 查看答案 试题属性 题型:科学探究题 难度:困难 Copyright @ 2008-2013 满分5 学习网 ManFen5.COM. All Rights Reserved.答案无忧
Copyright @ 2008-2013 满分5 学习网 ManFen5.COM. All Rights Reserved.答案无忧
|
【本文地址】