| 2021 | 您所在的位置:网站首页 › 碳酸氢根共轭酸和共轭碱 › 2021 |
2021
|
一:缓冲溶液 1:同离子效应: 在一个弱电解质(弱酸或者弱碱)的平衡体系里面加入与弱电解质具有相同离子的强电解质,可以降低弱电解质的电离程度。 也即: 在弱酸溶液中加入该酸的共轭碱,或在弱碱的溶液中加入该碱的共轭酸时,可使这些弱酸或弱碱的解离度降低。 因为加入了具有相同离子的强电解质,造成了平衡左移,导致了弱电解质溶解度下降。 比如: 2: 缓冲溶液: 能抵抗外加适量的强酸,强碱或稍加水稀释而溶液的pH值基本保持不变的溶液,称为缓冲溶液 组成:弱酸,强碱弱酸盐(弱碱,强酸弱碱盐)共轭酸碱对的混合溶液。 3:缓冲溶液的作用原理: 如果向溶液中增加碱,分解的氢氧根离子会和氢离子反应生成水,此时根据平衡移动原理,右边浓度减少,反应正向移动,所以醋酸会继续分解产生氢离子以维持pH值。 可以把醋酸钠当做抗酸成分,把醋酸当做抗碱成分。 再比如: 人体内部的缓冲对 当体内生成过多的氢氧根离子时,会和氢离子反应,根据反应平衡原理,化学反应正向移动,来抑制pH的升高,多出来碳酸氢根离子会通过肾脏排出。 4:缓冲溶液pH值的计算 5:缓冲容量 缓冲容量的大小决定于溶液中共轭酸碱对的浓度,及其比值。 当二者为1:1时缓冲容量最大。 二者的比值范围在1/10到10内 国际上几种标准缓冲溶液:
二:溶度积规则 1:溶度积常数 一定温度下溶度积常数一定 随温度升高而升高。
2:溶解度(s)与溶度积(k)之间的相互换算 溶解度:溶液中溶质的质量与溶液体积的比 3:溶度积原理: 用于判断反应方向是沉淀还是溶解 溶解为正方向,沉淀为反方向。 这里与反应平衡移动是可以类比过来的。
同样的,k值越大,说明正向反应越强烈。 Q>K 溶质析出 Q=K 饱和 Q |
【本文地址】
 醋酸是弱电解质,醋酸钠是强电解质两者含有共同的元素醋酸根。当二者共同存在于溶液中时,醋酸的溶解度降低,此时就会使溶液的pH值基本保持不变。
醋酸是弱电解质,醋酸钠是强电解质两者含有共同的元素醋酸根。当二者共同存在于溶液中时,醋酸的溶解度降低,此时就会使溶液的pH值基本保持不变。 当溶液中存在这对缓冲物质时, 如果向溶液中增加酸,分解的氢离子会和醋酸根反应生成醋酸以维持溶液的pH值。
当溶液中存在这对缓冲物质时, 如果向溶液中增加酸,分解的氢离子会和醋酸根反应生成醋酸以维持溶液的pH值。 当体内生成过多的氢离子时,会和碳酸氢根反应生成水和二氧化碳,溶解的二氧化碳转变为气相的二氧化碳,通过肺部排出。
当体内生成过多的氢离子时,会和碳酸氢根反应生成水和二氧化碳,溶解的二氧化碳转变为气相的二氧化碳,通过肺部排出。
 此处为近似计算0.1,对50的的变化忽略不计,可用原溶液浓度。 在某一温度下,pkθ是定值,代入公式即可。
此处为近似计算0.1,对50的的变化忽略不计,可用原溶液浓度。 在某一温度下,pkθ是定值,代入公式即可。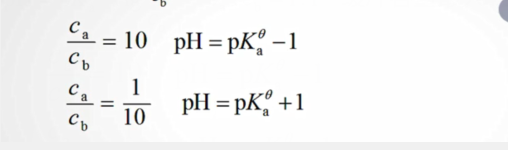 分别把10和1/10代入计算pH的公式可得pH值的范围为pkθ±1 也就是:
分别把10和1/10代入计算pH的公式可得pH值的范围为pkθ±1 也就是:  当二者比例为1:1时,计算pH值得公式就变为 pH=pKθ
当二者比例为1:1时,计算pH值得公式就变为 pH=pKθ 

 第一题: 甲基橙的变色范围是pH值为3.1-4.4。溶液的pH4.4时,甲基橙具黄色;而在pH3.1~4.4,则出现红黄的混合色橙色。 第二题代入公式计算:取pkθ最接近与pH值得数 第三题:代入公式,利用共轭酸碱的比值范围得出大致的范围
第一题: 甲基橙的变色范围是pH值为3.1-4.4。溶液的pH4.4时,甲基橙具黄色;而在pH3.1~4.4,则出现红黄的混合色橙色。 第二题代入公式计算:取pkθ最接近与pH值得数 第三题:代入公式,利用共轭酸碱的比值范围得出大致的范围 通式为:
通式为: 已知溶度积常数是一种平衡常数,我们也可以通过热力学参数来计算。 如:
已知溶度积常数是一种平衡常数,我们也可以通过热力学参数来计算。 如: 
 第一步求得是浓度。 (2):溶度积常数换算溶解度 溶解度的单位可以是克每升,也可以是摩尔每升
第一步求得是浓度。 (2):溶度积常数换算溶解度 溶解度的单位可以是克每升,也可以是摩尔每升  同类型的难溶电解质是指化学式中阴阳离子组成相似,如AB型、A2B型、AB2型等。例如BaCO3、BaSO3、BaSO4就属于同类型的难溶电解质
同类型的难溶电解质是指化学式中阴阳离子组成相似,如AB型、A2B型、AB2型等。例如BaCO3、BaSO3、BaSO4就属于同类型的难溶电解质 
 在反应平衡常数我们引入了任意状态的反应常数 Q 同样的我们在这里也引入任意反应状态的离子积常数Qi
在反应平衡常数我们引入了任意状态的反应常数 Q 同样的我们在这里也引入任意反应状态的离子积常数Qi