| 2020年基迪奥细菌/真菌基因组文章盘点 | 您所在的位置:网站首页 › 真菌细菌大小 › 2020年基迪奥细菌/真菌基因组文章盘点 |
2020年基迪奥细菌/真菌基因组文章盘点
|
实验设计 研究者从含有羽毛的土壤中分离出若干个能够降解羽毛的细菌分离株进行培养,通过降解实验鉴定到一类高效的羽毛降解菌(SCUT-3)。对SCUT-3进行全基因组测序,获得基因组信息,并进行了转录组测序,分析此类细菌降解羽毛的机制。 实验结果 通过降解实验发现在分离到的候选细菌中,SCUT-3的降解效果最佳,36h内能够完全降解羽毛与杆身(图1),羽毛中31.6%转化为了可溶性氨基酸,12.7%转化为肽段,降解产物进行鱼类饲料添加饲喂也达到了预期效果。 细菌基因组测序后基于16s rRNA构建进化树,结果表明SCUT-3属于链霉菌属(Streptomyces),对基因组进行组装,组装大小约为6.08Mb,注释获得5811个基因,对细菌的各类生理生化特性进行了补充测试。
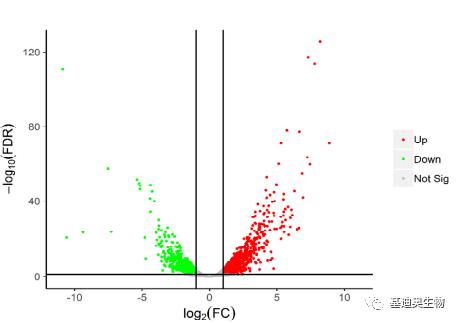
图1 SCUT-3羽毛降解效果 对细菌的羽毛降解特性进行了测试,结果表明在有其他营养来源(如LB培养基)可选条件下,SCUT-3细菌将优先使用其他营养源,关闭羽毛降解相关功能。因此,研究者设置了LB培养对照组与羽毛培养基实验组培养24h后进行转录组测序,分析羽毛降解功能的相关基因。转录组分析共检测到775个上调与623个下调的差异基因(DEG,图2),对显著差异的DEGs进行GO与KEGG富集分析,找到了羽毛降解功能相关的氧化磷酸化、氧化呼吸、物质转运等重要功能。
图2 组间差异基因火山图 之后,对细菌降解羽毛的机制涉及到的功能进行了验证与描述,羽毛降解过程包括了二硫键还原、蛋白酶水解、氨基酸转运、铁的吸收等,其中增强通风条件可以提高细菌羽毛的降解率、活性代谢,孢子形成/复苏和分裂等过程。 真菌基因组测序[2] 基因组denovo技术揭示桑实杯盘菌(C. shiraiana)的致病机制 期刊:Molecular plant-microbe interactions 单位:西南大学
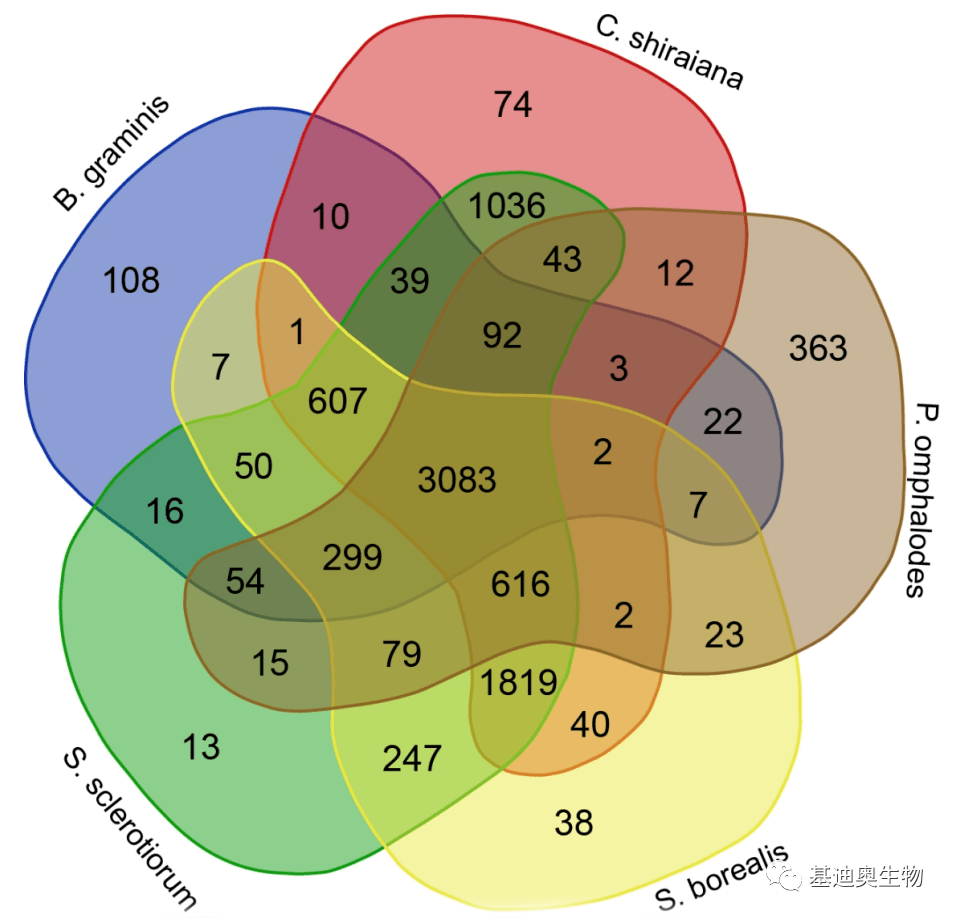
研究背景 桑实杯盘菌(Ciboria shiraiana)属子囊菌亚门真菌,是引发桑椹菌核病的主要原因,菌核病能够造成巨大的经济损失,当前对于此类真菌的了解较少,在基因组水平探索致病机制对于后续开发新的菌核病防治方案至关重要。 实验设计 从患病桑果中分离出致病菌进行纯化培养,收集真菌的菌丝提取DNA,采用三代+二代的形式进行基因组测序研究。 实验结果 杯盘菌(C. shiraiana)基因组的组装大小为39.2Mb,GC含量(41.6%)与S.sclerotiorum(41.8%)相当。通过预测,共获得14439个蛋白编码基因,213个tRNA和99个rRNA。重复序列预测结果表明大部分重复序列为转座因子(TE)。 将杯盘菌与其近缘物种进行基因家族分析,结果表明:5种真菌共有的常见基因组家族为3083个,与其他真菌相比,杯盘菌有74个特有的基因家族,共计189个基因,这些特有基因是该类真菌潜在的致病性靶标(图3)。将这些特有的基因进行富集分析,有15个基因在代谢途径中富集。
图3 基因家族Venn图分析 分解碳水化合物能力是坏死性真菌的重要特征,对碳水化合物活性酶(CAZymes)进行注释,结果表明杯盘菌(C. shiraiana)基因组包含有244个糖苷水解酶(GH)、7种多糖裂解酶(PL)、35个碳水化合物酯酶(CE)、99种糖基转移酶(GT)等。通过多物种预测比较发现,坏死性真菌的CAZymes的数量普遍高于营养性真菌。 为了深入研究杯盘菌的致病机制,收集接种到植株叶片上0、1、3、6、12、24h后的杯盘菌,进行qPCR验证,12种纤维素酶基因的表达量在接种12h后均显著上升。GH28家族在病原体果胶降解中起重要作用, 在叶片接种感染过程中有12个果胶酶基因在6h达到上调顶点,Cs05107随感染时间表达量逐渐上升,可能是该真菌致病的关键基因。 基因组+转录组测序+代谢组多组学关联[3] 基因组+转录组+脂质组揭示粘红酵母(Rhodotorula glutinis)基因组特征 期刊:BMC Genomics 单位:仲恺农业工程学院
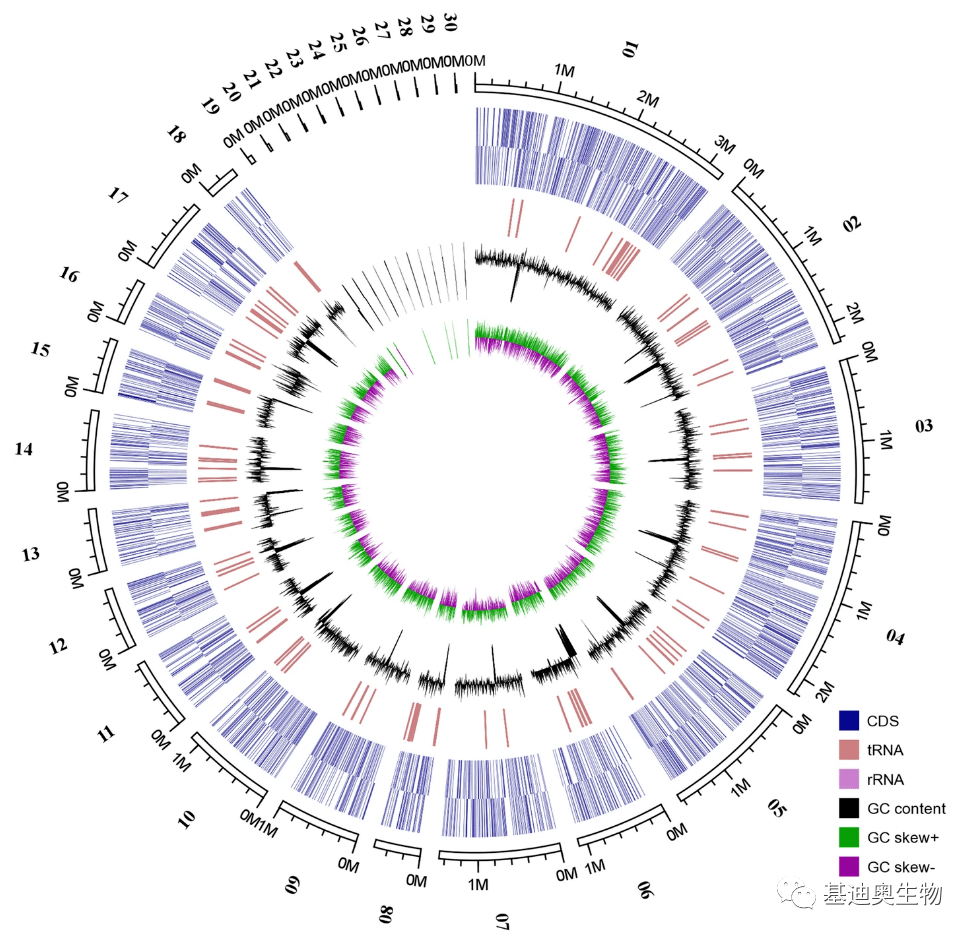
研究背景 粘红酵母(Rhodotorula glutinis)是一种重要的产油脂微生物,它能够合成类胡萝卜素等化合物,这些化合物在工业上具有广泛的用途,当前对于粘红酵母的基因组还缺乏深入的研究。 实验设计 从环境样本中分离获得粘红酵母菌株(R.glutinis ZHK),经预培养、扩大培养之后离心收集,液氮速冻,提取总DNA、RNA和代谢产物。利用基因组denovo+三代全长+RNA-seq+代谢组多组学揭示粘红酵母基因组特征,及其生物技术潜力。 实验结果 采用Pacbio平台三代全长基因组测序,粘红酵母菌株(R.glutinis ZHK)组装大小为21.8Mb,GC含量为67.8%,预测到6774个基因,156个tRNA(图4)。比较基因组学结果表明,粘红酵母中,大部分基因同源,特别是类胡萝卜素生物合成基因都经过了较强的纯化选择。
图4 粘红酵母菌株(R.glutinis ZHK)基因组圈图 利用GeneMark-ES整合RNA-seq和基因组信息,对基因组功能注释,预测到几个涉及脂类和类胡萝卜素代谢的关键基因以及某些工业酶的生物合成;靶向代谢组学分析粘红酵母脂质体,共鉴定了982种脂质,主要包括三酰基甘油、二酰基甘油三甲基同聚物和磷脂酰乙醇胺。菌株基因组序列结合分泌脂质类型的研究为后续菌种基因改造用于工业生产提供了理论参考。 小结 单菌研究对于认识新的微生物的基因/功能组成有着重要的意义,单菌的研究不局限于基因组的测序,可以结合转录组等组学方法多方位研究微生物的重要功能的发生机制。 文末福利 即日起,在OM商城下单满额,即送超多福利!(不与线下优惠共享) 福利一:好评多多,干货满满的生信培训班,转录组、微生物、10×生信培训班任你挑选! 福利二:100多种绘图工具,用户数突破6万的OmicShare会员,提升发文速度的利器! 福利三:独家生信技术资料分享,专业人员撰写的原创书籍,快速全面提高组学研究的独门秘笈! 参考文献 [1] Li, ZW., Liang, S., Ke, Y. et al. The feather degradation mechanisms of a new Streptomyces sp. isolate SCUT-3. Commun Biol 3, 191 (2020). [2] Zhu P, Kou M, Liu C, et al. Genome Sequencing of Ciboria shiraiana Provides Insights into the Pathogenic Mechanisms of Hypertrophy Sorosis Scleroteniosis. Mol Plant Microbe Interact. 2021;34(1):62-74. doi:10.1094/MPMI-07-20-0201-R [3] Li, CJ., Zhao, D., Cheng, P. et al. Genomics and lipidomics analysis of the biotechnologically important oleaginous red yeast Rhodotorula glutinis ZHK provides new insights into its lipid and carotenoid metabolism. BMC Genomics 21, 834 (2020).返回搜狐,查看更多 |
【本文地址】