| 甲酸 | 您所在的位置:网站首页 › 甲酸的化学性质 › 甲酸 |
甲酸
跳转到: 导航,
搜索
A+医学百科 >> 甲酸
甲酸
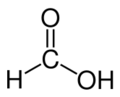
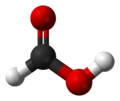 IUPAC名
Formic acid, Methanoic acid
别名
HCOOH
识别
CAS号
64-18-6
SMILES
O=CO
RTECS
LQ4900000
性质
化学式
CH2O2
HCOOH
摩尔质量
46.0254 g·mol⁻¹
外观
无色发烟液体
密度
1.22 g/mL (液)
熔点
8.4 °C (47.1 °F)
沸点
100.8 °C (213.3 °F)
溶解性(水)
混溶
pKa
3.744
黏度
1.57 cP, 26 °C
结构
分子构型
平面
偶极矩
1.41 D (气态)
危险性
警示术语
R:R10-R35
安全术语
S:S1/2-S23-S26-S45
MSDS
ScienceLab.com
主要危害
腐蚀性、刺激性
NFPA 704
IUPAC名
Formic acid, Methanoic acid
别名
HCOOH
识别
CAS号
64-18-6
SMILES
O=CO
RTECS
LQ4900000
性质
化学式
CH2O2
HCOOH
摩尔质量
46.0254 g·mol⁻¹
外观
无色发烟液体
密度
1.22 g/mL (液)
熔点
8.4 °C (47.1 °F)
沸点
100.8 °C (213.3 °F)
溶解性(水)
混溶
pKa
3.744
黏度
1.57 cP, 26 °C
结构
分子构型
平面
偶极矩
1.41 D (气态)
危险性
警示术语
R:R10-R35
安全术语
S:S1/2-S23-S26-S45
MSDS
ScienceLab.com
主要危害
腐蚀性、刺激性
NFPA 704
 2
3
0
闪点
69 °C (156 °F)
相关物质
相关羧酸
乙酸、丙酸
相关化学品
甲醛、甲醇
若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。
2
3
0
闪点
69 °C (156 °F)
相关物质
相关羧酸
乙酸、丙酸
相关化学品
甲醛、甲醇
若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。
甲酸(英文:Formic acid)又称作蚁酸,化学式为HCOOH。蚂蚁分泌物和蜜蜂的分泌液中含有蚁酸,当初人们蒸馏蚂蚁时制得蚁酸,故有此名。甲酸无色而有刺激气味,且有腐蚀性,人类皮肤接触后会起泡红肿。熔点8.4℃,沸点 100.8℃。由于甲酸的结构特殊,它的一个氢原子和羧基直接相连。也可看做是一个羟基甲醛。因此甲酸同时具有酸和醛的性质。在化学工业中,甲酸被用于橡胶、医药、染料、皮革种类工业。 目录 1 性质 2 制备 3 安全 4 化学性质 5 参见 6 参考资料 7 参考来源 性质甲酸与水和大多数的极性有机溶剂混溶,在烃中也有一定的溶解性。在烃中及气态下, 甲酸以通过以氢键结合的二聚体形态出现。在气态下,氢键导致甲酸气体与理想气体状态方程之间存在较大的偏差。液态和固态的甲酸由连续不断的通过氢键结合的甲酸分子组成。 甲酸具有与大多数其他羧酸相同的性质,尽管在通常情况下甲酸不会生成酰氯或者酸酐。直到不久以前,所有试图将甲酸转化成这些衍生物的尝试都以产物一氧化碳告终。甲酸酐可由甲酰氟和甲酸钠在零下78摄氏度反应得到。甲酰氯可由将氯化氢气体通过零下60度1-甲酰基咪唑的一氯甲烷溶液得到。甲酸脱水分解为一氧化碳和水。甲酸具有和醛类似的还原性。它能起银镜反应,把银氨络离子中的银离子还原成金属银,而自己被氧化成二氧化碳和水: HCOOH+2AgOH→2Ag+2H2O+CO2 甲酸是唯一能和烯烃进行加成反应的羧酸。甲酸在酸的作用下(如硫酸,氢氟酸),和烯烃迅速反应生成甲酸酯。但是类似于Koch反应的副反应也会发生,产物是更高级的羧酸。 大多数的甲酸盐溶于水。 制备制备其他化学药品(尤其是乙酸)的过程中,大量的甲酸作为副产物被生产出来。 然而这样的制备远远的不能满足目前对甲酸的需要,所以有些甲酸被直接生产。 在强碱作用下,甲醇和一氧化碳反应生成甲酸甲酯: CH3OH + CO → HCOOCH3在工业生产中, 此反应在液态和加压的状态下进行。 典型的反应条件为80摄氏度和40个大气压。广泛使用的碱为甲醇钠。水解甲酸甲酯得到甲酸。 HCOOCH3 + H2O → HCOOH + CH3OH水解甲酸甲酯需要大量的水来保证反应顺利进行。 有些生产商使用一种间接的水解途径, 即先将甲酸甲酯和氨反应产生甲酰胺,然后用硫酸水解甲酰胺得到甲酸: HCOOCH3 + NH3 → HCONH2 + CH3OH 2HCONH2 + 2H2O + H2SO4 → 2HCOOH + (NH4)2SO4这种技术有其自身缺点,尤其是在对副产物硫酸铵的处理上。有些生产商最近发展了一类节能的方法,即将甲酸从直接水解的大量水溶液中提取出来。在其中一种方法(由巴斯夫所使用)中,甲酸在有机碱的作用下由湿法萃取得到。 在实验室制备中,甲酸可由在无水丙三醇中加热草酸,然后蒸汽蒸馏得到。另外一种制备方法(必须要在通风橱中进行)是在盐酸作用下的异乙腈的水解。 C2H5NC + 2H2O → C2H5NH2 + HCOOH异腈的制备由乙胺和氯仿反应获得。(异腈过于令人不快的气味使此反应必须在通风橱中进行。) 安全
甲酸具有羧酸的通性。但甲酸同时具有一个醛基,这使它可以被进一步氧化: 2HCOOH + O2 → 2CO2 + 2H2O甲酸在浓硫酸或氧化铝催化下加热脱水生成一氧化碳,这是实验室制取纯净一氧化碳的方法。 HCOOH → CO + H2O (在浓硫酸催化下加热)甲酸也能在氧化锌或高锰酸钾催化下,进行脱氢反应: HCOOH → CO2 + H2 参见 甲酸盐 参考资料 NIST webbook ChemSub Online: 甲酸 参考来源 维基百科-甲酸 出自A+医学百科 “甲酸”条目 http://www.a-hospital.com/w/%E7%94%B2%E9%85%B8 转载请保留此链接 关于“甲酸”的留言:目前暂无留言 添加留言 更多医学百科条目 5个分类: 无附加数据页的化学条目 | 羧酸 | 有机溶剂 | 清洁产品成分 | 一碳有机物 |
【本文地址】