| 关于光电化学中RHE和Ag/AgCl之间的转换 | 您所在的位置:网站首页 › 氯化银电位和标准电位区别 › 关于光电化学中RHE和Ag/AgCl之间的转换 |
关于光电化学中RHE和Ag/AgCl之间的转换
|
首先你要明确一些基本的概念: ERHE(V):可逆氢电极(RHE)是电化学会用于表示电极电位是标准的“零电位”。(一般论文里面转换值) EAg/AgCl(V):一般的实验值,因为实验和绝对的零点位相比不现实,而是选择和参考电极之间进行对比之后的相对电压。(一般就是Ag电极,氧化汞电极) 这两者主要是起始的电位不同,范围的宽度是一样宽的。这个时候你就可以关注两者之间怎么进行转换了。 下面有一个公式:根据Nernst方程,将Ag/AgCl转换为可逆氢电极(RHE)尺度: (当然这里是以饱和的AgCl参比电极为例 。如果参比电极发生变化,那就是Eo AgCl这个参数改变,也就是你的参比电极选定后你的Eo AgCl这个参数就确定了,这个值一般百度都可以搜到,当然这里的影响因素还有pH值。) 这个公式篇来源论文(P2)doi.org/10.1016/j.jechem.2020.07.013doi.org/10.1016/j.jechem.2020.07.013  其中,电解液为1.0M氢氧化钠(pH=13.6)电解液。EoAg/AgCl在25℃下为0.1976V,EAg/AgCl为对Ag/AgCl参考电极的实验测量电位,ERHE为转换电位。rhe。 其中,电解液为1.0M氢氧化钠(pH=13.6)电解液。EoAg/AgCl在25℃下为0.1976V,EAg/AgCl为对Ag/AgCl参考电极的实验测量电位,ERHE为转换电位。rhe。所以你需要注意的点就(1)参比电极(2)pH值。 这里举个例子把吧!(http://doi.org/10.1021/jacs.1c00802)  这是李灿教授的一篇关于光电催化的一篇论文的LSV  这张图b里面电压窗口大概在0.2~1.2V之间,这个时候你要看清楚到底是V RHE,还是V vs AgCl。(当然这篇论文是V RHE)。这个时候如果是你要用的测试的用的是和前面的那个一样的参比电极(AgCL,盐桥为饱和KCl)和相同的电解质溶液(pH都是13.6)。所以上面的ERHE=EAgCl+1,可以直接代用(如果是你们的自己的体系和参比电极可以自己改下参数就行)。 然后我们要换成我们自己的(AgCl参比)测试区间只需要把前面的0.2`~1.2的基础上减去1就行了,大致我们的区间就在-0.8~0.2之间。当然这只是理论上的,你自己取区间的话还可以灵活一点。起点和终点都可以夺取周围的几个点,因为环境不可能完全一样。 当然这也是我最近看到后自己总结的一些看法,如果有不同的看法和想完善的话都可以留言或私信谈论哦!!希望对正在做科研的你有些帮助。  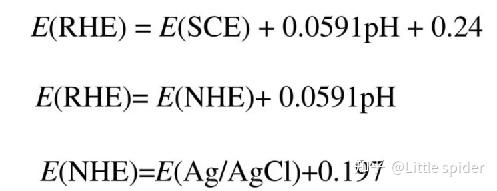
|
【本文地址】