| 非金属的气态氢化物的热稳定性和熔、沸点分别与什么有关? | 您所在的位置:网站首页 › 氢化物沸点变化规律 › 非金属的气态氢化物的热稳定性和熔、沸点分别与什么有关? |
非金属的气态氢化物的热稳定性和熔、沸点分别与什么有关?
|
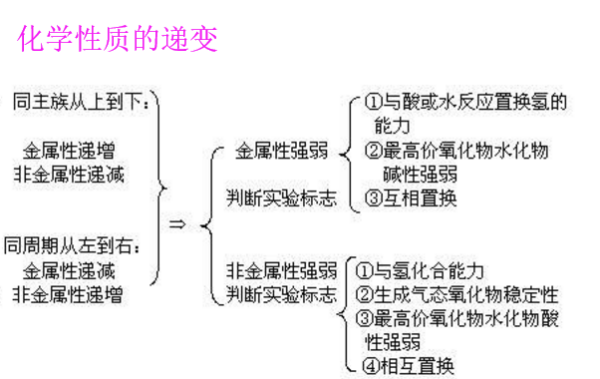
1、热稳定性与原子半径,原子间化学键强弱相关。原子半径越大,原子之间的化学键越弱越容易分解,即热稳定性越小。同周期元素的气态氢化物(自左向右)的稳定性逐渐增强;同主族元素的气态氢化物(自上向下)氢化物的稳定性逐渐减弱。比如热稳定性:HCl > HBr > HI2、熔沸点与分子间作用力相关。分子间力越大,熔沸点越高。一般情况下,分子间以色散力为主,而色散力与分子体积有关,所以半径越大,分子间作用力越大,熔沸点越高。 扩展资料1、常见气态氢化物的典型结构与分子极性。①HCl、HF等直线型的极性分子;②H2O、H2S等平面“V”构型的极性分子;③NH3、PH3等三角锥型结构的极性分子;④CH4、SiH4等正四面体型的非极性分子。2、同周期元素气态氢化物中,H-R(R为非金属元素)的键长逐渐减小,同主族元素气态氢化物中,H-R键长逐渐增大。气态氢化物的化学性质变化规律及特性(非金属性越强稳定性越好)。参考资料来源:搜狗百科-气态氢化物参考资料来源:搜狗百科-热稳定性参考资料来源:搜狗百科-熔点参考资料来源:搜狗百科-沸点 |
【本文地址】
公司简介
联系我们