| NaF 是离子的还是共价的:为什么,如何,路易斯结构,详细解释 | 您所在的位置:网站首页 › 氟化钠的性质是什么 › NaF 是离子的还是共价的:为什么,如何,路易斯结构,详细解释 |
NaF 是离子的还是共价的:为什么,如何,路易斯结构,详细解释
|
Naf,或氟化钠,是一种常用的化合物 牙膏和 水氟化。 当确定 Naf 是离子型还是共价型时,我们需要考虑之间键的性质 钠 和氟原子。在 这个案例, Naf 是离子化合物,这意味着 钠 原子 捐赠一个电子给 氟原子,导致形成 带正电的钠离子 (Na +)和 带负电的氟离子 (F-)。 这种电子转移会产生 强大的静电吸引力 离子之间,给出 Naf 它的 离子性质. 关键精华这是 简洁的表格 总结 关键信息 关于纳夫: 复合肥产线Naf(氟化钠)债券类型离子的化学式氟化钠常见用途牙膏、水氟化离子性质钠向氟化物提供电子形成的离子Na+(钠离子)、F-(氟离子)共价离子化合物的定义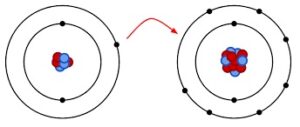 维基共享资源 维基共享资源共价和离子化合物 ,那恭喜你, 两种类型 of 化合物 其不同之处在于 它们的粘合特性 和属性。 共价化合物的解释共价化合物形成时 两个或更多 非金属原子 共享电子以实现稳定的电子构型。 在 这个类型 的粘合, 原子 涉及有 相似的电负性,导致 平等分享 电子。 这种电子共享创造了 牢固的纽带 之间 原子,被称为 共价键. 在共价化合物中,例如氟化钠 (NaF),之间的键合 钠 (Na) 和氟 (F) 原子通过共享电子而发生。 钠有 一价电子,而氟有七个。 通过共享一个电子,钠实现了 稳定的配置,氟达到 稳定的八位位组。 这种电子共享形式 共价键,导致形成 NaF化合物. 共价化合物通常具有较低的熔点和 沸点s 与离子化合物相比。 他们也往往是 不良导体 的电力在 他们的纯粹形式作为 共享电子 位于之间 键合的原子. 离子化合物的解释当存在时会形成离子化合物 转移 金属和金属之间的电子 非金属原子。 这种电子转移会产生 带电粒子 称为离子,它们通过 静电力. 金属原子 失去电子变成 带正电荷的阳离子,而 非金属原子 获得电子成为 带负电的阴离子. 对于 NaF,钠将其价电子捐赠给氟,从而形成 钠阳离子 (Na +)和 氟阴离子 (F-)。 这些相反 带电离子 相互吸引,形成离子键。 强 静电力 离子之间将化合物结合在一起。 离子化合物,如 NaF,通常具有高熔点和 沸点s 由于 强大的力量 离子之间的吸引力。 他们也是 良导体 当溶解在水中或熔化时产生电力,因为离子可以自由移动和携带 电荷. 总之,共价化合物涉及之间共享电子 非金属原子,而离子化合物涉及金属和金属之间的电子转移 非金属原子。 NaF的分子结构说明 共价性质 钠和氟之间的键,而 此 离子形成 亮点 离子特性 的化合物。 理解 区别s 之间 离子和共价化合物 帮助我们欣赏 独特的化学性质 展出的 每种类型 粘合。 了解氟化钠 (NaF) 氟化钠基本信息氟化钠 (NaF) 是 一种化合物 由钠 (Na) 和 氟 (F) 离子。 它常用于 各种应用,包括牙膏, 水氟化, 并作为 试剂 in 化学反应。 NaF 众所周知 其独特的粘合特性,这使得它成为一个有趣的研究化合物。 当我们谈论 NaF 的键合类型时,重要的是要了解 区别 之间 离子键和共价键。 当电子从一个原子完全转移到另一个原子时,就会发生离子键,从而形成 带电离子。 另一方面,共价键涉及原子之间共享电子。 NaF 离子如何?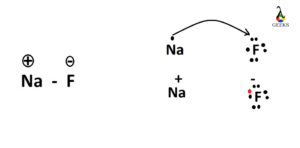 就 NaF 而言,钠和氟化物之间的键合本质上是离子键。 这意味着电子完全从钠转移到氟化物。 钠有 一价电子,而氟化物有 七个价电子。 钠很容易将其价电子提供给氟化物,从而形成 Na+ 和 F- 离子。 它的成形 of 这些离子 由...驱动 欲望 以获得稳定的电子构型。 钠达到 稳定的配置 通过失去其价电子并成为 带正电的离子 (钠+)。 另一方面,氟化物会增加 电子 并成为 带负电的离子 (F-)。 相反的电荷 离子相互吸引,在钠和氟化物之间形成离子键。 为什么 NaF 不是共价化合物?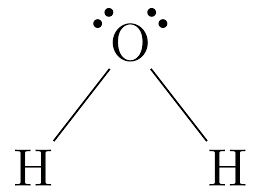 刘易斯点结构维基共享资源 刘易斯点结构维基共享资源NaF 不是共价化合物,因为它不涉及钠和氟化物之间共享电子。 在共价化合物中,例如 分子物质,原子共享电子以实现稳定的电子构型。 然而,在 NaF 的情况下,电子会完全转移,从而形成离子。 离子性质 通过检查可以进一步了解 NaF 它的属性。 离子化合物,如NaF,具有高熔点和 沸点s 由于强 静电力 对立之间 带电离子。 它们还易于溶于水,并在溶解或熔化时导电。 相反,共价化合物的熔点较低, 沸点s 并且通常不溶于水。 它们不导电,因为没有 带电粒子 当下。 总之,由于电子完全从钠转移到氟化物,NaF是一种离子化合物。 这导致 Na+ 和 F- 离子的形成,它们通过强力结合在一起 静电力。 理解 债券性质 和 复合型 NaF 提供了以下见解 迷人的世界 的化学键合。 深入研究 NaF 的结构NaF路易斯结构当涉及到理解 结构 NaF(氟化钠)的含量,有必要深入研究 其路易斯结构. 刘易斯结构 提供 视觉表现 原子如何结合在一起 一个分子 或复合。 就 NaF 而言,它可以帮助我们了解 化学键合 钠 (Na) 和 氟化物 (F) 原子. NaF 是一种离子化合物,这意味着它由通过离子键结合在一起的离子组成。 离子键是通过电子从一个原子转移到另一个原子而形成的。 在 NaF 中,钠向氟化物提供一个电子,从而形成 Na+ 和 F- 离子。 这种电子转移 创建 强大的静电吸引力 对立之间 带电离子,导致形成 NaF晶格. NaF是碱性盐吗?现在我们来探讨一下NaF是否是 碱性盐。 为了确定这一点,我们需要检查 属性 NaF 并了解 它的特点 作为离子化合物。 离子化合物,如 NaF,通常具有高熔点和 沸点s 由于强 静电力 离子之间。 氟化钠有 熔点 993°C 和 a 沸点 1700°C,表明 其高稳定性. 就溶解度而言,NaF极易溶于水。 什么时候 氟化钠晶体 添加到水中, 离子键s Na+ 和 F- 离子之间的断裂,离子解离,导致形成 钠阳离子 (Na +)和 氟阴离子 (F-) 在 解决方案. 氟化钠也展出 一些有趣的化学性质 由于 它的 离子性质。 例如,当它溶解在水或水中时可以导电。 此 熔融状态。 这是因为 运动 离子允许 流量 of 电流. 另一方面,共价化合物涉及原子之间共享电子。 在NaF中,有 无电子共享 介于钠和氟化物之间。 相反,电子发生完全转移,使其成为离子化合物而不是共价化合物。 总而言之,NaF 分子结构 哪里 钠和 氟离子 通过离子键结合在一起。 它是一种离子化合物 独特的化学性质 与离子键有关。 债券性质 NaF 涉及 离子形成 并且缺乏共价性。 通过了解 NaF 的键合类型、性质和结构,我们深入了解 迷人的世界 of 化合物 和 多种多样的方式 其中原子可以相互作用形成 不同的物质. 不同条件下的NaF当氟化钠与水反应时会发生什么?当氟化钠(NaF)与水反应时, 有趣的化学反应 发生。 NaF 是一种离子化合物,这意味着它由以下组成 带正电荷的钠离子 (Na +)和 负面的 氟离子 (F-)。 在水中,极性 水 分子允许它们包围和分离 Na+ 和 F- 离子, 导致 解散 氟化钠。 解散 水中出现 NaF 的原因是 吸引力 之间 正电荷和负电荷. 水分子 环绕 Na+离子, 它们的氧原子 面对 钠 离子,同时 氢原子 脸朝外。 相似地, 水 分子包围 F-离子, 它们的氢原子 面对 氟离子及 氧原子s 面向外。 这个流程 of 离子分离 水合作用至关重要 解散 水中的NaF等离子化合物。 水分子 有效打破 离子键s 之间 Na+ 和 F- 离子,让他们可以自由活动 解决方案。 这导致形成 氟化钠溶液,其中 Na+ 和 F- 离子 分散在各处 水. 氟化钠易溶于水吗?是的,氟化钠 (NaF) 极易溶于水。 如前所述,水的极性性质使其能够有效溶解 NaF 等离子化合物。 强大的吸引力 之间 水 分子和 Na+ 和 F- 离子 导致 完全溶解 水中的NaF。 溶解度 水中 NaF 的含量可通过以下方式定量 其溶度积 常数(Ksp)。 Ksp值 NaF 相对较高,表明 其高溶解度 在水里。 这意味着 大量的 NaF能溶于水,形成 均匀溶液. 重要的是要注意到这一点 溶解度 氟化钠在 其他溶剂 可能会有所不同。 虽然 NaF 极易溶于水,但它可能具有 有限溶解度 甚至不溶于 非极性溶剂。 这是因为 区别 极性介于水和 非极性溶剂,这影响了能力 溶剂分子 相互作用并溶解 NaF离子. 总之,NaF是一种离子化合物,由于其易溶于水 吸引力 之间 Na+ 和 F- 离子 和极地性质 水分子. 这个溶解度 在水中使 NaF 成为一种有用的化合物 各种应用,例如 牙科产品 和 水氟化. 比较与对比NaF 是离子型还是共价型还是两者都有?当谈到 NaF(氟化钠)的键合类型时,了解这一点很重要 基本概念 的化学键合。 化学键 可以分为 两种主要类型:离子键和共价键。 离子键涉及电子从一个原子转移到另一个原子,从而形成离子。 另一方面,共价键涉及原子之间共享电子。 对于 NaF,键合本质上主要是离子键合。 钠(Na)是金属,而氟(F)是非金属。 金属倾向于失去电子以获得稳定的电子构型,而非金属倾向于获得电子。 在 NaF 中,钠向氟提供一个电子,从而形成 钠阳离子 (Na +)和 氟阴离子 (F-)。 这种电子转移导致离子化合物的形成。 NaF是离子化合物还是共价化合物?NaF 被认为是离子化合物,因为 其离子键性质。 离子化合物通常由以下组成 金属阳离子 和 非金属阴离子。 在 NaF 中,钠充当 阳离子,而氟化物则充当 阴离子. 强静电吸引力 对立之间 带电离子 将化合物结合在一起,形成 晶格结构. 离子化合物,例如 NaF,具有 不同的属性。 他们通常坚守在 室内温度,具有高熔点和 沸点s,并且 良导体 溶于水或熔化时产生电力。 这些属性 源自 强离子键 以及离子在其中自由移动的能力 一个办法 or 熔融状态. NaF是离子键还是共价键?NaF中钠和氟之间的键可以描述为离子键。 离子键是通过电子从一个原子完全转移到另一个原子而形成的。 对于 NaF,钠将其价电子提供给氟,从而形成 Na+ 和 F- 离子。 静电引力 之间 这些离子 创建 离子键. 另一方面,共价键涉及原子之间共享电子。 这种电子共享使原子能够实现稳定的电子构型。 然而,就 NaF 而言, 电子钠和氟之间的负性差异很大,导致电子完全转移而不是共享。 总之,NaF表现出离子键合,使其成为离子化合物。 转移 电子从钠到 氟结果 形成 Na+ 和 F- 离子,它们通过强作用结合在一起 静电力。 了解化学键的性质,无论是离子键还是共价键,都有助于我们理解 属性 和行为 不同的化合物. 常见问题有关 NaF 及其离子或共价性质的常见问题NaF,也称为氟化钠,是一种化合物 主题 of 许多问题 关于 它的键合类型。在 本节,我们将解决一些 最常见的问题 关于NaF及其是否表现 离子或 共价特性. 问:NaF的键合类型是什么?A:NaF表现出离子键。 当电子从一个原子完全转移到另一个原子时,就会形成离子键。 对于 NaF,钠 (Na) 向氟 (F) 提供电子,从而形成 Na+ 和 F- 离子。 问:离子键与共价键有何不同?答:离子键涉及电子的完全转移,从而形成 带电离子。 另一方面,共价键涉及原子之间共享电子。 在NaF中,钠和氟之间的键由于电子的完全转移而呈离子键。 问:NaF 作为离子化合物有什么特性?答:NaF作为一种离子化合物,有以下几种性质: 不同的属性。 它有 高熔点 和 沸点 由于强 静电力 之间的 带正电荷的钠离子 和 负面的 氟离子。 NaF 也可溶于水,并在溶解或熔化时导电,因为离子可以自由移动和携带 电荷. 问:NaF 的分子结构如何影响其离子性质?答:NaF的分子结构为 重复格子 of 钠和 氟离子. 钠离子 (Na+) 被包围 六个氯离子 (F-) 在 三维排列. 这样的安排 相反的 带电离子 有助于 整体稳定性 和 离子性质 氟化钠。 问:NaF 中离子键的化学性质是什么?A:NaF 中的离子键表现 几种化学性质。 它们通常很强且稳定,使 NaF 在以下温度下成为固体化合物: 室内温度。 离子化合物如 NaF 往往具有高熔点和 沸点s, 常溶于 极性溶剂,并且在溶解或熔化时可以导电 在场 of 自由离子. 问:NaF 中的共价键与离子键有何不同?答:共价键涉及原子之间共享电子,从而形成分子。 在 NaF 中,钠和氟之间的键是离子键,因为电子完全转移。 另一方面,共价化合物共享电子,导致形成分子而不是离子。 问:NaF 是否被视为共价化合物?答:不,NaF 不被视为共价化合物。 由于钠和氟之间电子完全转移,它是一种离子化合物。 共价化合物涉及共享电子,而 NaF 中不会发生这种情况。 问:NaF 中的键的性质是什么?答:NaF 中的键本质上是离子键。 它涉及电子从钠到氟的完全转移,从而形成相反的 带电离子. 问:NaF 是否表现出任何共价特性?答:不,NaF 不会表现出来 共价特性。 由于钠和氟之间电子完全转移,它主要是一种离子化合物。 问:NaF 中是否存在共价键?答: 没有,有 无共价性 in 氟化钠。 共价性 是指原子之间共享电子,这在NaF中不会发生。 NaF中的键是纯离子键,具有完全的电子转移。 总之,NaF是一种离子化合物, 纽带 通过电子从钠到氟的完全转移而形成。 它展示了它的属性 典型的离子化合物,例如高熔点和 沸点s、在水中的溶解度以及溶解或熔融时的导电能力。 结论总之,化合物的性质,无论是离子型还是共价型,取决于 方式 之间发生的结合 其组成原子。 当存在时会形成离子化合物 转移 电子从一个原子转移到另一个原子,从而形成 正离子和负离子。 另一方面,当原子共享电子以实现稳定的电子构型时,就会形成共价化合物。 确定化合物是离子型还是共价型对于理解至关重要 它的属性 和行为。 离子化合物往往具有高熔点和 沸点s,溶于水时导电,并形成 晶体结构。 另一方面,共价化合物通常具有较低的熔点和 沸点s,不导电 他们的纯粹形式,并且可以以气体、液体或固体形式存在。 总体而言, 分类 离子或共价化合物的提供 宝贵的见解 成 他们的化学行为 并帮助我们理解 巨大的多样性 中的物质 世界 在我们周围。 常见问题解答1. 溴化锂是离子型还是分子型?溴化锂,或 溴化锂,是离子化合物。 这是因为 电子 从转移 锂原子 至 溴原子,形成离子。 2. NaF 是离子型还是共价型还是两者兼而有之?NaF,也称为氟化钠,是一种离子化合物。 这是因为钠(一种金属)将电子转移到氟化物(一种非金属),从而产生离子。 3. Na2CO3 是离子型还是共价型还是两者兼而有之?Na2CO3,或 碳酸钠,是离子化合物。 这是因为 电子 从转移 钠 原子s到 碳酸根离子. 4. SO3 是离子型还是共价型?SO3,或三氧化硫,是一种共价化合物。 这是因为硫和氧, 两者都非-金属,共享电子形成化合物。 5. CH4 是离子型还是共价型?CH4,或甲烷,是一种共价化合物。 这是由于电子之间共享 碳和氢原子. 6. NaF的分子结构是什么?NaF 或氟化钠的分子结构由以下组成 钠离子 (Na +)和 氟离子 (F-)。 钠原子 将电子转移到 氟原子,形成离子键。 7. 离子键的化学性质是什么?离子键是通过电子从金属转移到非金属而形成的。 它们导致离子的形成,通常是 牢固的纽带 具有高熔点和 沸点s。 当它们溶解在水中时也会导电。 8. 共价键的化学性质是什么?共价键是由之间共享电子形成的 两个非-金属。 这些债券 导致分子的形成。 共价化合物的熔点较低, 沸点s 与离子化合物相比,不导电。 9. MgO 是离子型还是共价型?氧化镁,或 氧化镁,是离子化合物。 这是由于电子从 镁原子 至 氧原子,形成离子。 10.NaF有什么性质?NaF,即氟化钠,是一种离子化合物,具有高熔点和高熔点等特性。 沸点s,以及溶解在水中时的导电能力。 它也溶于水,通常呈白色。 |
【本文地址】