| 盐类水解规律及离子方程式的书写 | 您所在的位置:网站首页 › 弱电解质化学方程式大全 › 盐类水解规律及离子方程式的书写 |
盐类水解规律及离子方程式的书写
|
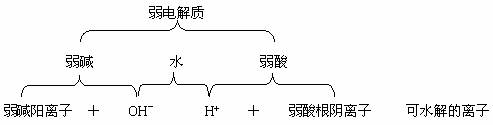
一、盐类水解的四大规律 1. 什么离子水解? 根据盐类水解的定义,知盐类水解的关键是生成了弱电解质。由下图示可知。
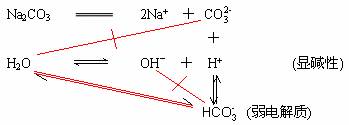
因此,盐中的弱离子(弱碱阳离子和弱酸根阴离子)一定要发生水解。 2. 什么盐水解? 强酸和弱碱所生成的盐叫强酸弱碱盐,强碱与弱酸所生成的盐叫强碱弱酸盐,弱酸与弱碱所生成的盐叫弱酸弱碱盐,强酸和强碱所生成的盐叫强酸强碱盐。 结论:含有弱离子的盐(强酸弱碱盐、强碱弱酸盐、弱酸弱碱盐等三类盐)要水解,而不含有弱离子的盐(强酸强碱盐)不水解。 3.盐类水解后水溶液的酸碱性 (1) 强碱弱酸盐的水解 1) 强碱弱酸盐要水解,水解后水溶液显碱性; 2) 这类盐包括:K2CO3、Na2S、K2S、Na3PO4、NaH2PO4、NaHCO3、KHCO3、KAc、…… (2) 强酸弱碱盐的水解 1) 强酸弱碱盐要水解,水解后水溶液显酸性; 2) 这类盐包括:Cu(NO3)2、CuSO4、CuCl2、(NH4)2SO4、NH4Cl、NH4NO3、AlCl3、FeCl3…… (3) 弱酸弱碱盐要强烈水解,水解情况复杂。若生成的弱酸比弱碱强,则水溶液显酸性;若生成的弱碱比弱酸强,则水溶液显碱性,如(NH4)2CO3。若生成的弱酸与弱碱的强度相当,则水溶液显中性,如NH4Ac水解。 (4) 强酸强碱盐不水解,水溶液显中性。(即强酸与强碱发生中和反应彻底。) 故有: 盐 + 水 这类盐包括:KNO3、NaNO3、KCl、Na2SO4、NaCl、…… 4.水解离子方程式的书写 (1) 强碱弱酸盐 1) 弱酸根阴离子参与水解,生成弱酸或酸式弱酸根; 2) 多元弱酸根阴离子分步水解,(阴离子带几个电荷就要水解几步)水解离子方程式步步照写,水的系数始终是1。不过,第一步水解最易,第二步较难,第三步水解更难。 3) 水解离子方程式用“ 4) 通式:Am-+H2O A-+H2O (2) 强酸弱碱盐 1) 弱碱阳离子参与水解,生成弱碱; 2) 多元弱碱阳离子分步水解,水解离子方程式一步完成,水的系数为阳离子的电荷数; 3) 水解离子方程式用“ 4) 通式:Mn++nH2O (3) 弱酸弱碱盐 弱酸根阴离子和弱碱阳离子都参与水解,反应后生成弱酸和弱碱。 通式:Mn++Am-+nm(OH)n+HnAH2O=mM 总结为: 弱水解,弱水解; 越弱越水解,两弱强水解。 酸碱性看“强”字,水解的离子看“弱”字。 门当户对:弱碱阳离子水解生成氢离子,弱酸根阴离子水解生成氢氧根离子。 二、水解离子方程式的书写方法 1.图示法 (1) Na2CO3
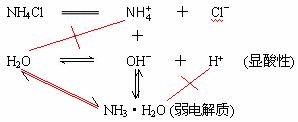
离子方程式为: 相应的化学方程式为:Na2CO3+H2O (2) NH4Cl
2.一般离子方程式的书写法 按照书写一般离子方程式的四个步骤进行。 如:NH4Cl 按照盐类水解是中和反应的逆反应,现写出化学方程式如下: NH4Cl+ H2O
这里要注意多元弱酸生成的盐,水解生成碱和酸式盐。 如Na2CO3: Na2CO3+H2O 2Na+ +
3.缺啥补啥法 按照弱离子参与水解的原则,首先找出弱离子,弱离子与水反应生成对应的同电性的离子(氢离子或氢氧根离子),然后等式两边缺啥补啥,最后配平。 如CuSO4:参与水解的是Cu2+,生成对应的阳离子H+。 Cu2++H2O(H+・OH-) 把水看成是H+・OH-,显然,阳离子将与结合生成Cu(OH)2, Cu2++H2O(H+・OH-) Cu2++2H2O 又如 NaHCO3水解;参与水解的是,生成对应的阴离子OH-。
4.通式法。这是最好,最死板的方法。 如Al2(SO4)3: 按照通式:Mn++nH2O 即可 得出:Al3++3H2O 又如Na3PO4: 按照通式:Am-+H2O A-+H2O 即可得出:
|
【本文地址】