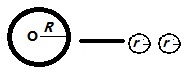| 科学网 | 您所在的位置:网站首页 › 开尔文公式用于计算弯曲液面的什么性质 › 科学网 |
科学网
|
热力学基本方程在表面化学中的几个应用
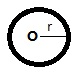
已有 5484 次阅读 2022-1-15 07:03 |系统分类:教学心得 含有表面张力的热力学基本方程为[1]:dG=γ▪dAs=-S▪dT+V▪dp+δW' (1) 本文尝试将式(1)用于拉普拉式方程、毛细管液面上升高度、开尔文公式及吉布斯吸附等温式的推导. 表面化学通常不涉及化学反应或相变,如果不特别强调, 式(1)中有效功恒为0,即:δW'≡0. 拉普拉斯方程推导 本文讨论气泡成长及液滴分散两种情况下的拉普拉斯方程。 1.1 气泡成长 气泡示意图参见图1
图1 气泡示意图 气泡的初始半径为r,气泡的体积V=4/3▪πr3, 表面积As=4π▪r2,dAs=8πr▪dr; 另假设气泡成长过程恒温(dT=0),δW'≡0, 此时式(1)可化简为:dG=γ▪dAs=V▪dp (2) 将dAs及V代入可得:γ▪8πr▪dr=4/3▪πr3▪dp 化简并积分可得:p2-p1=-6γ(1/r2-1/r1) (3) 式(3)中p2、p1分别代表气泡终态与初态的附加压力(下同);r2、r1依次代表气泡终态与初态的曲率半径; 假设气泡终态曲率半径r2=∞, 此时气泡近似视为平面液体,其附加压力p2≈0,将r2、p2分别代入式(3)可得:p1=-6γ/r1 (4) 整理式(4)可得:Δp=-6γ/R (5) 式(5)即为气泡成长过程对应的拉普拉斯方程;Δp为气泡的附加压力;γ为液体的表面张力;R为气泡的曲率半径. 由式(5)可见,气泡曲率半径越大,附加压力亦越大. 1.2 液滴分散 液滴分散过程参见图2
图2 液滴分散过程示意图 大液滴的初始半径为 R,小液滴半径为r. 分散过程系统总体积保持恒定,V=4/3▪πR3;一个小液滴体积V小=4/3▪πr3; 分散得到小液滴数目:n=V/V小=V/(4/3▪πr3) n个小液滴的总表面积: As=n▪4πr2=3V/r (6) 另约定液滴分散过程恒温(dT=0),δW'≡0, 此时式(2)可化简为:γ▪(-3V/r2)▪dr=V▪dp 上式整理并积分可得:p2-p1=3γ(1/r2-1/r1) (7) 假设大液滴初始半径r1=∞,p1=0,此时式(7)可化简为: p2=3γ(1/r2) (7) 整理式(7)可得:Δp=3γ/R (8) 式(8)即为液滴分散过程对应的拉普拉斯方程;Δp为气泡的附加压力;γ为液体的表面张力;R为小液滴的曲率半径. 由式(8)可知:液滴曲率半径越小,附加压力越大. 1.3 拉普拉斯方程通式 结合式(5)及(8),提出弯曲液面的拉普拉斯方程通式如下: Δp=k▪γ (9) 式(9)中Δp为弯曲液面的附加压力;γ为液体的表面张力;k称为拉普拉斯系数. 由于弯曲液面的曲率半径不易准确测定,测量过程通常选取蒸馏水作为参比物获取拉普拉斯系数k. 2. 毛细管液面上升高度 毛细管液面上升高度参见图3
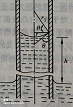
图3 毛细管液面上升高度示意图 由式(9)可得: Δp=k▪γ =ρgh 整理上式可得:h=k▪[γ /(ρg)] (10) 式(10)中,h为毛细管内液面上升高度,γ 为毛细管内液体的表面张力,ρ为毛细管内液体密度,g为重力加速度. 式(10)可进一步整理为:h=K▪γ (11) 式(11)中K称为毛细管常数,可通过参比物蒸馏水确定. 3. 微小液滴的饱和蒸气压-----开尔文公式推导 微小液滴蒸发过程参见图4.
图4 微小液滴蒸发过程示意图 图4中过程①、③分别是半径为R、r的液滴恒温可逆蒸发;过程②是半径为R的大液滴分散为半径为r的小液滴;过程④理想气体恒温压缩过程,其蒸汽压由pR增大至pr. 由图4循环可得:ΔG1+ΔG4=ΔG2+ΔG3 依题:过程①、③为液滴恒温可逆蒸发,ΔG1、ΔG3均为0, 则:ΔG4=ΔG2 依题过程②:ΔG2=∫(γ▪dA)=γ▪(A2-A1)=γ▪{4πr2▪[V/(4/3▪πr3)]-4πR2} 整理可得: ΔG2=3V γ▪(1/r-1/R) (12) 式(12)中V、R分别为大液滴体积与半径,r为小液滴的半径. 过程④:ΔG4=∫[(nRT/p)▪dp]=nRT▪ln(pr/pR) (13) 由上可得:nRT▪ln(pr/pR) =3Vγ▪(1/r-1/R) RT▪ ln(pr/pR)=3Vγ▪(1/r-1/R)/(n)=3Vmγ▪(1/r-1/R) (14) 式(14)中Vm表示大液滴的摩尔体积. 如果将大液滴视为平面水,则:1/R→0,可忽略.,此时式(14)可化简为: RT▪ ln(pr/p)=3Vmγ▪(1/r) (15) 式(15)即为微小液滴的饱和蒸气压对应的开尔文公式. 式(15)中p为平面水的饱和蒸气压. 需要强调:用式(15)计算气泡的饱和蒸气压时,曲率半径带负值. 4. 吉布斯吸附等温式推导 溶质的表面吸附量为系统单位表面积所含有的溶质的物质的量,表示为:Γ=nB/As. 上式中Γ称溶质的表面吸附量,也称表面过剩, 单位为mol/m2; nB为溶质B的物质的量,单位为mol;As为系统的表面积,单位为m2. 对于单相二组分(α+β)液相系统: G=γ▪As (16) dG=γ▪dAs (17) G=Gα+Gβ=nα▪μα+nβ▪μβ (18) dG=μα▪dnα+μβ▪dnβ (19) 式(16)+式(18)可得:2G=γ▪As+nα▪μα+nβ▪μβ (20) 2dG=γ▪dAs+As▪dγ+nα▪dμα+μα▪dnα+nβ▪dμβ+μβ▪dnβ (21) 式(17)+(19)可得:2dG=γ▪dAs +μα▪dnα+μβ▪dnβ (22) 对比式(21)与式(22)可得: As▪dγ+nα▪dμα+nβ▪dμβ=0 移项:As▪dγ=-nα▪dμα-nβ▪dμβ 等式两边同除以As:dγ=-(nα/As)▪dμα-(nβ/As)▪dμβ 又因为Γi=ni/As,代入可得:dγ=-Γα▪dμα-Γβ▪dμβ 如果α组分为溶剂水,则上式可化简为:dγ=-Γβ▪dμβ (23) 对于单相多组分系统,μβ=μ*β+RT▪lnαβ dμβ =RT▪d(lnαβ) (24) 将式(24)代入式(23)可得:dγ=-Γβ▪RT▪d(lnαβ) 整理上式可得:Γβ=-[αβ/(RT)]▪(dγ/dαβ) (24) 式(24)即为吉布斯吸附等温式. 5.结论 ①拉普拉斯方程通式为 Δp=k▪γ ; ②毛细管液面上升高度:h=K▪γ ; ③开尔文公式为:RT▪ ln(pr/p)=3Vmγ▪(1/r); ④吉布斯吸附等温式为: Γβ=-[αβ/(RT)]▪(dγ/dαβ). 参考文献 [1]余高奇. 表面张力的客观性. 科学网博客, 2022,1 https://blog.sciencenet.cn/blog-3474471-1321074.html 上一篇:“表面张力”的客观性下一篇:ΔG的物理意义与实例剖析 收藏 IP: 27.18.14.*| 热度| |
【本文地址】