| MED焦点 | 您所在的位置:网站首页 › 左旋多巴治疗帕金森病的注意事项有 › MED焦点 |
MED焦点
|
PD的发病机制复杂,其病因和确切机制迄今尚不清楚,较公认的学说是帕金森病是一种神经系统变性疾病,与纹状体内的多巴胺(DA)含量显著减少有关。DA合成减少使纹状体DA含量降低,黑质-纹状体通路多巴胺能与胆碱能神经功能平衡失调,胆碱能神经元活性相对增高,使锥体外系功能亢进,发生震颤性麻痹。 但在2017年,美国拉霍亚免疫学研究所(LJI)的科学家发现,一些T细胞会将α-突触核蛋白(α-synuclein)当作靶标,它们会错误的攻击地攻击大脑细胞,导致帕金森病的进展。而这一发现,可以猜测帕金森病更有可能也是自身免疫疾病。LJI科学家的发现,让我们可以针对T细胞来监测和延缓疾病的进展,甚至治疗帕金森病。
目前,抗帕金森药物治疗作为首选,且是整个治疗过程中的主要治疗手段。国内外已上市的抗帕金森病药物主要包括多巴胺能药物以及非多巴胺能药物。多巴胺能药物包括:复方左旋多巴、多巴胺受体激动剂(DAs)、单胺氧化酶B型抑制剂(MAO‐BI)、儿茶酚-O-甲基转移酶抑制剂(COMTI),非多巴胺能药物包括:抗胆碱能药物、抗谷氨酸能药物和腺苷A2受体拮抗剂。抗帕金森病药物的应用及注意事项如下表所示:
除以上药物治疗以外,临床上通常需要针对帕金森的运动症状和非运动症状采取与手术治疗、肉毒毒素治疗、运动疗法、心理干预、照料护理等疗法结合的全面综合治疗。而无论哪种治疗方式,都只能改善症状,不能阻止病情的发展,更无法治愈。因此,临床上亟待开发探索能成功治疗帕金森病的新方法,来帮助每一位深受帕金森病折磨的人。 目前,抗帕金森治疗药物临床试验方兴未艾,有帕金森病研究组织针对美国国立卫生研究院网站(clinicaltrials.gov)上登记注册的共145项有关帕金森病药物临床试验作了一项统计分析(数据截至2020年01月21日),有57项(39%)临床试验是疾病长期改善(Disease Modifying Therapies,DMT)治疗,其余88项(61%)是对症治疗(Symptomatic Therapies, ST),其中51项(35%)处于1期临床,66项(46%)处于2期临床,28项(19%)处于3期临床。
随着对帕金森病发病机理的深入研究,一些具有治疗潜力的新兴疗法正在进行临床试验或即将进入临床试验,有望改善、控制甚至逆转帕金森病,造福帕金森病患者。
干细胞(StemCells)是一类具有自我更新复制能力和多向分化潜能的细胞,在合适的条件下或给予适当的刺激,干细胞可以分化成为任何一种成体组织细胞,包括多巴胺能神经元,这种能力为成功治疗帕金森病在内的神经变性疾病提供了可能。 自1979年研究人员在大鼠动物实验中首次利用细胞移植疗法治疗帕金森病以来,越来越多具有治疗潜力的帕金森病干细胞疗法进入到实质性临床研究中。 截至目前,在clinicaltrials.gov上注册的有关干细胞应用于帕金森病临床治疗的临床研究有32项,其中涉及的干细胞类型主要有神经干细胞、胚胎干细胞、间充质干细胞和诱导多能干细胞等。 研究表明,不同类型和不同来源的干细胞在帕金森病治疗中均能够发挥神经再生与修复的作用。干细胞移植治疗帕金森病主要作用机制是利用其分泌神经营养因子、免疫调节等发挥神经保护功能,促进损伤的多巴胺能神经元修复,或者将其诱导分化为多巴胺能神经元替代体内损伤的多巴胺能神经元,发挥细胞替代作用。 其中获得2012年度诺贝尔生理学或医学奖的诱导多能干细胞(induced Pluripotent Stem Cell, iPSC)技术在帕金森病干细胞疗法领域被寄予厚望。2020年5月14日,国际顶级权威医学期刊《The New England Journal of Medicine》以简报的形式报道了一例帕金森病患者接受自身中脑多巴胺能前体细胞移植后病情好转的案例。多巴胺能前体细胞是在体外从自体iPSC分化而来,这些细胞具有黑质致密部神经元的表型特性,在人源化小鼠模型的实验中显示这些细胞缺乏免疫原性。随后,这些细胞被分两次、间隔6个月植入到这名帕金森患者体内,移植部位分别为左半球和右半球的壳核。移植手术进行18-24个月后患者帕金森症状趋于稳定甚至有所改善。 拜耳全资子公司BlueRockTherapeutics在2022年1月18日宣布在与University Health Network合作开展的一项用iPSC来源的多巴胺能神经元细胞(DA01)治疗帕金森病的1期开放标签临床试验中,已经完成对加拿大首位晚期帕金森病患者给药。DA01是一种多能干细胞衍生的多巴胺能神经元,有潜力再生机体失去的生理功能,并可能改善和逆转帕金森病。DA01通过手术移植到患者的大脑中,融入大脑并恢复失去的生理功能。这种治疗方法如果获得成功,将会对帕金森病的治疗带来重大进步。
2022年1月10日,美国CA Huntington Beach分子医学研究所(IMM)与其合作伙伴在《npj Vaccines》上发表了一篇研究论文。他们认为,大脑中错误折叠的蛋白如淀粉样蛋白-β(Aβ)、τ蛋白和α突触核蛋白(α-synuclein,α-Syn)的积累会导致突触功能障碍、神经元损伤以及相关神经退行性疾病的发作。而路易体痴呆(DLB)和帕金森病(PD)是以病理性α-Syn的异常积累为特征,从而导致与炎症相关的神经性病变,而高浓度α-Syn抗体可以抑制或减少这种病理性分组在大脑中的扩散。 该研究团队运用MultiTEP平台技术设计了4种针对病理性α-突触核蛋白的DNA疫苗,可靶向该病理分子的3个淋巴B细胞表位,旨在诱导产生高水平特异性的α-突触核蛋白抗体,分别命名为PV-1947D、PV-1984D、PV-1949D、PV-1950D。这4种疫苗在PD或DLB模型小鼠体内均诱导了高滴度特异性的α-突触核蛋白抗体,显著改善了PD/DLB样病理。其中以PV-1950和PV-1950D的疫苗接种获得的效果最显著,且雌性小鼠对疫苗的抗体反应水平高于雄性小鼠,均可显著性减少小鼠大脑中α-突触核蛋白和改善神经退行性病变。 基于以上临床前研究的基础,他们最终选择了PV-1950D疫苗作为未来IND候选疫苗,期待进一步取得突破性进展应用于临床。
基因治疗(Gene Therapy)是一种旨在通过基因修饰细胞来缓解相关症状甚至逆转疾病进展来治疗疾病的一种方法。对于帕金森病,基于多巴胺能神经元的丢失或相关神经递质失衡的病理基础,基因治疗技术通过将目的基因导入到特定脑区影响特异性蛋白表达来缓解帕金森病。 自2003年8月1日第一项帕金森病基因治疗研究至今,有多种基因治疗药物已进入临床试验阶段。根据作用机制,大致可以分为以下几类: (1) 营养因子类,如CERE-120、AAV2-GDNF,通过营养多巴胺神经元细胞从而改善疾病进程,缓解症状; (2) 多巴胺合成关键基因或疾病代谢途径关键酶基因替代治疗,如AADC、ProSavin、OXB-102均是多巴胺合成的关键酶基因,而GAD合成的抑制性神经递质在运动通路平衡中起到重要作用,PR001A在帕金森病患者能量代谢过程中起到重要作用; (3) 基因表达调控,BIIB094阻断LRRK2突变患者蛋白质翻译,控制疾病。 目前已结束的临床试验结果显示,基因治疗虽然不同程度上改善了帕金森病患者的临床症状,但各种不良反应以及其他限制疗效的问题也随之出现,临床上亟待优化帕金森病基因治疗的基因载体以改善有效性和安全性。 尽管帕金森病的新兴疗法取得了很大的进展,已显现的一些积极结果预示着这些疗法在PD治疗中具有广阔前景,但也会因各种随之而来的问题限制临床应用,需要进一步的研究以及临床试验验证。我们期待着开启帕金森病治疗的新时代! 主要参考文献资料: [1] 中华医学会神经病学分会帕金森病及运动障碍学组, 中国医师协会神经内科医师分会帕金森病及运动障碍学组. 中国帕金森病治疗指南(第四版)[J].中华神经科杂志, 2020, 53(12):14. [2] Dorsey E R , Constantinescu R ,Thompson J P , et al. Projected number of people with Parkinson disease in themost populous nations, 2005 through 2030.[J]. Neurology, 2007, 68(5):384-386. [3] Scientists uncover new targets fortreating Parkinson's disease. Retrieved Mar 22th, 2022 from https://medicalxpress.com/news/2022-03-scientists-uncover-parkinson-disease.html [4] Mcfarthing K , Buff S , Rafaloff G , et al. Parkinson's Disease Drug Therapies in the ClinicalTrial Pipeline: 2020[J]. Journal of Parkinson's Disease, 2020, 10(3):757-774. [5] Perlow M , Freed W , Hoffer B , etal. Brain grafts reduce motor abnormalities produced by destruction ofnigrostriatal dopamine system[J]. Science, 1979, 204(4393):643-647. [6]. Schweitzer J S , Song B , HerringtonT M , et al. Personalized iPSC-Derived Dopamine Progenitor Cells forParkinson's Disease[J]. New England Journal of Medicine, 2020,382(20):1926-1932. [7] CAMBRIDGE, Mass., January 18, 2022.BlueRock Therapeutics Announces First Patient Dosed in Canada in Phase 1 Trialin Patients with Advanced Parkinson’s Disease. https://media.bayer.com/baynews/baynews.nsf/id/BlueRock-Therapeutics-Announces-First-Patient-Dosed-Canada-Phase-1-Trial-Patients-Advanced?Open&parent=news-overview-category-search-en&ccm=020 [8] Kim et al., (2022). Efficacy andimmunogenicity of MultiTEP-based DNA vaccines targeting human α-synuclein:prelude for IND enabling studies. npj Vaccines [9] 周凯歌, 张敬星, 靳令经. 帕金森病基因治疗临床注册研究进展[J]. 中华神经科杂志, 2020, 53(12):5.
|
【本文地址】


 摘自《中国帕金森病治疗指南(第四版)》
摘自《中国帕金森病治疗指南(第四版)》
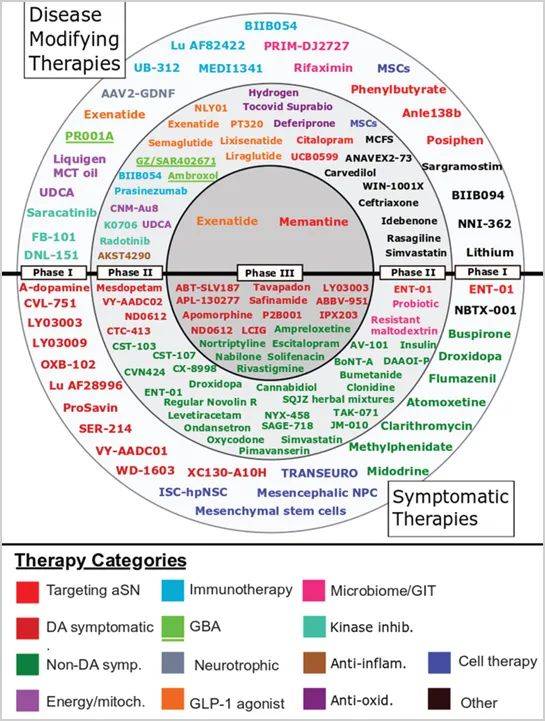 截至2020年01月21日,ClinicalTrials.gov公示的PD药物临床试验中的药物(按临床分期、DMT/ST
截至2020年01月21日,ClinicalTrials.gov公示的PD药物临床试验中的药物(按临床分期、DMT/ST



 返回搜狐,查看更多
返回搜狐,查看更多