| 初中化学 | 您所在的位置:网站首页 › 化学电子排布图规律 › 初中化学 |
初中化学
|
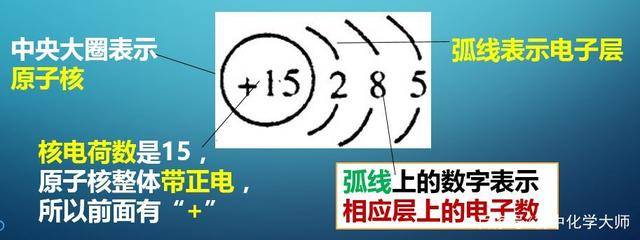
电子,又称核外电子,也就是原子核外面的电子。那么每一层的电子是随便画的吗?一般的原子有多少个电子层呢?层与层之间有什么区别呢? 核外电子是分层运动的,又称为分层排布,我们现在已经知道的原子,相应的核外电子,最少的1层,最多的7层。从里往外数的话,是第1层、第2层…。 那么每层最多容纳的电子的数量(电子数),是平均的吗?这些数字是否有什么规律呢? 研究结果表明,第1层最多容纳两个电子,第2层最多容纳8个电子,最外层最多容纳8个电子。如果原子只有1层,那么这,我们初中化学,只要求掌握元素周期表前20种元素的核外电子排布规律,如图: 因为原子都是电中性的,所以原子核内有多少个质子(即带多少个正电荷),核外电子也就有多少个(即带多少个负电荷),也就是: 圈里的数字=第1层数字+第2层数字+…+最外层数字 可以看出,前20种元素,从内到外的规律是288, 以磷原子的原子结构示意图为例:
数学规律:每层的最多的电子数是 2n^2(2n的平方)。 2能量规律 核外电子的运动状态是不同的。因为原子核带正电、电子带负电,所以离核近的电子能量较低,离核远的电子能量较高。能量较低的意思,可以理解为较为稳定,能量较高的意思就是容易与其他电子“手拉手”。(电子和电子层的关系,可以理解为“能量绑定”,这一点我们在后面离子的形成会详细介绍) 在化学变化中,原子的最外层电子容易得或者容易失去,所以原子的化学性质与原子的最外层电子数量有密切的联系。 原子的最外层,最多容纳8个电子,所以关键的数字就是4和8,4是一半,8是满的。 我们再观察前20种元素的 核外电子排布示意图: 3核外电子排布规律 简单介绍一下规律: 1.位于最右侧的稀有气体原子,最外层都是满的(2个或8个),化学性质比较稳定,很难与其他物质发生反应; 2.位于偏右侧的,非金属元素的原子,最外层电子数一般都是大于4的,比较容易得到电子(以氧原子为例:); 3.位于偏左侧的,多是金属元素的原子,最外层电子数一般都是小于4的,比较容易失去电子(以钠原子为例:) 像碳、硅这种最外层电子数等于4的,有时候得,有时候失,既不易得电子,也不易失电子。 4小结 至于原子在化学变化中,到底得几个电子或者是几个电子,我们在下面的课程会从物质的形成来详细分析。
举报/反馈返回搜狐,查看更多 |
【本文地址】