| 含氧量计算学习笔记 | 您所在的位置:网站首页 › 亨利常数和亨利系数 › 含氧量计算学习笔记 |
含氧量计算学习笔记
|
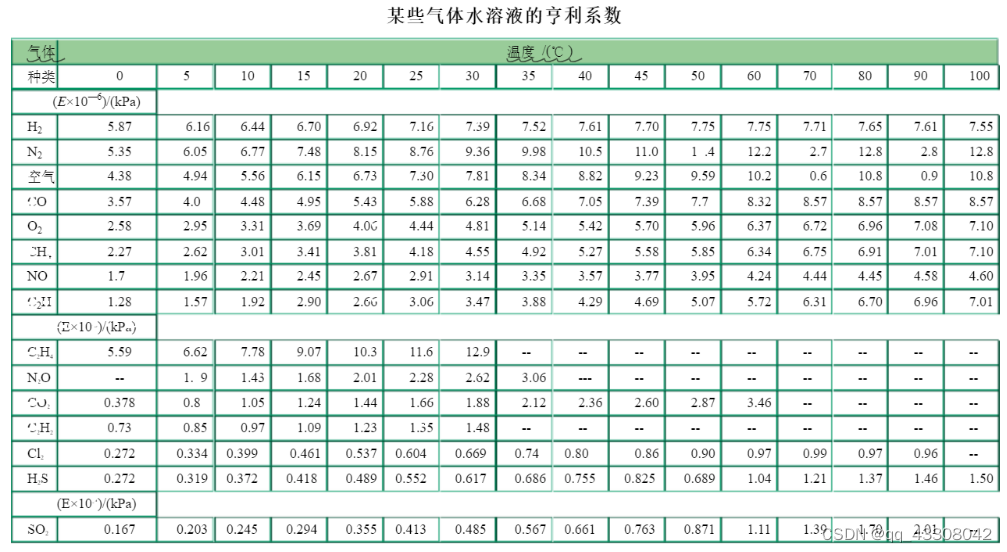
亨利在研究一定温度下气体在液体中的溶解度时,发现一定温度下气体在液体中的溶解度和该气体的平衡分压成正比,正比例常数(即亨利系数)的数值决定于温度、压力以及溶质和溶剂的性质。 亨利定律表达式:p=E*X. P:氧气在水上空的分压。 E:氧气在给定温度下的亨利系数。 X:氧气在水中的摩尔分数。 注:1mol=6.02*10^23个原子或分子。 相对原子质量是指以一个碳-12原子质量的1/12作为标准,任何一个原子的真实质量跟一个碳-12原子质量的1/12的比值,称为该原子的相对原子质量。原子量为质量单位,符号位u,它的定义为碳-12原子质量的1/12。(一个碳-12原子质量为1.993*10^-26KG) 可知:标准大气压为101.325kpa,大气中含氧量为21%。 求得氧气在水上空的分压P=101.325*0.21=21.28kpa。 查到氧在水中的亨利系数常数E=(2.55+0.073T)*大气压。(T为温度℃) 因不知道此处大气压为多少(学的都已经还给老师了),直接百度查表了。 由百度文库查到气体在水溶液中的亨利系数表如下:
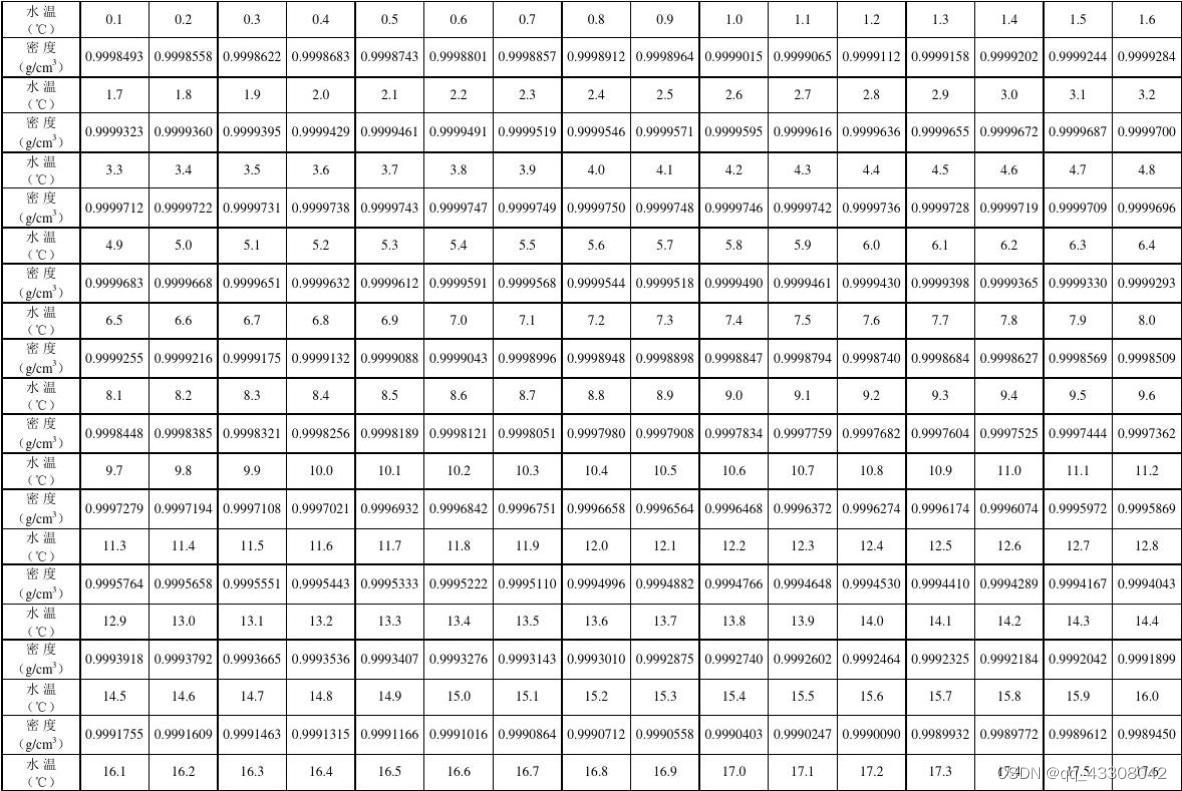
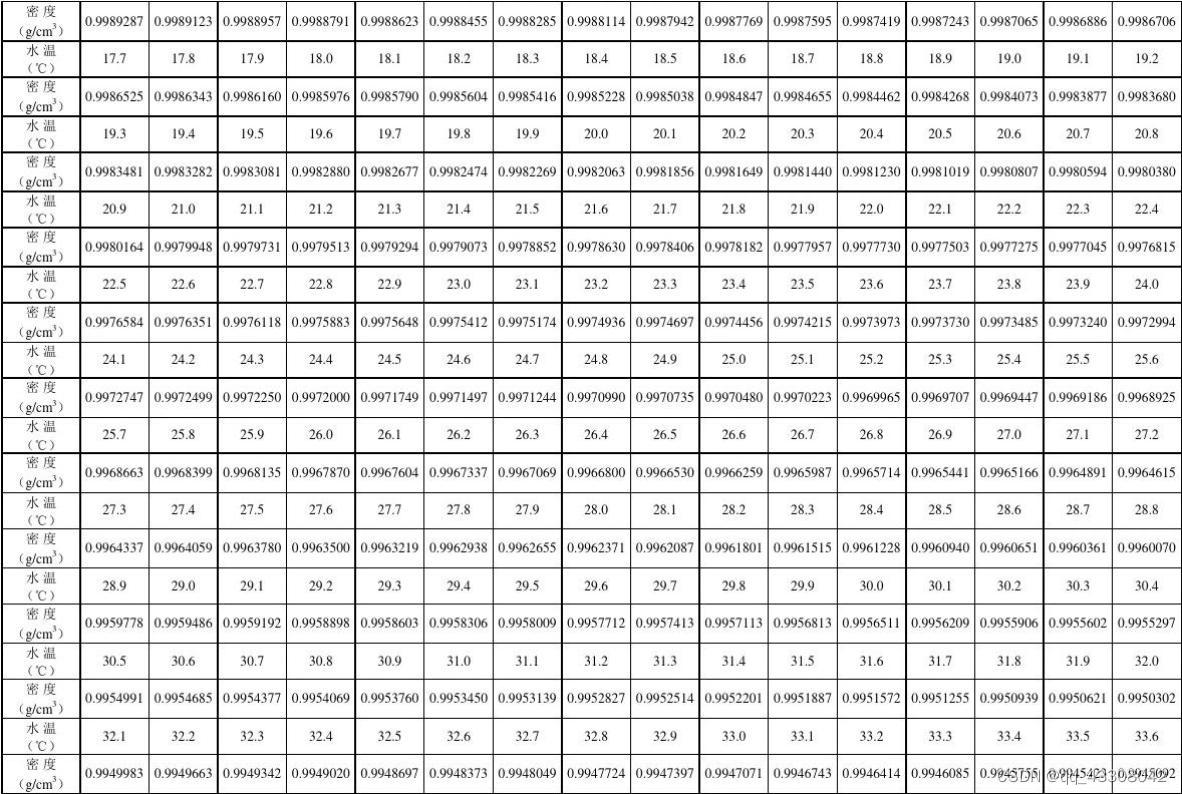
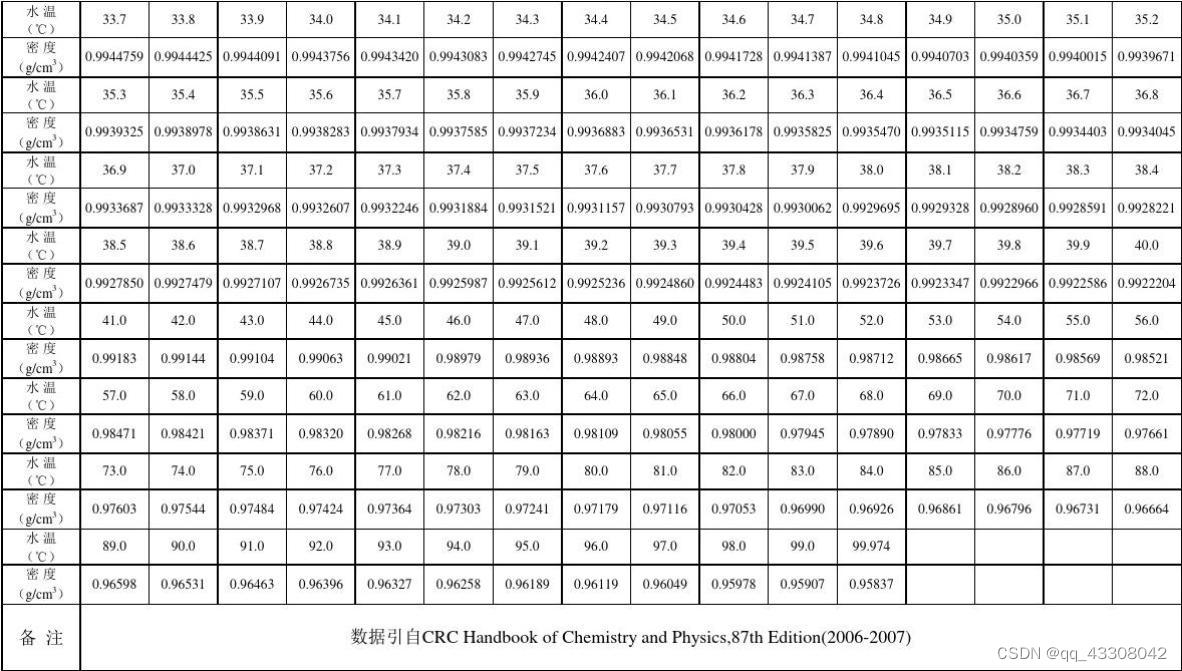
在30摄氏度时,亨利系数E=4.81*10^6 kpa。 X(氧气在水中的摩尔分数)=P(氧气在水上空的分压)/E=21.28/(4.81*10^6)=4.424*10^-6 查到水在不同温度时的密度表如下:
由表查得30℃水密度为995.65g/L,每升水的摩尔数为995.65/18=55.313mol(1mol水分子为18g)。 前面计算得到X(氧气在水中的摩尔分数)为4.424*10^-6。 1L水中氧气含量为=55.313*4.424*10^-6=0.000235mol 氧气分子质量为32g/mol,1L水中氧气质量=0.000235*32=0.00752kg=7.52mg |
【本文地址】