| 常见手性小分子催化剂 | 您所在的位置:网站首页 › trip怎么念 › 常见手性小分子催化剂 |
常见手性小分子催化剂
|
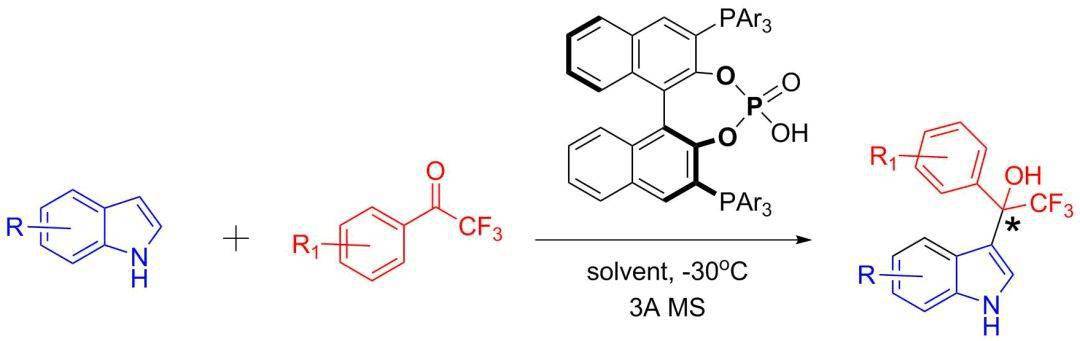
【Org. Lett. 2018, 20, 590−593】 Steven R. Kass等人报道了2,2,2-三氟苯乙酮在吲哚3-位进行非常规Friedel–Crafts 烷基化反应,可以达到96%的产率和96%的ee值。
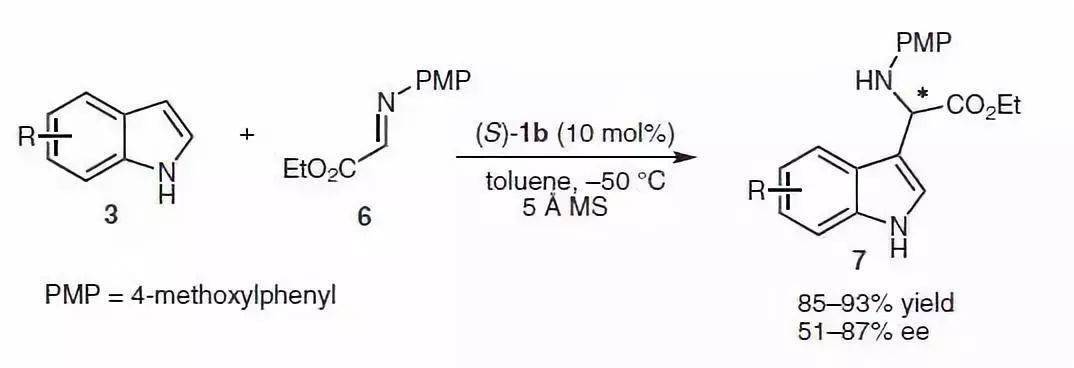
【 Org. Lett. 2018, 20, 2689−2692】 手性磷酸催化下丙酮酸的亚胺对吲哚进行不对称 Friedel–Crafts反应,得到手性氨基酸。
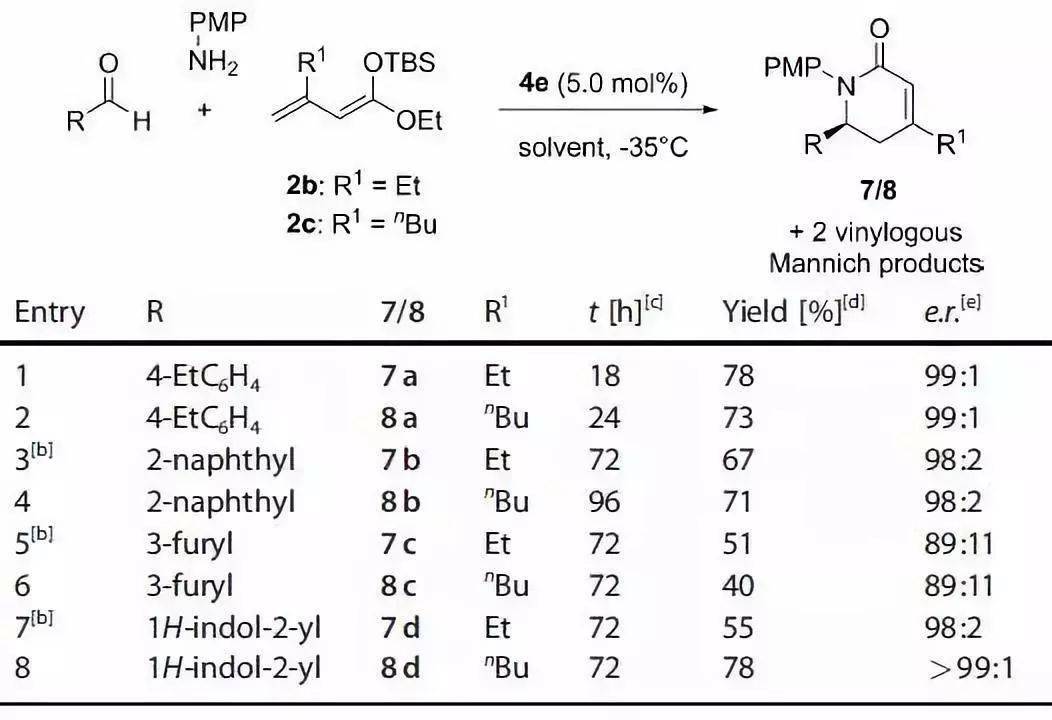
【 Synlett 2010, 9, 1289–1301】 二、 Mannich反应 用于常规的 Mannich反应 取得很好的效果。
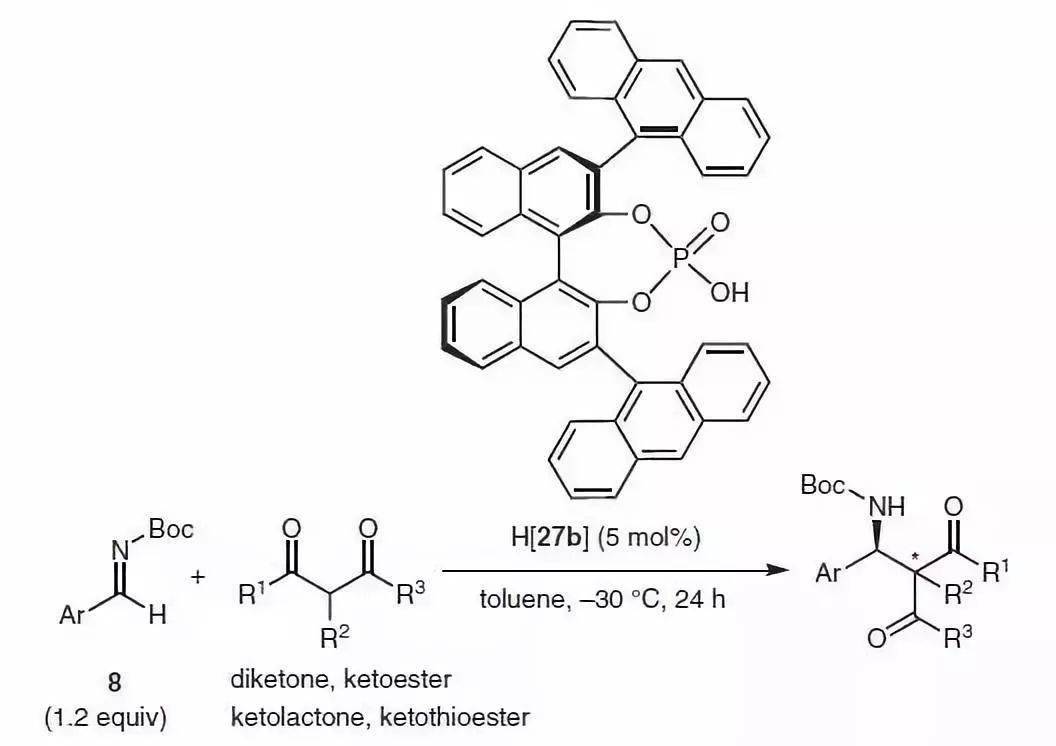
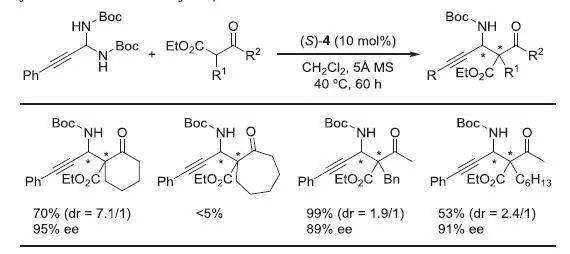
【 Synthesis 2010, 3785–3801】 N-Boc-苯乙炔胺缩甲醛和β-酮酯进行对映选择性Mannich-类型反应。并取得很好的对映选择性结果。
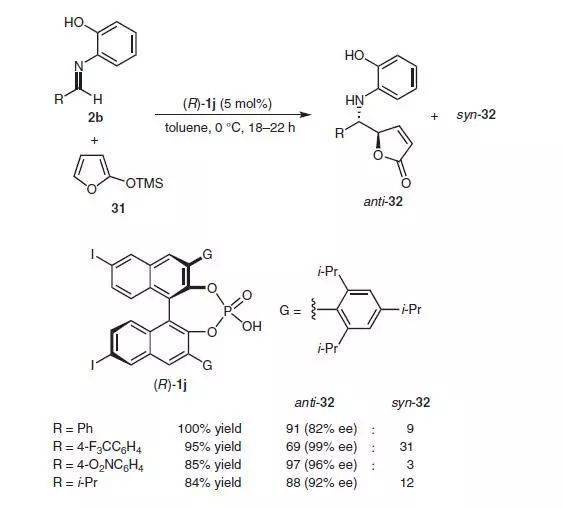
手性磷酸催化下三甲基硅基呋喃和亚胺进行不对称烯基-Mannich反应,取得了很高的产率和对映选择性。
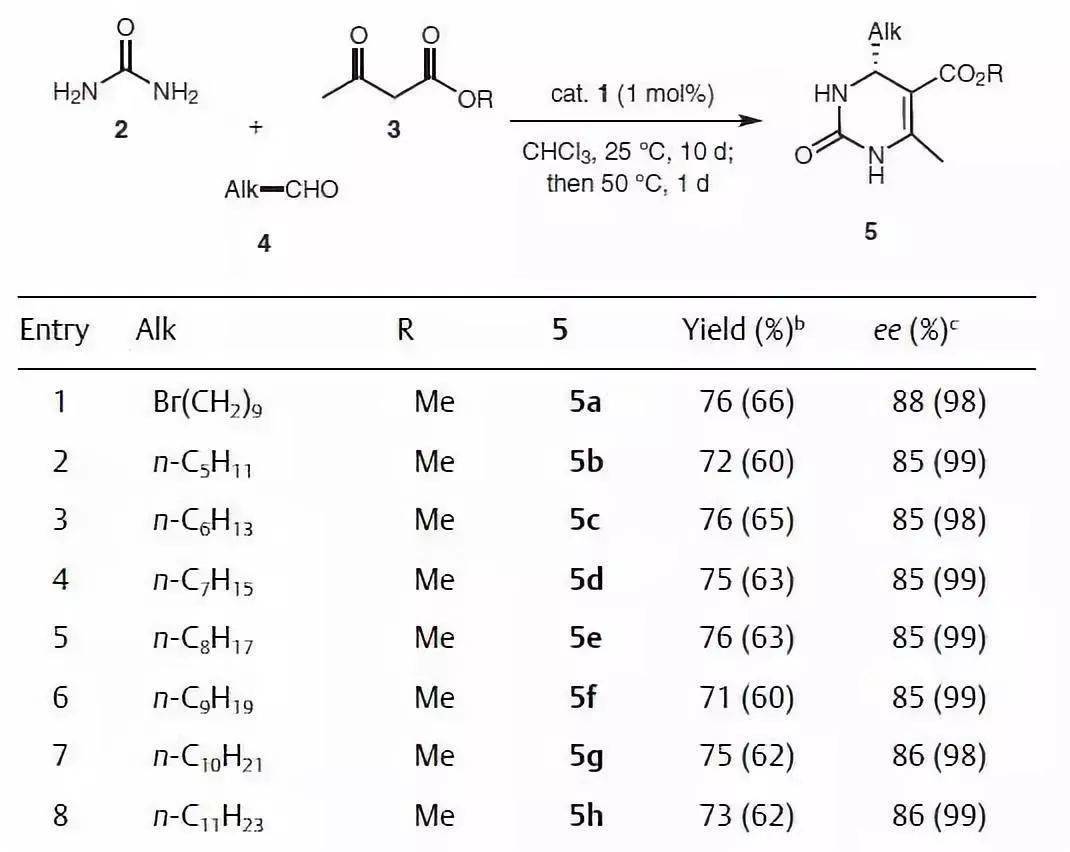
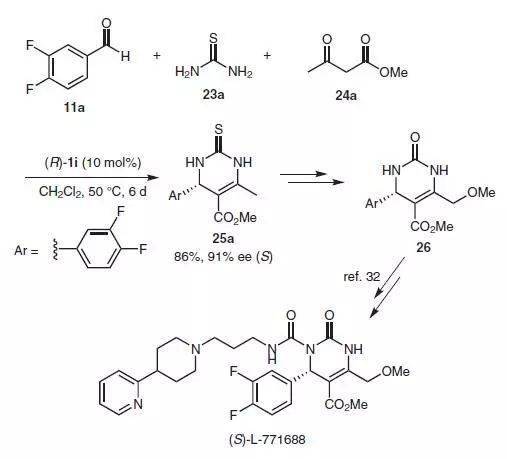
【 Adv. Synth.Catal. 2008, 350, 399 】 三、 Biginelli反应 手性磷酸催化的对映选择性 Biginelli反应 ,取得很高的产率和ee值。
【 Synthesis 2018, 50, 2394–2406】
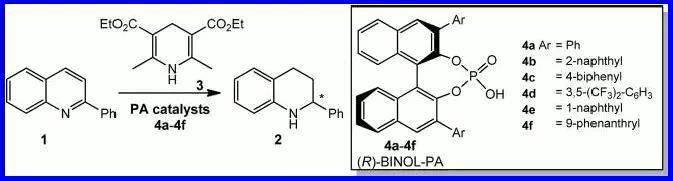
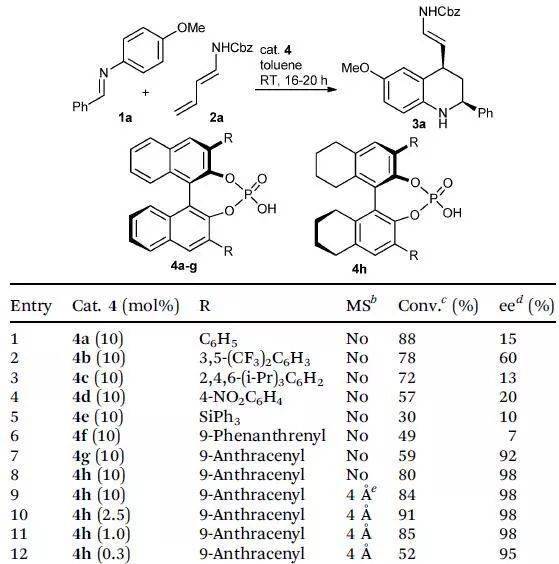
【 J. Org. Chem. 2008, 73, 7651】 四、不对称氢转移反应 ( R )-BINOL衍生的手性磷酸配体催化下2-苯基喹啉和Hantzsch酯反应进行不对称氢转移反应得到手性的四氢喹啉。
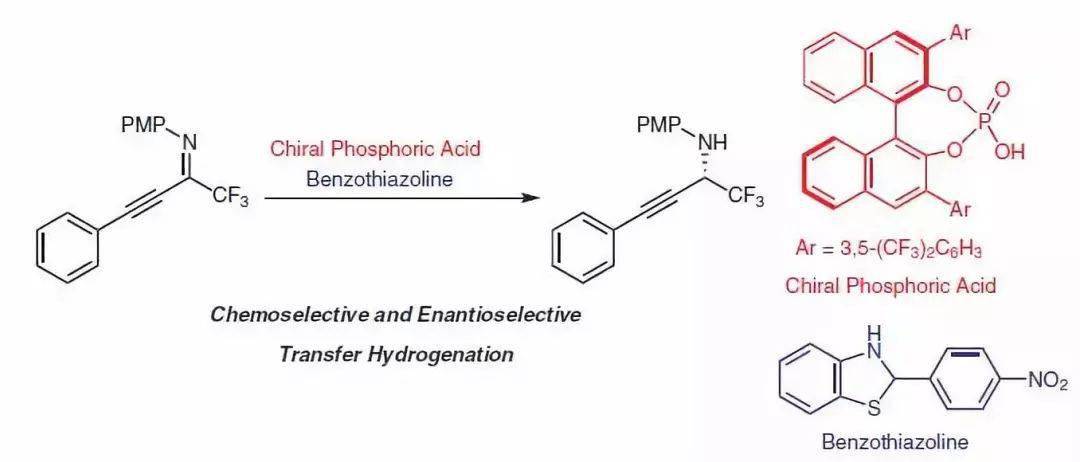
【 J. Org. Chem. 2018, 83, 2779−2787】 亚胺的 不对称氢转移反应,当Hantzsch酯的氢转移效果不好是,可以考虑使用苯并噻唑啉作为氢源。
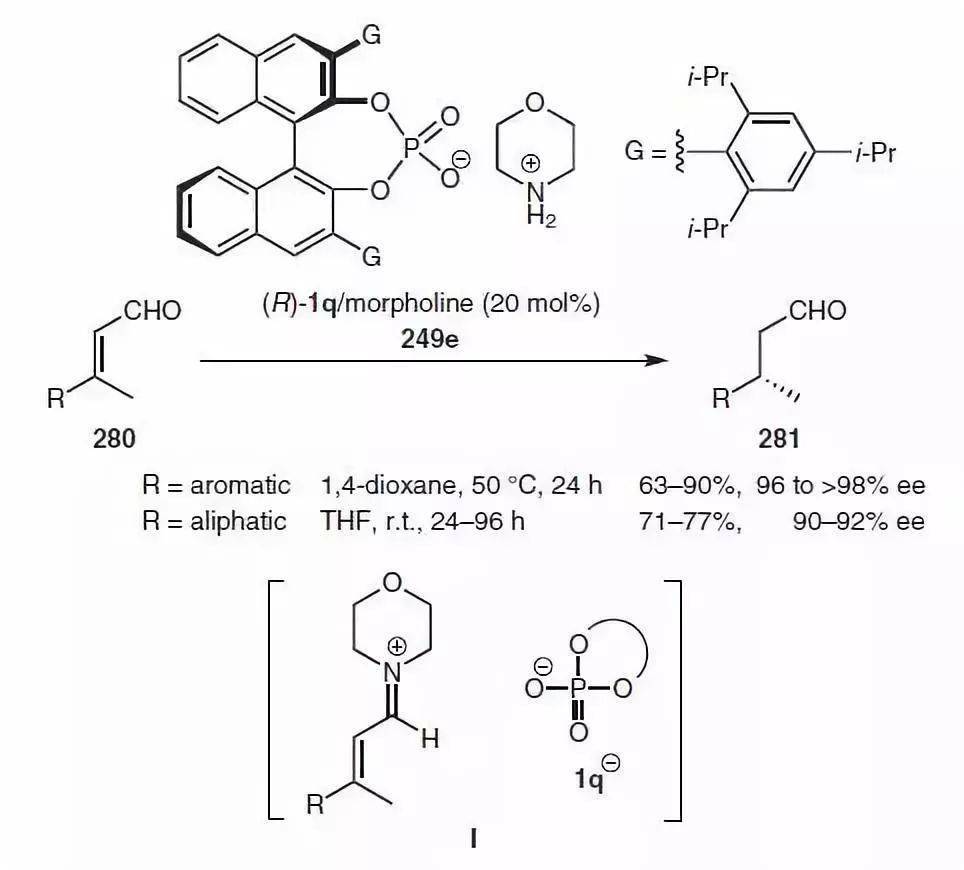
【 Synlett 2018, 29, 1607–1610】 α ,β-不饱和醛,在手性磷酸的吗啡啉盐催化下, Hantzsch酯作为氢源,进行 不对称氢转移反应。取得了很高的产率和ee值。
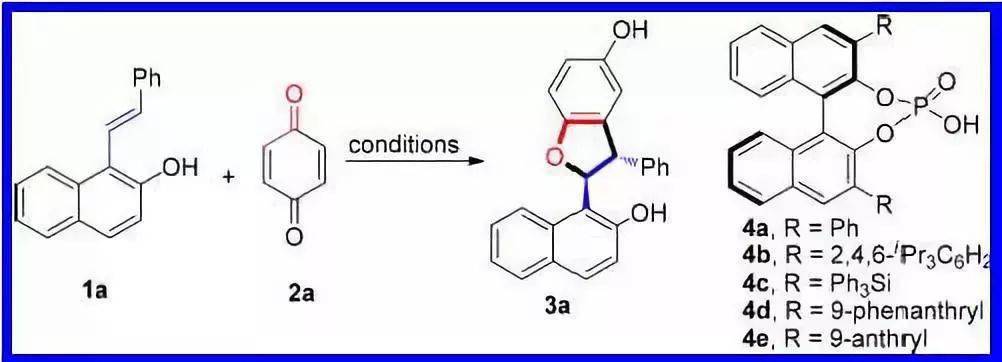
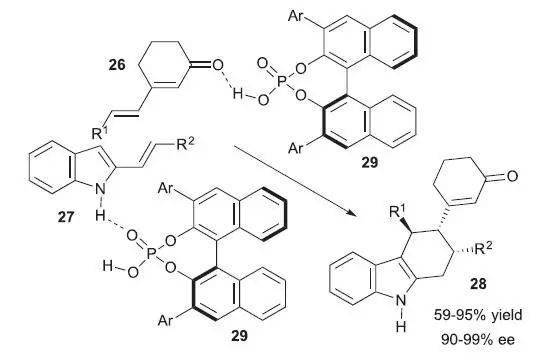
【 Angew. Chem. Int. Ed. 2006, 45, 4193】 五、不对称环加成反应 手性磷酸催化下( E )-1-苯乙烯基萘酚和1,4-苯醌进行对映选择性的[3 + 2]环加成反应取得很好的结果(up to99% yield, >20:1 dr, 99% ee)。
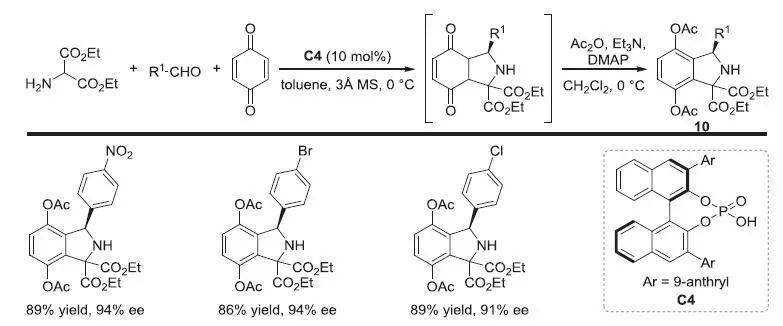
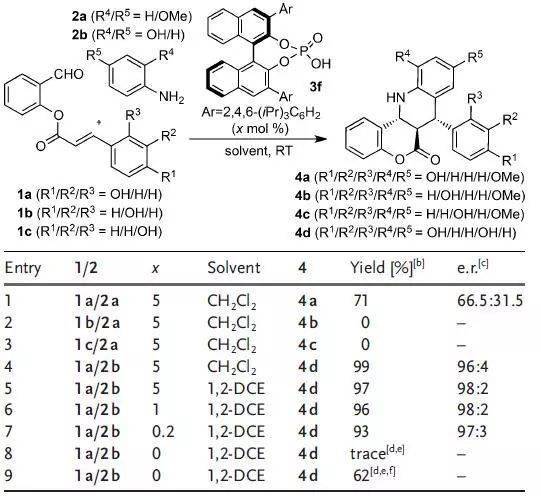
【 Org. Lett. 2018,20, 2929−2933】 胺先和醛生成亚胺,在手性磷酸催化下,再与苯醌进行[3+2]环加成反应。
【 Tetrahedron Letters 2018, 59, 473–486】 双功能催化剂的手性磷酸,同时催化两个底物进行不对称 Diels-Alder反应 。
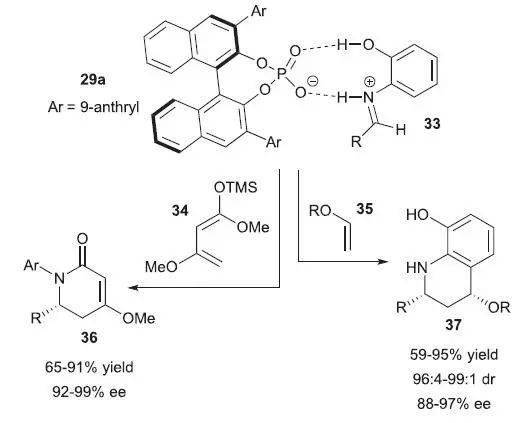
手性磷酸催化下亚胺作为杂亲二烯体进行不对称 Hetero-Diels–Alder反应 。
【 Chem. Eur. J. 2017, 23, 513 – 518】 Povarov反应 作为 反电子流向的Hetero-Diels–Alder反应,也可以在手性磷酸催化下反应,并得到很好的非对映选择性。
【 Angew. Chem. Int. Ed. 2017, 56, 10573 –10576】 手性磷酸催化下1- N -酰胺基-1,3-丁二烯的端基双键和 N -芳基亚胺进行烯基 Povarov反应 ,取得很高的产率和ee值。
【 Chem. Commun. , 2013, 49, 880-882】 六、其他类型反应 1、不对称 Pictet-Spengler反应
【 Org. Lett. , 2011,13, 5636–5639】 2、不对称 Robinson关环反应
【 Eur. J. Org. Chem. 2012, 4508–4514】 3、氮杂- Pinacol重排反应
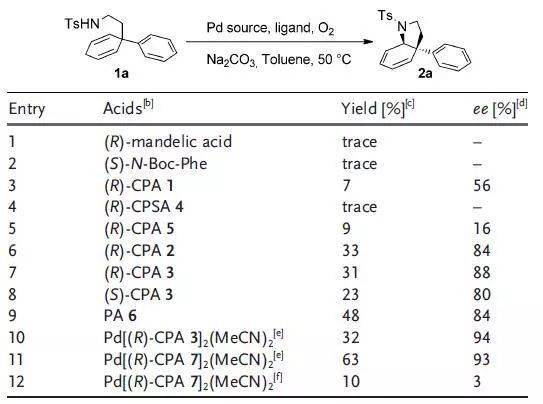
【 Angew. Chem. Int. Ed. 2017, 56, 9217 –9221】 4、氮杂- Wacker氧化反应
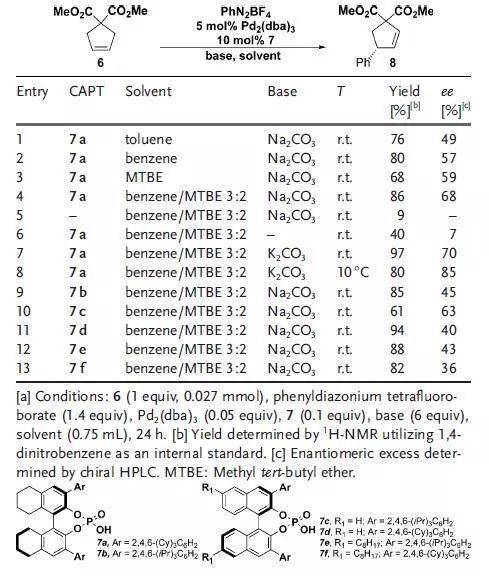
【 Angew. Chem. Int. Ed. 2018, 57, 1995 –1999】 5、 Heck反应
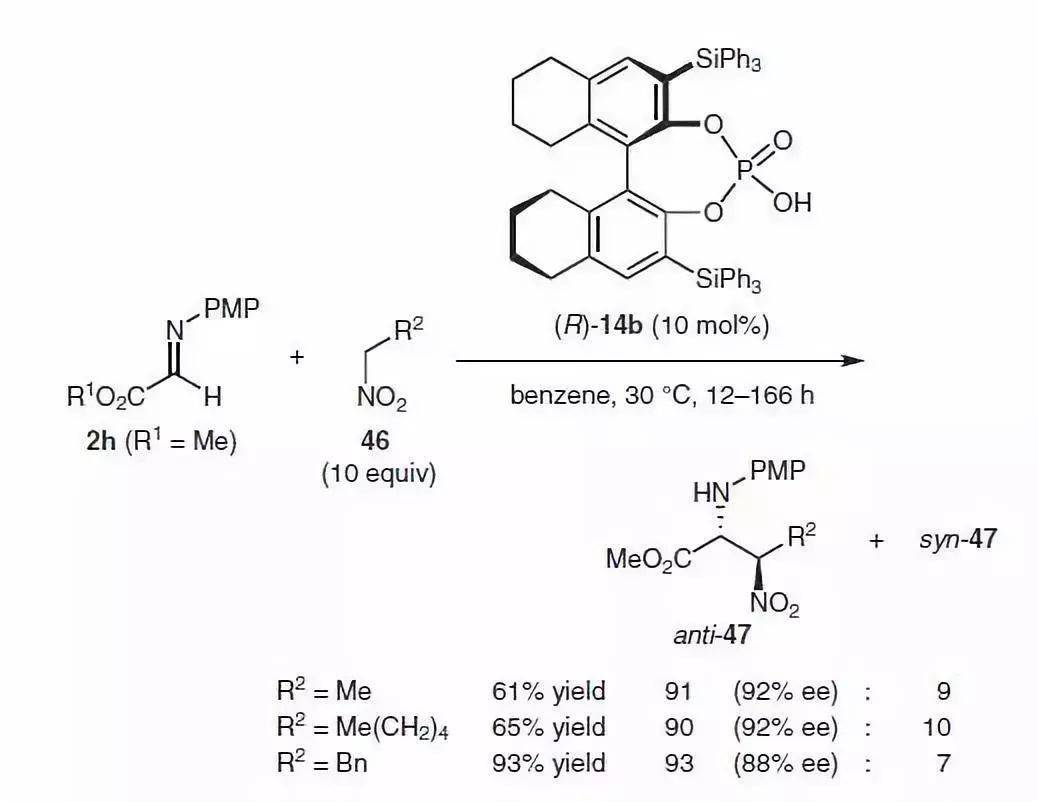
【 Angew. Chem. Int. Ed. 2017, 56, 5806 –5811】 6、 Aza-Henry反应
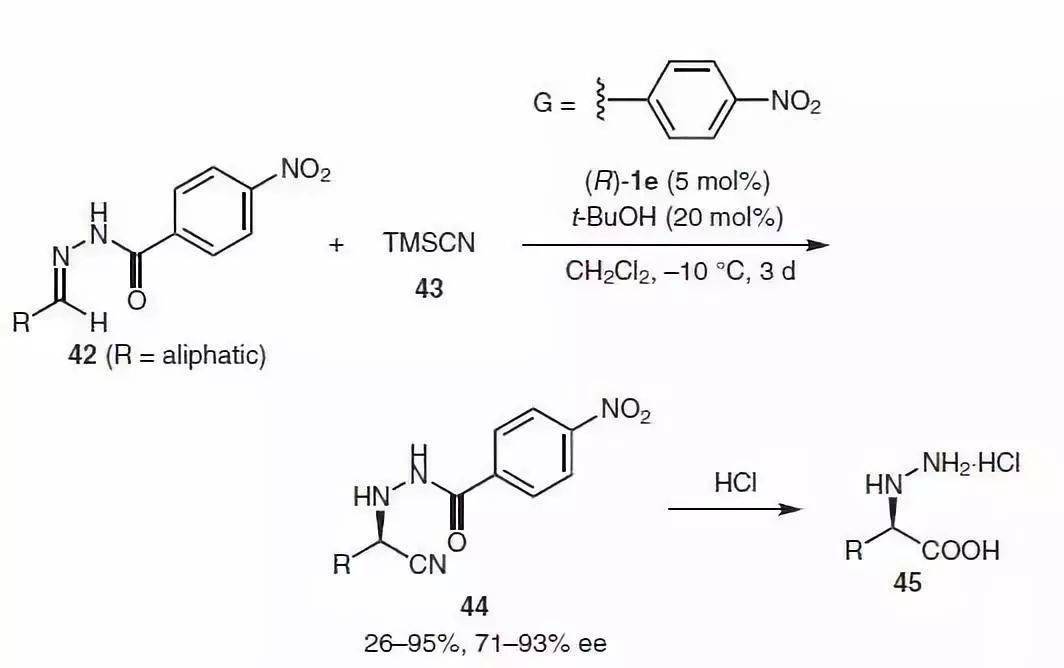
【 Org. Lett. 2008, 10, 1731】 7、 Strecker反应
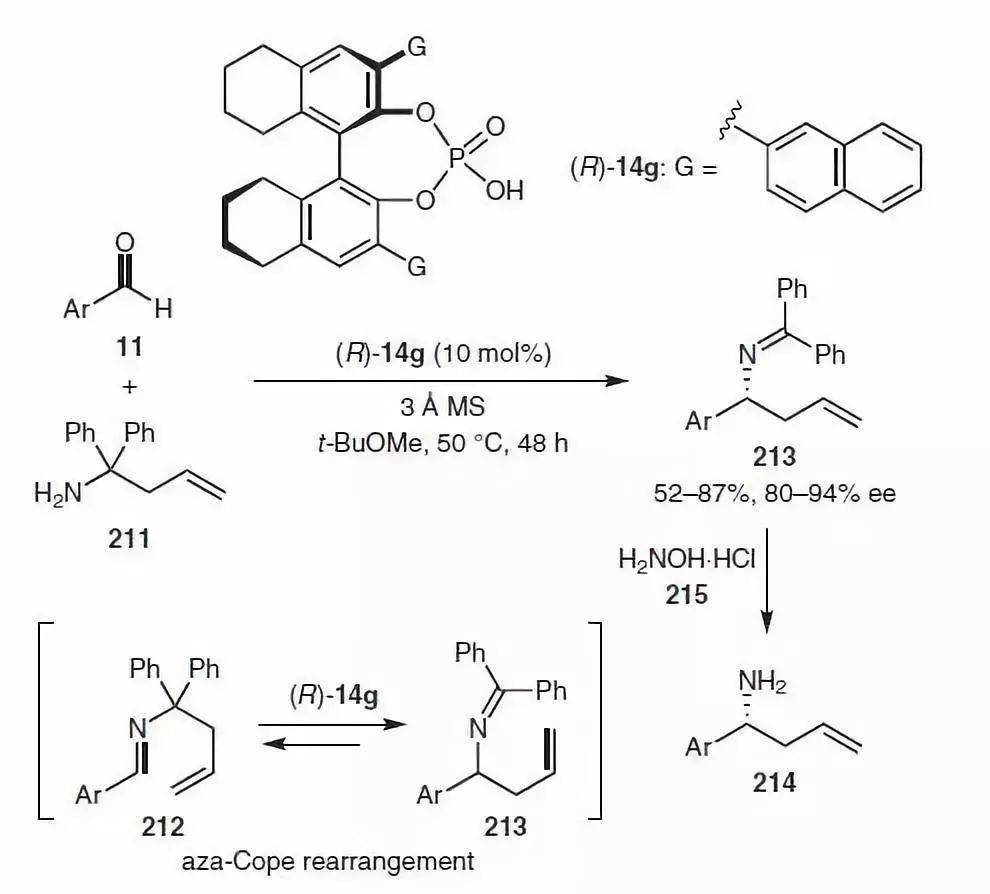
【 Org. Lett. 2010, 12, 188】 8、 aza-Cope重排反应(氮杂-Cope重排)
【 Synthesis 2010, 12, 1929–1982】 返回搜狐,查看更多 |
【本文地址】