| RNA | 您所在的位置:网站首页 › rna-seq结果分析 › RNA |
RNA
|
学习目标
了解设置重复对于
RNA-seq 分析的重要性
了解生物重复次数、测序深度和鉴定到的差异表达基因之间的关系
了解如何设计
RNA-seq 实验,以避免批次效应
1. 注意事项
了解 RNA 提取和 RNA-seq 文库制备实验过程中的步骤,有助于设计 RNA-seq 实验,但有一些特殊的注意事项需要明确: 重复次数和类型 避免混淆 处理批次效应 2. 重复实验重复可以通过技术重复或生物学重复来实现,如下图: 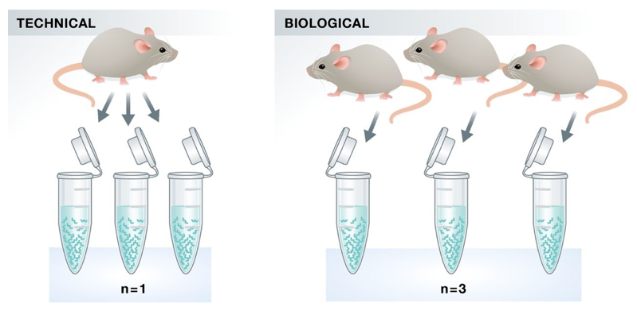 Klaus B., EMBO J (2015) 34: 2727-2730
技术重复
Klaus B., EMBO J (2015) 34: 2727-2730
技术重复
使用相同的生物样本重复实验步骤,以准确测量技术差异并在分析过程中将其去除。 生物学重复使用相同条件下的不同生物样本来衡量样本间的差异。 在微阵列时代,技术重复被认为是必要的;然而,当前的 RNA-seq 技术,技术差异远低于生物差异,因此不需要技术重复。相反,生物重复对于差异表达分析是绝对必要的。 对于差异表达分析,生物学重复越多,对生物学变异的估计就越好,我们对平均表达水平的估计也就越精确。因此,数据可以进行更准确的建模并识别更多差异表达的基因。 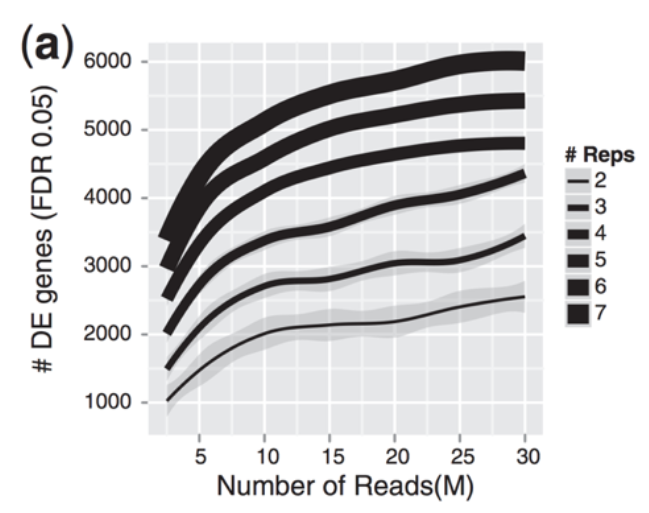 Liu, Y., et al., Bioinformatics (2014) 30(3): 301–304
Liu, Y., et al., Bioinformatics (2014) 30(3): 301–304
如上图所示,生物重复比测序深度更重要,测序深度是每个样本测序的读数总数。该图显示了测序深度和重复次数对鉴定出的差异表达基因数的关系。与增加测序深度相比,重复次数的增加往往会得到更多的差异表达基因。因此,通常更多的重复比更高的测序深度更好,但需要注意的是,检测低表达的差异表达基因和执行异构体水平(可变剪切)的差异表达分析需要更高的深度。 下面列出了一些关于重复和测序深度的建议,用于实验规划: 通用建议: ENCODE 建议每个样本有 3000 万个 SE reads。 如果有大量的重复 (>3),每个样本 1500 万次 reads 通常就足够了。 如果可能,进行更多的生物重复。 通常建议读取长度 >= 50 bp含有低表达基因: 同样,重复比测序深度更有作用。 深度更深,至少有 30-60 百万 reads ,具体取决于表达水平。异构体水平的差异表达: 新亚型的深度应该更大(每个样本 > 6000 万 reads)。 对 RNA 质量进行质控。其他类型的 RNA 分析(内含子保留、small RNA-Seq 等): 取绝于具体的分析 ★总之,尽量做生物学重复。 ” 3. ConfoundConfounding 是指:无法区分结果是由什么原因导致的。 例如,我们知道性别对基因表达有很大影响,如果我们所有的对照组小鼠都是雌性而所有处理组小鼠都是雄性,那么我们的治疗效果就会被性别混淆。我们无法区分是处理的作用和性别的作用。 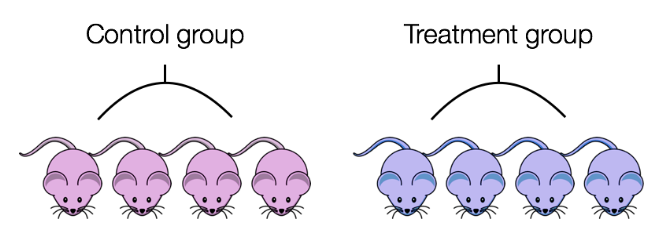 如何避免:
如果可能,确保每种情况下的动物都是相同的性别、年龄和批次。
如果不可能,则确保在不同条件下平均分配动物。
如何避免:
如果可能,确保每种情况下的动物都是相同的性别、年龄和批次。
如果不可能,则确保在不同条件下平均分配动物。
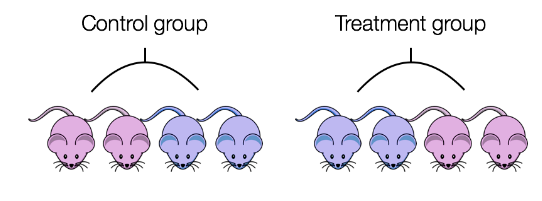 deconfound
4. 批次效应
deconfound
4. 批次效应
批次效应是 RNA-seq 分析的一个重要问题,仅由批次效应就能导致显著的表达差异。 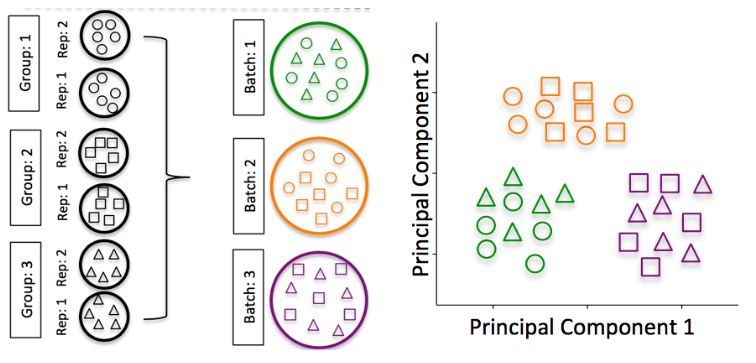 Hicks SC, et al., bioRxiv (2015)
如何确定是否有批次效应
是否所有的
RNA 提取都是在同一天进行的?
是否所有的文库构建都是在同一天进行的?
是否同一个人对所有样品进行了
RNA 提取与文库制备?
是否对所有样品使用了相同的试剂?
是否在同一地点进行
RNA 提取与文库制备?
Hicks SC, et al., bioRxiv (2015)
如何确定是否有批次效应
是否所有的
RNA 提取都是在同一天进行的?
是否所有的文库构建都是在同一天进行的?
是否同一个人对所有样品进行了
RNA 提取与文库制备?
是否对所有样品使用了相同的试剂?
是否在同一地点进行
RNA 提取与文库制备?
如果任何一个答案是“否”,那么就存在批次效应。 5. 建议 如果可能,以避免分批的方式设计实验。 如果无法避免分批: 不要按批次混淆实验: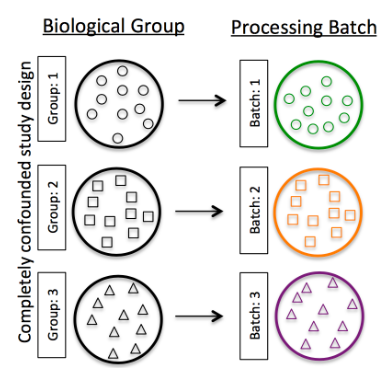 Hicks SC, et al., bioRxiv (2015)
跨批次拆分不同样本组的重复。重复次数越多越好(超过 2 个)。
Hicks SC, et al., bioRxiv (2015)
跨批次拆分不同样本组的重复。重复次数越多越好(超过 2 个)。
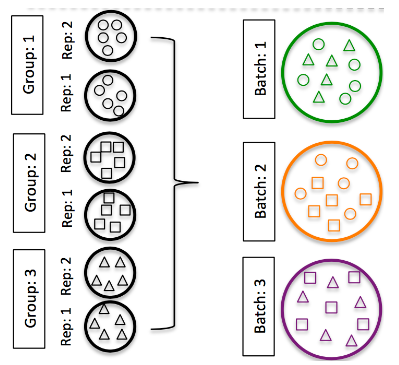 Hicks SC, et al., bioRxiv (2015)
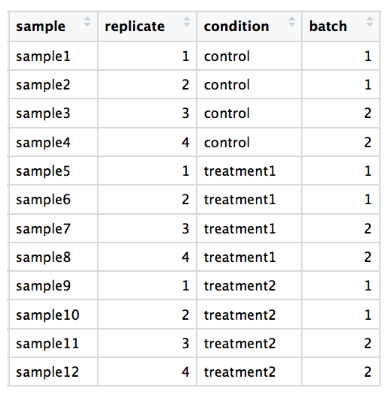
请务必在实验数据中包含批次信息。在分析过程中,如果没有混淆,可以回归出由于批次引起的变异,所以有这些信息,它不会影响结果。
Hicks SC, et al., bioRxiv (2015)
请务必在实验数据中包含批次信息。在分析过程中,如果没有混淆,可以回归出由于批次引起的变异,所以有这些信息,它不会影响结果。
欢迎Star -> Github 学习目录( 学习目录( |
【本文地址】