| 【王老师带你玩转FlowJo®】之脱胎换骨的细胞增殖分析 | 您所在的位置:网站首页 › proliferation词根 › 【王老师带你玩转FlowJo®】之脱胎换骨的细胞增殖分析 |
【王老师带你玩转FlowJo®】之脱胎换骨的细胞增殖分析
|
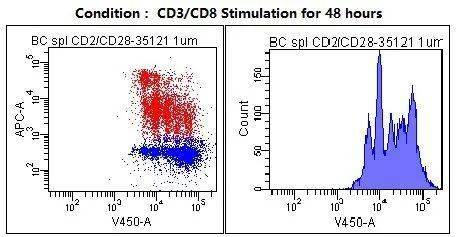
1.2 VPD 450检测: BD生物科学的BD Horizon™ VPD 450是一种非荧光的酯化染料,同样可以被吸收进入细胞。染料一旦进入细胞内部,酯酶会切割酯基,将染料变成细胞内的荧光产品。随着细胞的复制,细胞内的染料数量逐渐减少,形成了特征的图案。由此,我们可以采用多色流式技术从有限的样品量中获得更多的数据。
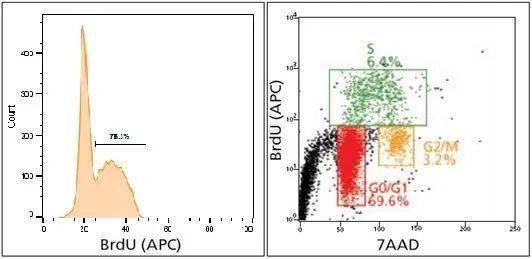
1.3 BrdU检测: Brdu是5-溴脱氧尿嘧啶核苷,BrdU可代替胸腺嘧啶渗入DNA的合成,BrdU荧光抗体检测渗入量,反映细胞增殖情况。此外Brdu可以在分析细胞周期时让S期更为精准。
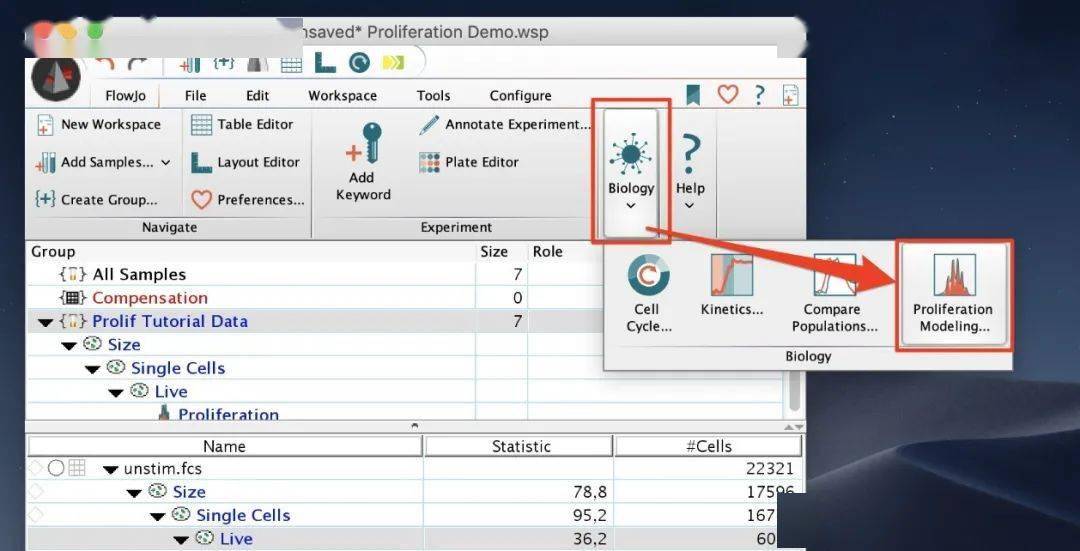
(点击图片可放大查看) //2.FlowJo®细胞增殖分析平台 // / BD FlowJo® 通过以上实验获得相关数据后,分析时手动标记操作繁琐并且不精准。这时就可以用到FlowJo V10的增值分析工具(Proliferation Tool)。
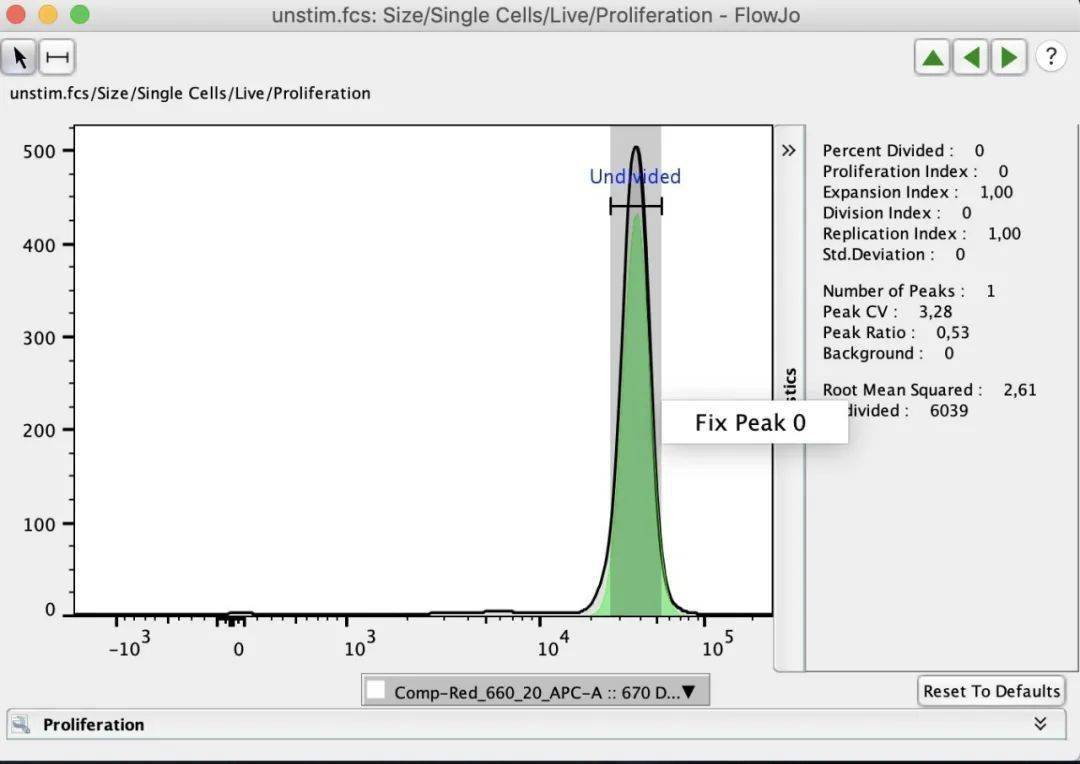
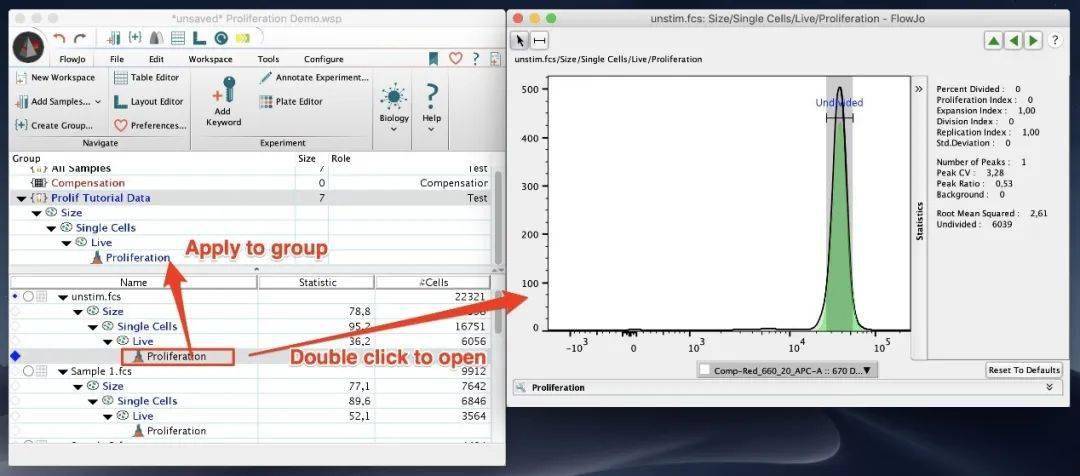
2.1 确定“第0代”峰 增殖实验通常将使用未刺激的样品开始分析,以确定“第0代”峰。第0代高峰代表未分裂的细胞,在增殖实验中收集的样本中应该有相对一致的强度和CV。在增殖实验中,在未受刺激峰周围画一个线性门门来设置“0代”峰。
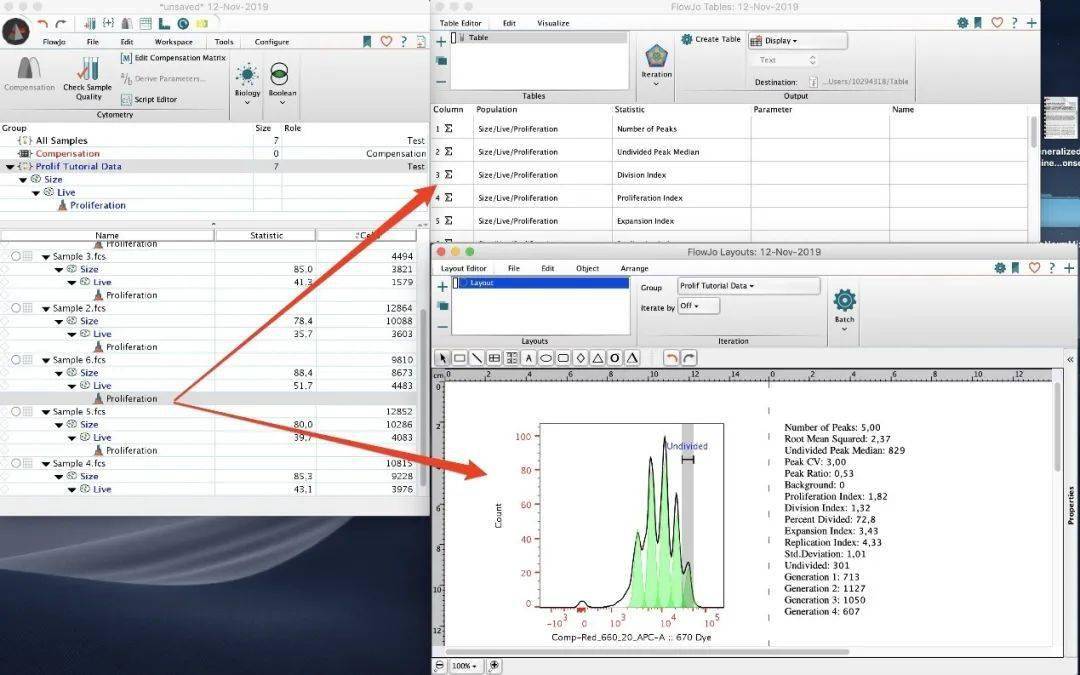
2.2 策略应用到相关样本 上一步操作完成后会在workspace中形成一个增殖分析node。双击node可以打开增殖分析窗口。拖动node可以将分析策略应用到相关样本。
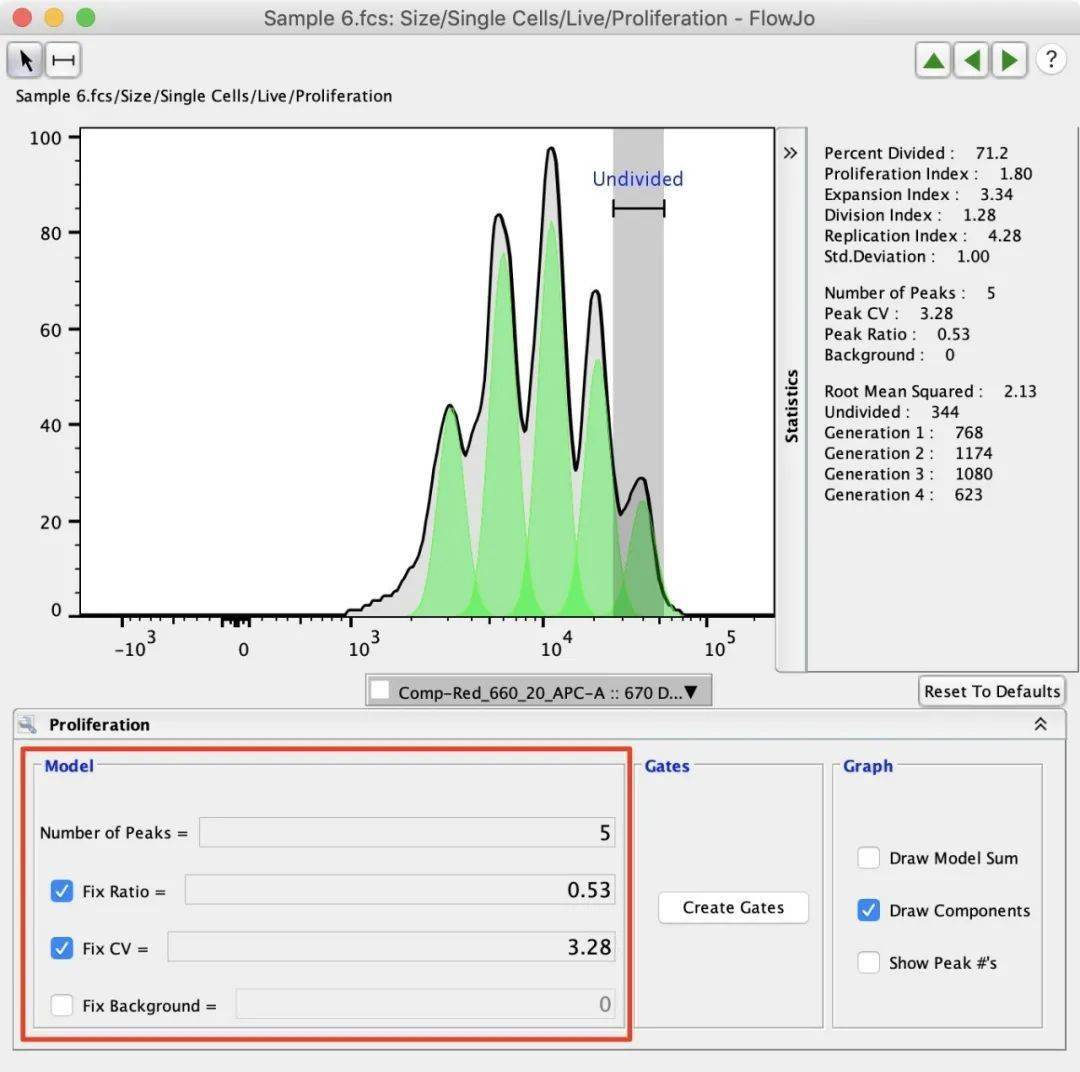
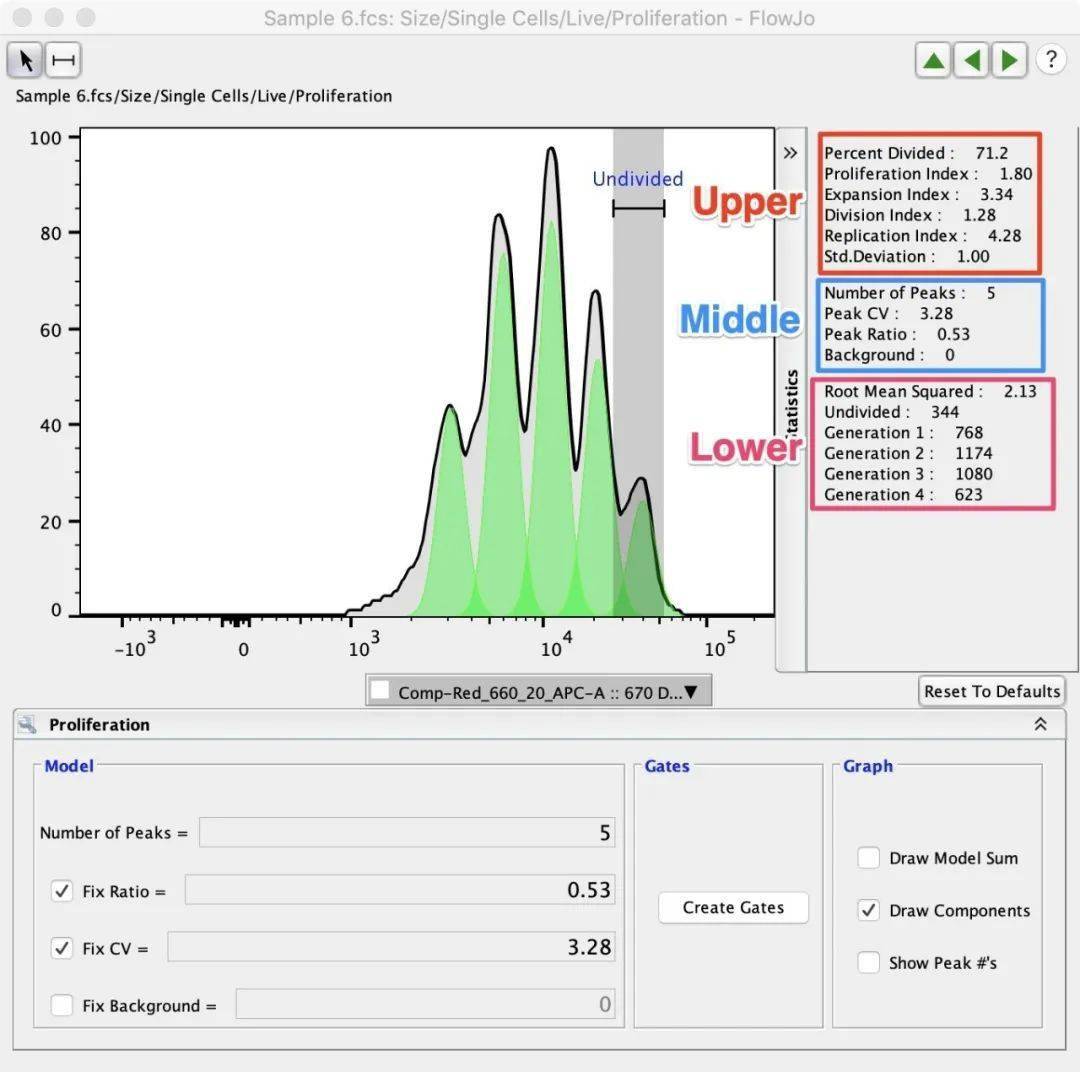
2.3 数据自动分析和手动微调 FlowJo®首先会拟合出代表该群体的最优峰比和CV。这些可以手动调整和修复,以便它们在扩散分析中保持一致。还需要调整峰值的数量,以表示分析中出现的峰值的数量。通常,FlowJo®将设置一个接近预期0.5%的峰值比率。预计细胞每分裂一次,两个子代细胞中的每一个都会有一半的染色量,因此它们的信号强度也会减半。
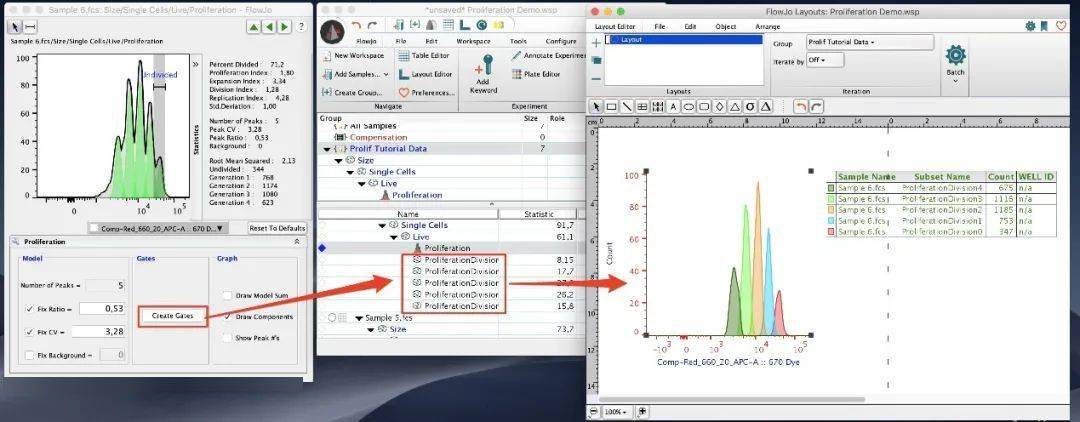
2.4 自动生成每个增殖峰的细胞门 “Create Gates”按钮可以用来快速地在代表每个增殖峰的细胞群上创建门。
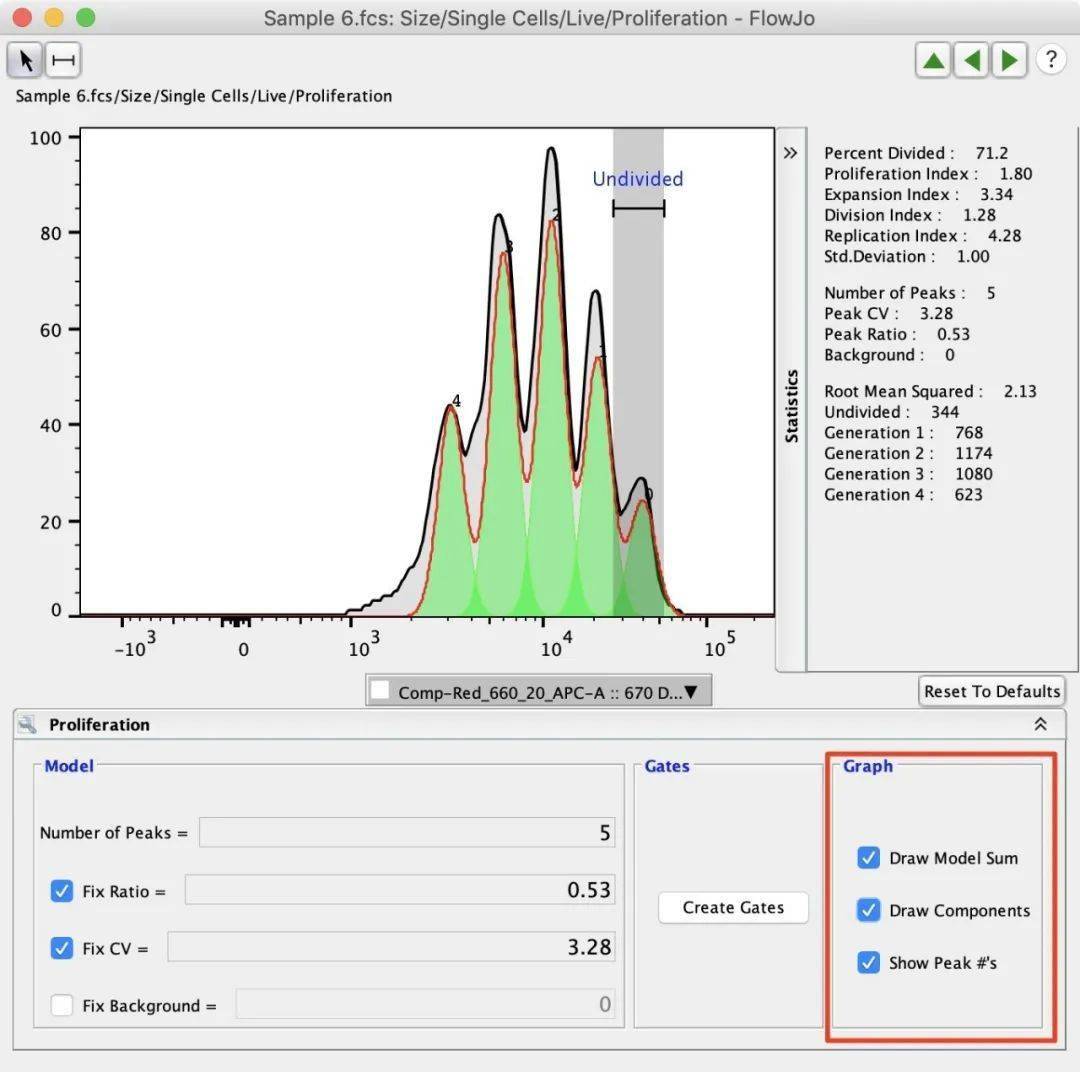
2.5 图像选项优化结果图 图形选项通过添加峰值数或Draw Model Sum来影响增殖显示,Draw Model Sum将增殖峰值的重叠相加,创建一个类似于原始数据的形状。
2.6 增殖统计数据获得 与增殖分析相关的统计信息显示在增殖窗口的右侧。下面将对它们进行更详细的解释。上面一组统计数据显示了增殖分析中常用的分析值。中间一组统计信息显示用户设置的统计值。底部的统计数据包括均方根(RMS)和与每个峰值相关的细胞计数,因为它代表了扩散模型与原始数据之间的差异。
2.7 数据结果导出 可以将增殖node拖放到layout editor窗口中,以创建增殖结果图及其相关的统计信息。还可以将增殖节点拖放到table editor中,以生成增殖平台中使用的统计数据表。
2.8 增殖数据定义 Division Index:分裂指数是指原始细胞群中细胞分裂的平均次数。即使对于从未分裂的细胞也是平均水平。(例如:包括未分裂的细胞峰)。 Proliferation Index:增殖指数是细胞分裂的总数除以进入分裂的细胞数。增殖指数只考虑了至少经历过一次分裂的细胞,也就是说,只有增殖的细胞才反映在增殖指数中。这是一个很有用的进行样本间比较的值,因为它只考虑增殖的细胞。 增殖指数更真实地反映了样本中增殖细胞的生物学特性;分裂指数反映了整个样本等状况。 Peak CV:增殖峰CV是峰的变异系数。所有峰值的CV值都相同。通常情况下,这个数字是4-7%。 Peak ratio:增殖峰比率是后续峰之间的荧光比率。例如:0.5表示n峰的荧光量是n - 1峰的一半。比值> 0.5是没有生物学意义的,通常出现在log amp不是很好。所以该值应该接近0.5。 2.9 增殖数据案例分析 举例:作为增殖指数和分裂指数如何计算的例子,如下: G0 = 15888 G1 = 32922 G2 = 1364 G3 = 897 *培养开始时的细胞数:15888 + (32922/2)+ (13647/4)+ (897/8)= 35872.875 *分裂细胞总数:(32922/2)*1 + (13647/4)*2 + (897/8)*3 = 23620.875 *进入分裂的细胞数:35872.875 - 15888 = 19984.875 *分裂指数:23620.875 / 35872.875 = 0.66 *增殖指数:23620.875 / 19984.875 = 1.18 如果模型对数据拟合不理想,可以通过调整模型参数得到较好的拟合模型。 与FlowJo®中的所有其他平台一样,增殖node可以通过拖动应用于一组样本。每一代都可以双击node打开图表单独分析。 2.10 增殖文献分享 - Interpretation of Cellular Proliferation Data: Avoid the Panglossian. Mario Roederer, Cytometry Part A, 79A: 95 101, 2011 - Assessing Antigen-Specific Proliferation and Cytokine Responses Using Flow Cytometry. Allsopp and Langhorne, Edited by Denise Doolan, Malaria Methods and Protocol, p. 409 - Antigen/Mitogen-Stimulated Lymphocyte Proliferation. Whiteside, Measuring Immunity, Chpt. 31 p. 364 - Use of Cell-Tracking Dyes to Determine Proliferation Precursor Frequencies of Antigen-Specific T Cells. Givan, Fisher, Waugh, Bercovici, Wallace. Flow Cytometry Protocols 2nd Ed. p.109 - Proliferation Assays Based on BrdU Incorporation or CFSE Labeling. Maecker, Immunotherapy of Cancer, Disis, p.62 - Monitoring T Cell Proliferation. Hodgkin, Hawkins, Hasbold, Gett, Deenick, Todd, Hommel. Analyzing T Cell Responses By Dirk Nagorsen, Francesco M. Marincola, p. 122 (以上图片可点击放大查看) 以上就是王老师为大家带来的FlowJo®增殖分析平台全面的全面解析,希望能够给每一位流式工作者带来帮助。最新升级版FlowJo®增殖分析平台平台尽在V 10.7版本,快来下载体验吧!
最后我还要提醒老师们的是,目前正版FlowJo®还可以申请30天免费试用版本,我们也为大家准备了新手速成培训课程;对于已购买的老师们,我们更是准备了详细的视频培训讲解,大家赶快用起来吧! 更多精彩|关注我们
版权声明和使用限制 本微信公众号归属BD,使用本账号或从本账号下载内容都表明您同意遵守以下声明:本账号包含的所有内容,包括但不限于内容的选择、结构或设计均由BD或其许可方所有,且受著作权法等其他知识产权法和反不正当竞争法的保护。未经BD事先书面同意,不得以任何方式修改、复印、复制、上传、发布、传输或散布本网站的全部或部分内容,包括任何代码和软件。您仅能出于个人目的从本网站下载内容,除非您同时满足以下条件才能以商业目的下载并使用本网站的内容:(1)未对该等内容作任何修改;(2)保留所有的版权和其他所有权声明;(3)已经获得BD事先书面同意;(4)并且当您展示或以其他方式使用该内容时,必须标注“经BD同意使用”。对本声明的任何违反均构成违法及不公平的商业行为,BD保留依照相关法律及规定向侵权者追究法律责任的权利。返回搜狐,查看更多 |
【本文地址】