| 硫化氢 | 您所在的位置:网站首页 › h2s的立体结构 › 硫化氢 |
硫化氢
|
编号系统
CAS号:7783-06-4 MDL号:MFCD00011444 EINECS号:231-977-3 RTECS号:MX1225000 BRN号:3535004 PubChem号:24888266 物性数据
1.性状:无色、有恶臭味的气体[1] 2.pH值:4.5(1%水溶液)[2] 3.熔点(℃):-85.5[3] 4.沸点(℃):-60.3[4] 5.相对密度(水=1):1.54[5] 6.相对蒸气密度(空气=1):1.19[6] 7.饱和蒸气压(kPa):2026.5(25.5℃)[7] 8.临界温度(℃):100.4[8] 9.临界压力(MPa):9.01[9] 10.辛醇/水分配系数:0.23[10] 11.闪点(℃):-106[11] 12.引燃温度(℃):260[12] 13.爆炸上限(%):46.0[13] 14.爆炸下限(%):4.0[14] 15.溶解性:溶于水、乙醇、二硫化碳、甘油、汽油、煤油等。[15] 毒理学数据
1、小鼠、大鼠吸入LC50:634×10-6/1h、712×10-6/1h;大鼠吸入LC50:444×10-6/4h。 硫化氢主要经呼吸道吸收,人吸入(70~150mg/m3)/(1~2h),出现呼吸道及眼刺激症状, 硫化氢可以麻痹嗅觉神经,吸2~5min后不再闻到臭气。吸入(300mg/m3)/1h,6~8min出现眼急性刺激症状,稍长时间接触引起肺水肿。吸入硫化氢能引起中枢神经系统的抑制,有时由于刺激作用和呼吸的麻痹而导致最终死亡。 在高浓硫化氢中几秒内就会发生虚脱、休克,能导致呼吸道发炎、肺水肿,并伴有头痛、胸部痛及呼吸困难。硫化氢贮存区附近不应有氧化可燃材料、酸或其他腐蚀性材料。避免暴露于高温环境。 2.急性毒性[16] LC50:618mg/m3(444ppm)(大鼠吸入) 3.刺激性 暂无资料 4.亚急性与慢性毒性[17] 家兔吸入0.01mg/L,每天2h,3个月,引起中枢神经系统的机能改变,气管、支气管黏膜刺激症状,大脑皮层出现病理改变。小鼠长期接触低浓度硫化氢,有小气道损害。 5.其他[18] LCLo:600ppm(人吸入30min) 生态学数据
1.生态毒性[19] TLm:0.0071~0.55mg/L(96h)(黑头呆鱼);0.0448~0.0478mg/L(96h)(蓝鳃太阳鱼) 2.生物降解性 暂无资料 3.非生物降解性 暂无资料 4.其他有害作用[20] 该物质对环境有危害,应注意对空气和水体的污染。 分子结构数据
1、摩尔折射率:无可用的 2、摩尔体积(cm3/mol):无可用的 3、等张比容(90.2K):无可用的 4、表面张力(dyne/cm):无可用的 5、介电常数:无可用的 6、极化率(10-24cm3):无可用的 7、单一同位素质量:33.98772 Da 8、标称质量:34 Da 9、平均质量:34.0809 Da 计算化学数据
1、疏水参数计算参考值(XlogP):0.5 2、氢键供体数量:1 3、氢键受体数量:1 4、可旋转化学键数量:0 5、互变异构体数量:无 6、拓扑分子极性表面积(TPSA):1 7、重原子数量:1 8、表面电荷:0 9、复杂度:0 10、同位素原子数量:0 11、确定原子立构中心数量:0 12、不确定原子立构中心数量:0 13、确定化学键立构中心数量:0 14、不确定化学键立构中心数量:0 15、共价键单元数量:1 性质与稳定性
1.在有机胺中溶解度极大。在苛性碱溶液中也有较大的溶解度。在过量氧气中燃烧生成二氧化硫和水,当氧气供应不足时生成水与游离硫。室温下稳定。可溶于水,水溶液具有弱酸性,与空气接触会因氧化析出硫而慢慢变浑。能在空气中燃烧产生蓝色的火焰并生成SO2和H2O,在空气不足时则生成S和H2O。有剧毒,即使稀的硫化氢也对呼吸道和眼睛有刺激作用,并引起头痛,浓度达1mg/L或更高时,对生命有危险,所以制备和使用H2S都应在通风橱中进行。 2.稳定性[21] 稳定 3.禁配物[22] 强氧化剂、碱类 4.聚合危害[23] 不聚合 贮存方法
储存注意事项[24] 储存于阴凉、通风的易燃气体专用库房。远离火种、热源、库温不宜超过30℃。保持容器密封。应与氧化剂、碱类分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备。 合成方法
1.将20%~30%磷酸慢慢地从分液漏斗滴到Na2S?9RO浓水溶液中,将所产生的气体经无水氯化钙与五氧化二磷干燥,制得硫化氢气体,经液化压入钢瓶。 2.用硫黄和氢直接合成制得硫化氢纯度高
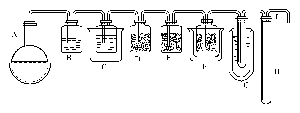
图XVI-3 制备硫化氢的装置 纯氢减压后进入干燥器进一步纯化,然后经计量进入反应器底部与硫黄直接接触反应,生成硫化氢,硫化氢经洗涤器洗涤,再进入硫蒸气冷凝器将其中剩余的硫蒸气冷凝下来。纯净的硫化氢气体经压机压缩后进入硫化氢冷凝器,液体硫化氢收集在贮罐中。 用硫化钙与氯化镁反应制备液态硫化氢的反应装置如图所示,全部操作应在通风橱中进行。 图制备硫化氢的装置 A 为置于水浴中的烧瓶;B,C,D,E,F 为250mL玻璃瓶,分别装有水、饱和Ba(OH)2 (外面用冰盐冷浴)、氯化钙、五氧化二磷、玻璃棉(外面以干冰冷却); G为50mL试管,杜瓦瓶中为干冰乙醚冷冻剂;H为汞封;I 为出口 在发生瓶A中装入500mL饱和氯化镁溶液,并加入10g固体氯化镁和50g优质硫化钙。当混合物加热到60℃时,即可平稳和连续地产生硫化氢气体。C瓶中的氢氧化钡吸收最初产生的硫化氢,转变为硫氢化钡后,硫化氢即可通过,而其他挥发性酸性杂质则被吸收。系统中空气未排尽前可使气体不通过汞封H,以加快排空气的过程。反应一段时间后在试管G中即有液态硫化氢凝聚。 3.硫化铝水解法:在烧瓶中放入适量硫化铝固体,从滴液漏斗中慢慢滴入水,即可顺利地产生十分纯的硫化氢气体。 用途
1.用于合成荧光粉,电放光、光导体、光电曝光计等的制造。有机合成还原剂。用于金属精制、农药、医药、催化剂再生。通用试剂。制取各种硫化物。 2.用于制造无机硫化物,还用于化学分析如鉴定金属离子。[25] 安全信息危险运输编码:UN 1053 2.3 危险品标志: 安全标识:S9 S16 S36 S38 S45 S61 危险标识:R12 R16 R50 文献[1~25]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8 备注暂无 表征图谱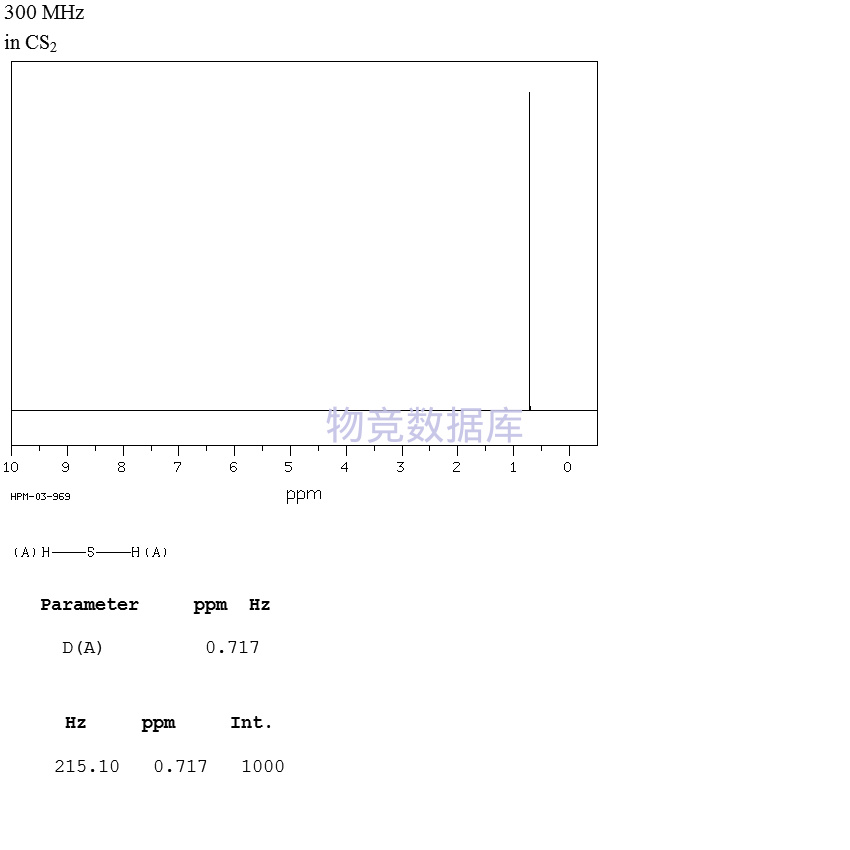
核磁碳1 (1/1) |
【本文地址】
 易燃
易燃  极毒
极毒  危害环境
危害环境