| 基于真实世界与靶点网络聚类的茵栀黄颗粒治疗黄疸的联合用药方案及分子机制分析 | 您所在的位置:网站首页 › atc药品编码电子版 › 基于真实世界与靶点网络聚类的茵栀黄颗粒治疗黄疸的联合用药方案及分子机制分析 |
基于真实世界与靶点网络聚类的茵栀黄颗粒治疗黄疸的联合用药方案及分子机制分析
|
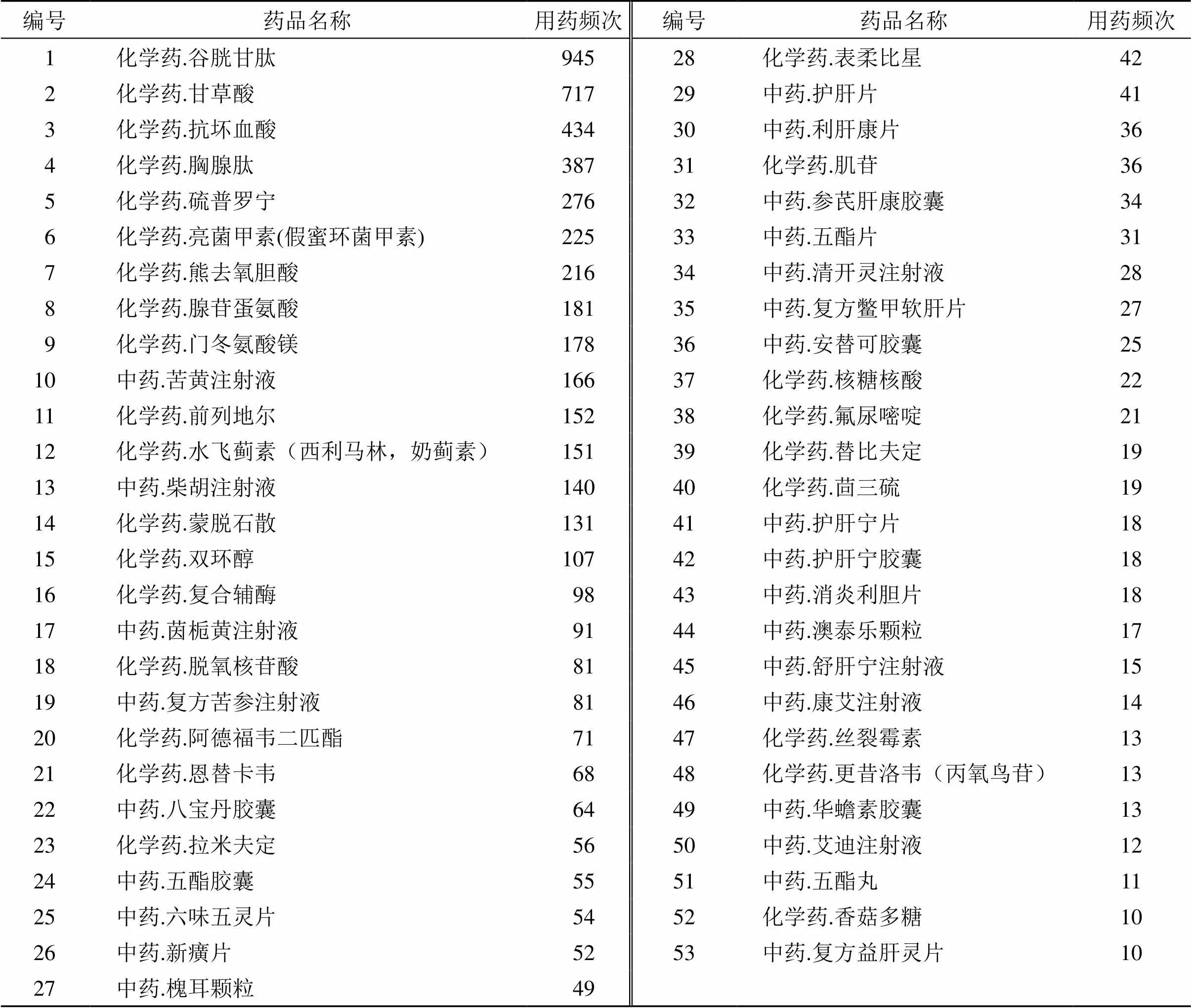
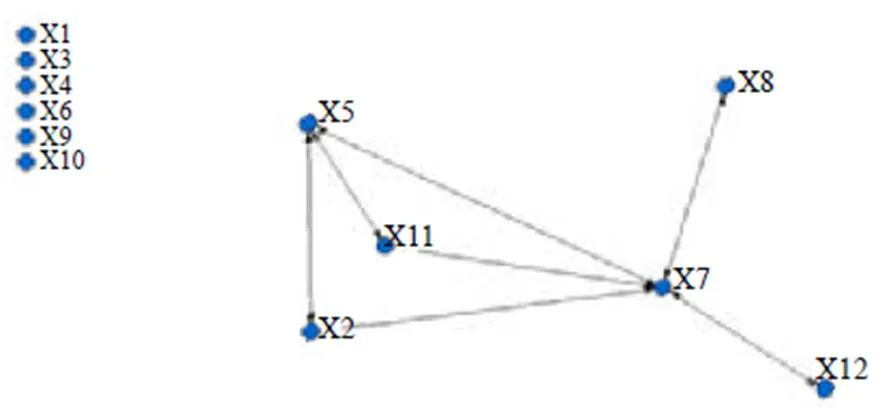
崔 鑫,张 成,席俊羽,谢瑀婷,刘 毅*,谢雁鸣* 基于真实世界与靶点网络聚类的茵栀黄颗粒治疗黄疸的联合用药方案及分子机制分析 崔 鑫1,张 成1,席俊羽1,谢瑀婷2,刘 毅1*,谢雁鸣1* 1. 中国中医科学院中医临床基础医学研究所,北京 100700 2. 中国人民大学统计学院,北京 100872 挖掘茵栀黄颗粒治疗黄疸的核心联用药物方案的临床应用规律,为探索临床不同诊疗思路、用药经验和提高中医药临床证据的循证等级提供参考。基于全国39家医院信息管理系统(hospital information system,HIS)黄疸患者的用药数据,运用Tabu搜索算法,对真实世界茵栀黄颗粒治疗黄疸的联合用药情况进行回顾性分析。同时,采用靶点网络分析核心联合用药方案的分子网络机制,并通过分子对接技术对其作用机制进行验证。根据Tabu搜索算法聚类分析的结果,结合肝病相关指南和文献,识别出3种茵栀黄颗粒治疗黄疸的核心联用药物方案:(1)针对药物性肝损伤导致的黄疸,可以联用谷胱甘肽;(2)针对胆汁淤积导致的黄疸,可以联用亮菌甲素;(3)针对病毒性肝炎导致的黄疸,可以联用双环醇。3种方案的分子网络机制均具有多成分、多靶点、多通路的特点,茵栀黄联用谷胱甘肽治疗黄疸的分子网络机制主要与机体的炎症免疫、Toll样受体信号通路传导、谷胱甘肽代谢通路和细胞死亡负调控的生物过程有关;茵栀黄联用亮菌甲素治疗黄疸的分子网络机制主要与动脉粥样硬化、胆汁分泌等关键通路有关;茵栀黄联用双环醇治疗黄疸的分子网络机制主要与上皮细胞信号转导通路和癌症相关的信号通路有关。数据挖掘得出的茵栀黄颗粒核心联合用药方案,基本符合相关指南及诊疗规范,并对其作用机制进行了探索,为优化临床联合用药、合理用药提供了一定的指导和参考。建议临床实际应用过程中,根据黄疸的疾病进展情况,合理评估临床联合用药方案的疗效及安全性,注意用药配伍禁忌。 茵栀黄颗粒;黄疸;真实世界研究;联合用药;谷胱甘肽;亮菌甲素;双环醇;黄芩苷;栀子苷;羟基乙酮;绿原酸 黄疸是由于人体内胆红素过量聚积所致,临床以巩膜、黏膜、皮肤黄染为主要表现[1]。黄疸多见于新生儿患者,严重的新生儿黄疸发病率和死亡率均较高[2],印度新生儿黄疸的死亡率高达30.8%[3]。严重的新生儿黄疸是导致患儿长期神经认知功能障碍、脑瘫、耳聋、学习困难等后遗症的主要原因,给全球带来了沉重的健康和经济负担[4]。黄疸可由肝炎、肝硬化、肝癌、溶血性贫血等多种肝脏疾病引起[5]。目前成人黄疸的治疗尚无广泛认可的临床指南,一般以保肝降酶退黄为基本治则,同时针对不同病因进行对症治疗[6]。对于新生儿黄疸的治疗,英国国家卫生与临床优化研究所于2014年6月发布了相关临床指南,明确指出蓝光照射是治疗新生儿黄疸的安全有效疗法;同时该指南还提出,在中国传统医学中推荐使用中药茵陈治疗新生儿黄疸[7]。 茵栀黄颗粒来源于《伤寒论》的茵陈蒿汤,是中医药治疗黄疸的代表性方剂,由茵陈、栀子、黄芩、金银花四味中药的提取物组成,具有利湿退黄、清热解毒的功效[8]。临床上主要用于治疗黄疸和急、慢性肝炎[9]。研究表明茵栀黄颗粒能够降低血清胆红素水平[10],并保护肝细胞,且目前未见不良事件/ 反应报道[11],临床有效性、安全性较好。尽管茵栀黄颗粒在治疗黄疸方面有着独特的优势,但其优效的临床联合用药方案尚不明确。本研究运用Tabu搜索算法对茵栀黄颗粒治疗黄疸的优效联合用药方案进行数据挖掘,分析总结治疗黄疸的核心药物联合茵栀黄颗粒的临床应用规律。同时,本研究采用网络药理学的方法探索优效联合用药方案的分子网络机制,并通过分子对接对其作用机制进行初步验证。以期为探索临床不同诊疗思路、用药经验,提高中医药临床证据的循证等级提供参考。 1 资料与方法1.1 数据来源本研究临床联合用药数据由中国中医科学院中医临床基础医学研究所建立的多维数据仓库提供[12],共提取了全国39家医院信息管理系统(hospital information system,HIS)的1840例黄疸用药患者的数据信息。 联合用药方案的分子网络机制分析中的药物成分及其靶点来源于《中国药典》2020年版、TCMSP数据库、Drug Bank数据库、SEA和Swiss Target Prediction平台;黄疸相关的疾病靶点来源于OMIM数据库和GeneCards数据库。蛋白质相互作用(protein protein interaction,PPI)网络数据来源STRING数据库。富集分析的生物过程和关键通路来源于g:Profiler和Matescape平台。分子对接验证的三维分子结构来源于ZINC及PubChem数据库。 1.2 纳入和排除标准将符合以下标准的患者定义为茵栀黄颗粒治疗黄疸的有效人群:(1)符合《诊断学》第9版[13]中关于黄疸的诊断标准:患者血清总胆红素(total bilirubin,TBil)>17.1 μmol/L(1.0 mg/dL);(2)患者在住院期间使用了茵栀黄颗粒;(3)患者的治疗结局为治愈或好转。 以下药物不纳入分析:(1)各类溶媒,如葡萄糖、氯化钠等;(2)各类维生素(如有研究证据表明某种维生素对黄疸治疗有效,也可纳入分析);(3)未在茵栀黄颗粒用药期间联合使用的药物。 1.3 数据标准化由于各临床医院信息系统的设置及编码规则存在差异,因此本研究运用数据仓库技术(extract-transform-load,ETL)将多元异构数据进行整合,对提取的患者个人信息数据进行离散化处理,进而构建统一的标准化数据仓库[14]。 数据标准化根据统一制定的规则进行,疾病的中医诊断、证候根据《中华人民共和国国家标准·中医临床诊疗术语》来统一[15];疾病的西医诊断按照《内科学》第8版教材[16]和WHO制定的ICD-10编码标准[17]进行规范。化学药按照WHO制定的解剖-治疗-化学的药物分类系统(Anatomical Therapeutic Chemical,ATC)来统一编码标化[18],中药名称的标准化主要参考《国家基本药物目录》[19]、《国家医保目录》[20]和《中国药典》2020年版[21]。 1.4 筛选联合用药的复杂网络构建方法本研究选用Tabu搜索算法对标准化数据仓库构建的复杂信息网络进行结构关系的划分,将最终形成的指标群数提前设定,通过最终形成的指标群体的数集大小来判断指标群划分,因此能够真实反映各指标之间客观存在的网络结构关系[12]。通过Tabu搜索算法分析真实世界临床联合用药的多层次结构关系,进而探索挖掘黄疸临床优效干预方案的药物组成规律[22]。 1.5 分子网络机制分析及验证方法本研究首先从《中国药典》2020年版分别收集核心联合用药方案中药物的有效成分,并通过TCMSP数据库获得中药有效成分对应的靶点,通过Drug Bank数据库获得化学药对应的靶点;通过OMIM数据库和GeneCards数据库获得黄疸相关的靶点数据。然后,分别将核心联合用药方案干预黄疸的靶点映射至STRING数据库获得PPI网络,并导入Cytoscape软件进行拓扑属性分析。最后,通过g:Profiler平台和Matescape平台分析3种联合用药方案作用于黄疸的生物过程和关键信号通路。分子对接验证通过检索ZINC及PubChem数据库,分别获取核心联用药物方案的有效成分和其关键靶点的三维分子结构,利用软件对其两两进行分子对接验证,并将其中对接较好的组合进行可视化展示。 1.6 统计分析本研究应用SAS软件(版本9.4,SAS Institute Inc.,Cary,NC,USA)对纳入患者的一般特征进行描述性分析。通过UCINET6软件运行Tabu算法。运用Cytoscape软件(V3.7.2)进行分子网络机制分析;PPI分析物种设置为人,PPI网络置信度设置为0.4,度(degree)值设置为大于中位数,进行关键靶点筛选;基因本体论(gene ontology,GO)生物过程和京都基因和基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)信号通路富集分析按照≤0.01进行关键通路筛选。运用Autodock Vina软件进行分子对接验证,并使用Pymol进行可视化。 2 结果2.1 纳入人群和药物统计在数据集成仓库中,共提取出黄疸的用药人群1840例,其中治疗结局为好转或治愈人群共1557例。符合纳排标准的联用药物共90种,包含中药58种,化学药32种。 2.2 药物使用频次统计本研究筛选纳入了使用频次在10次及以上的药物,共计53种。药物使用频次见表1,可见化学药谷胱甘肽、甘草酸、抗坏血酸和中药苦黄注射液、柴胡注射液、茵栀黄注射液使用频次较高,是治疗黄疸的常用药物。 2.3 核心有效方案识别2.3.1 药物子群划分 经过测度分析,由53种中西药构成的复杂网络共划分为12个子群,具体划分结果见表2,其中方案组成中的药物编号对应药物使用频次统计表中的编号。 根据整体网络密度、子网络密度矩阵及关系矩阵,可以得出2、5、7、8、11、12的子群结构之间有较紧密的结构联系,其中子群5、7与其他群的连边数最多,表明它们与其他药物子群联系更为紧密,详见图1。 2.3.2 药物子网络构建 药物子群展开网络图见图2,其中药物1-化学药.谷胱甘肽、6-化学药.亮菌甲素、15-化学药.双环醇与其他药物的联系较为紧密,是治疗黄疸的核心药物。 通过进一步结合肝炎等与黄疸密切相关的疾病诊疗指南、现有文献报道[23-27],以及这3种药品的说明书,可以归纳得出茵栀黄颗粒治疗黄疸的核心联用优效方案:(1)针对药物性肝损伤导致的黄疸,可以联用谷胱甘肽;(2)针对胆汁淤积导致的黄疸,可以联用亮菌甲素;(3)针对病毒性肝炎导致的黄疸,可以联用双环醇。
表1 茵栀黄颗粒治疗黄疸联合药物使用频次
表2 中西药物子群
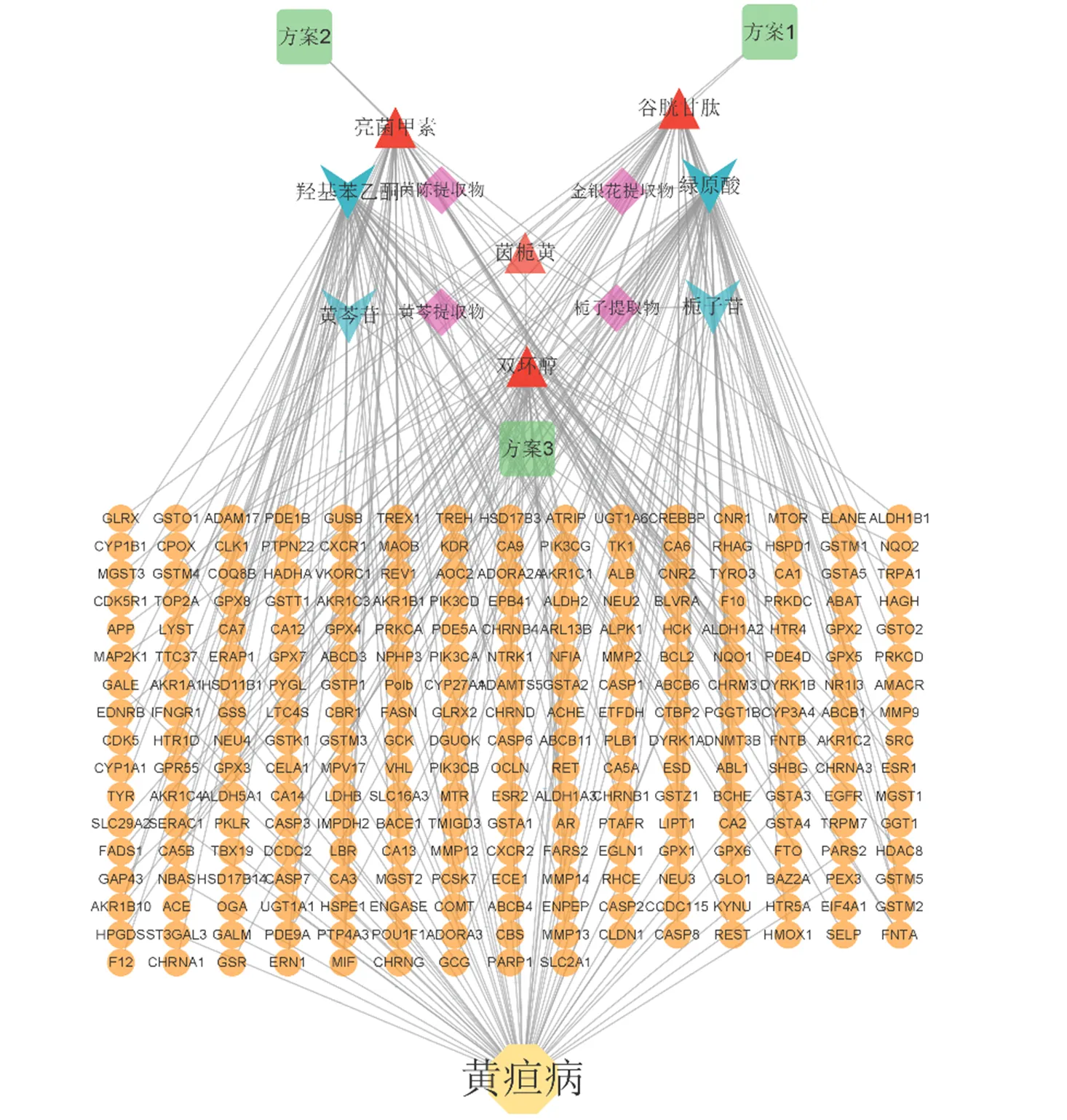
图1 药物子群划分网络图 2.4 分子网络机制分析2.4.1 药物靶点收集 通过《中国药典》2020年版获得了茵栀黄颗粒组方中茵陈提取物、栀子提取物、黄芩提取物、金银花提取物的有效成分,分别为羟基苯乙酮、栀子苷、黄芩苷、绿原酸,并通过TCMSP数据库查找这4种有效成分对应的靶点。
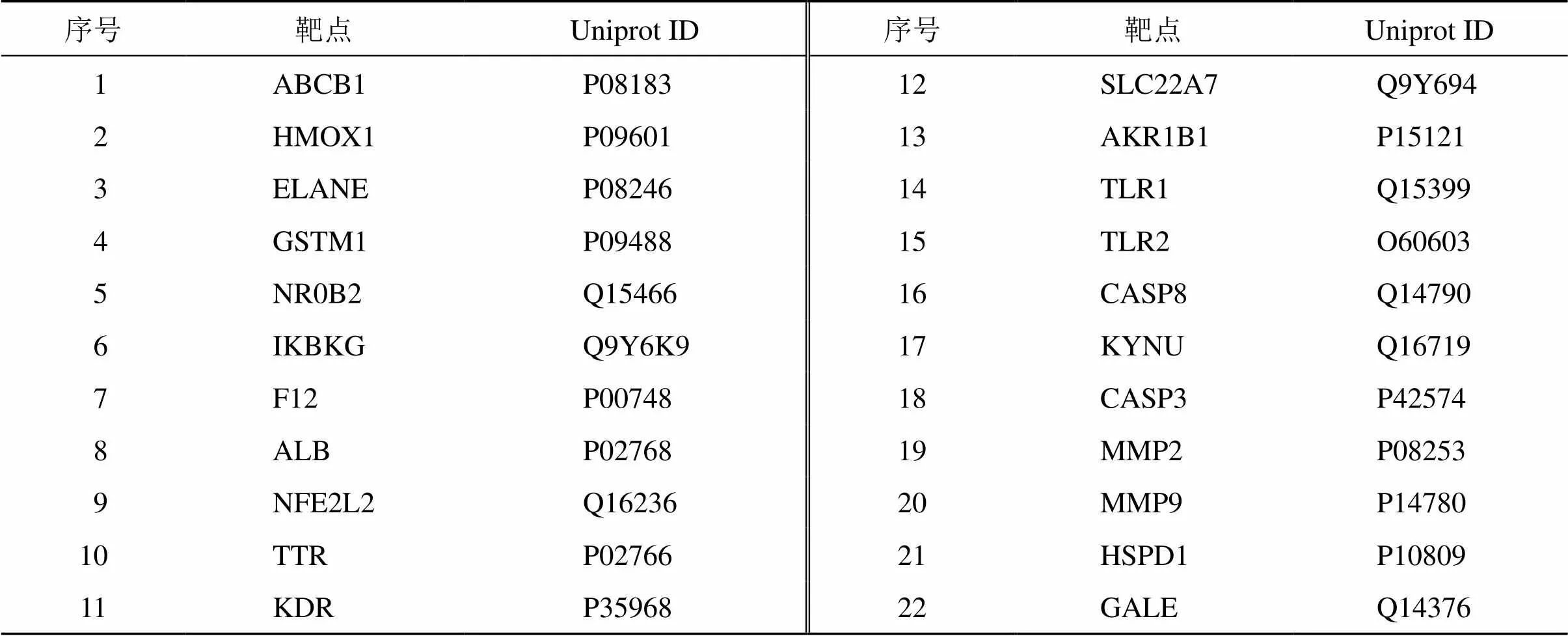
图2 药物子网络展开图 经查找共收集到栀子苷对应靶点8个,分别是碳酸酐酶II(carbonic anhydrase II,CA2)、B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)、血红素加氧酶1(heme oxygenase 1,HMOX1)、神经调节蛋白(neuromodulin,GAP43)、膜相关磷脂酶B1(membrane-associated phospholipase B1,PLB1)、胰高血糖素(glucagon,GCG)、谷胱甘肽S-转移酶Mu-1(glutathione S-transferase Mu 1,GSTM1)、谷胱甘肽S-转移酶Mu-2(glutathione S-transferase Mu 2,GSTM2);黄芩苷对应靶点2个,分别是凝血因子Xa(coagulation factor Xa,F10)和DNA拓扑异构酶II(DNA topoisomerase II,TOP2A)。 由于羟基苯乙酮和绿原酸在TCMSP中未查询到对应的靶点,因此本研究分别运用SEA和Swiss Target Prediction网页分析工具进行靶点预测,SEA平台预测结果以<0.05筛选具有统计学意义的靶点,Swiss Target Prediction平台预测结果以概率值(probability)大于0为标准,筛选可能成为目标药物成分靶点的结果,然后将2个平台的预测结果合并后去重,最终得到羟基苯乙酮对应靶点101个,绿原酸对应靶点64个。 在DrugBank数据库中分别检索后得到谷胱甘肽药物靶点41个,删除1个来源不确定是否为人类的靶点(glutathione peroxidase),最终获得40个靶点。由于亮菌甲素和双环醇在数据库中未检索到药物靶点,因此本研究分别运用SEA和Swiss Target Prediction平台进行预测,最终获得亮菌甲素药物靶点40个,双环醇药物靶点42个。以本研究中的用药方案、药物、成分、疾病、靶点为节点,其相互关系为边,构建“用药方案-药物-成分-疾病-靶点”图,见图3。 2.4.2 疾病相关靶点收集 在OMIM数据库检索得到黄疸相关靶点140个。GeneCards数据库初步检索得到黄疸相关靶点3400个,通过2次筛选相关性评分(relevance score)不小于中位数的靶点,筛选获得黄疸相关靶点699个。将2个数据库的靶点合并后去重,最终获得652个黄疸的相关靶点。 2.4.3 药物干预疾病的靶点 分别将3种联合用药方案的药物靶点与黄疸的相关靶点取交集,获得茵栀黄颗粒联合谷胱甘肽(联合用药方案1)干预黄疸靶点25个,茵栀黄颗粒联合亮菌甲素(联合用药方案2)干预黄疸靶点22个,茵栀黄颗粒联合双环醇(联合用药方案3)干预黄疸靶点25个,见表3~5。 2.4.4 PPI网络构建与拓扑属性分析 分别将上述3种联合用药方案干预黄疸的靶点映射至STRING数据库(检索时间:2022年6月12日),获得PPI网络,并导入Cytoscape软件进行拓扑属性分析。茵栀黄颗粒联合谷胱甘肽干预黄疸的PPI网络由24个节点和102条边构成,其关键靶点为HMOX1、白蛋白(albumin,ALB)、半胱天冬酶-3(Caspase-3,CASP3)、基质金属蛋白酶-9(matrix metalloproteinase-9,MMP9)、Toll样受体2(Toll-like receptor 2,TLR2),见图4-a;茵栀黄颗粒联合亮菌甲素干预黄疸的分子网络由22个节点和69条边构成,其关键靶点为TLR2、CASP3、ALB、HMOX1、中性粒细胞弹性蛋白酶(neutrophil elastase,ELANE),见图4-b;茵栀黄颗粒联合双环醇干预黄疸的分子网络由23个节点和109条边构成,其关键靶点为TLR2、ALB、CASP3、原癌基因酪氨酸蛋白激酶(proto-oncogene tyrosine-protein kinase,SRC)、表皮生长因子受体(epidermal growth factor receptor,EGFR),见图4-c。
图3 “用药方案-药物-成分-疾病-靶点”网络图
表3 茵栀黄颗粒联合谷胱甘肽干预黄疸的靶点
表4 茵栀黄颗粒联合亮菌甲素干预黄疸的靶点
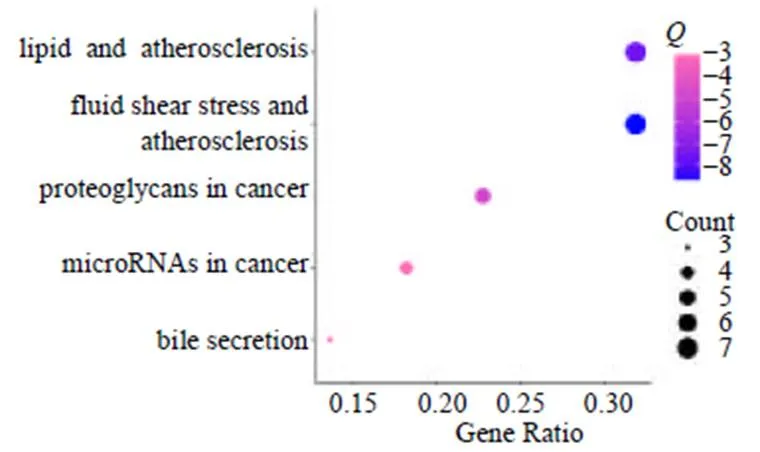
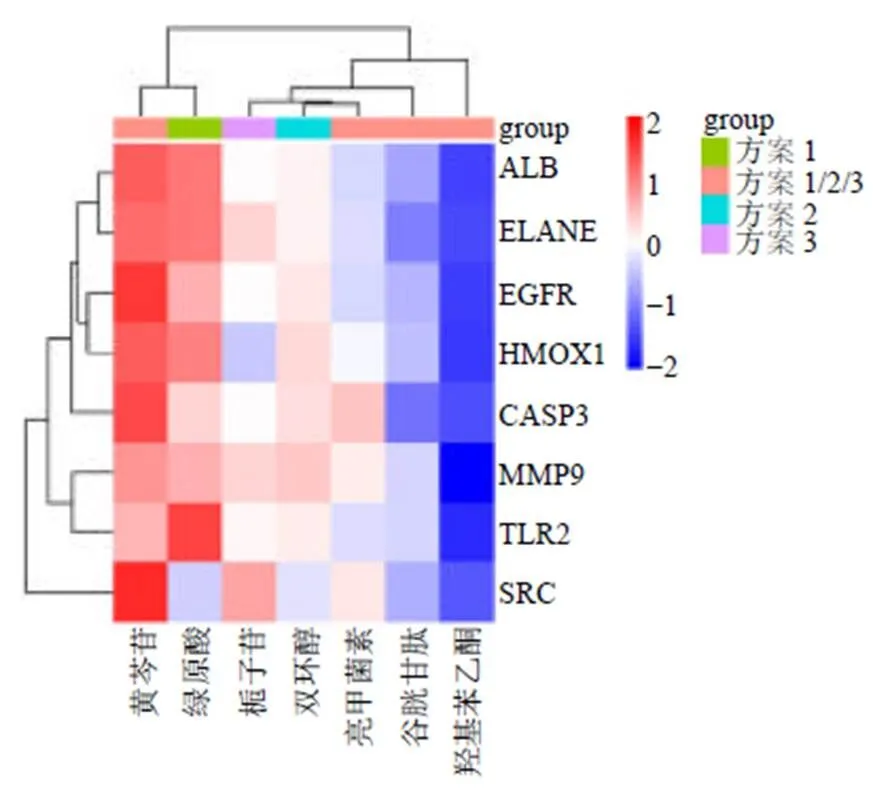
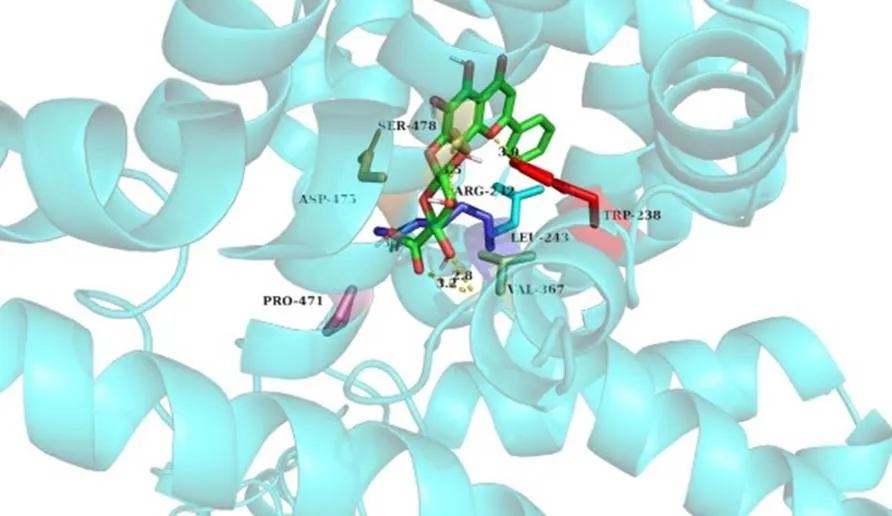
表5 茵栀黄颗粒联合双环醇干预黄疸的靶点 2.4.5 GO生物过程富集分析 运用g:Profiler平台分别对3种联合用药方案干预黄疸的交集靶点进行GO生物过程富集分析,得到茵栀黄颗粒联合谷胱甘肽干预黄疸的GO生物过程 25条,茵栀黄颗粒联合亮菌甲素干预黄疸的GO生物过程15条,茵栀黄颗粒联合双环醇干预黄疸的GO生物过程30条,富集结果见图5-a~c。可见,3种联合用药方案干预黄疸均主要参与机体的炎症免疫、Toll样受体信号通路传导和细胞死亡负调控的生物过程。 2.4.6 KEGG信号通路富集分析 采用Matescape平台对3种治疗黄疸的联合用药方案的KEGG信号通路进行富集分析,设置value cutoff为0.01,并绘制气泡图,见图6~8。如图显示,茵栀黄颗粒联用谷胱甘肽方案参与的关键信号通路有6条,茵栀黄颗粒联用亮菌甲素、双环醇的关键信号通路均各有5条;同时,3种干预方案的共有关键信号通路均与动脉粥样硬化、胆汁分泌有关。此外,联用谷胱甘肽的用药方案还包含谷胱甘肽代谢通路,联用双环醇的用药方案还与上皮细胞信号转导通路有关。 2.5 分子对接验证通过检索ZINC及PubChem数据库,分别获取3种干预方案的有效成分黄芩苷、栀子苷、羟基苯乙酮、绿原酸及化学药谷胱甘肽、亮甲菌素、双环醇与关键靶点HMOX1、ALB、CASP3、MMP9、TLR2、ELANE、SRC、EGFR的三维分子结构,利用Autodock Vina软件进行两两分子对接验证(表6),并将其中对接较好的组合使用Pymol进行可视化展示(图9、10)。由表6可知,除羟基苯乙酮和SRC组合之外,其他组合均可形成稳定结构(结合能<−5.0 kcal/mol,1 kcal=4.186 kJ)。由图9、10可知,分子对接结果最好的成分依次是黄芩苷>绿原酸>栀子苷>双环醇>亮甲菌素>谷胱甘肽>羟基苯乙酮,对接最好的靶点依次是ALB>MMP9>CASP3>HMOX1=EGFR>ELANE>TLR2>SRC,对接最好的组合是ALB与黄芩苷的组合,其主要通过氢键和疏水口袋结合。
a-茵栀黄颗粒联合谷胱甘肽 b-茵栀黄颗粒联合亮菌甲素 c-茵栀黄颗粒联合双环醇 红色圆形节点表示度值(degree)排名前5位的节点,即PPI网络中的核心靶点;灰色线条代表各靶点之间的相互作用关系,线条粗细表示互作关系的综合得分(combined score)大小 3 讨论目前国内外尚无公认的成人黄疸治疗指南,对于黄疸的诊治多从病因角度着手,常与肝病紧密联系,其临床优效用药方案仍在不断探索中。茵栀黄颗粒作为临床常用治疗黄疸的中成药,常与化学药联合使用。因此,在多中心、大样本的电子病历数据基础之上,通过挖掘临床常用的茵栀黄颗粒优效联合用药方案,可以为黄疸的治疗提供临床实证经验。本研究运用Tabu搜索算法进行聚类分析,并与现有肝病相关指南和文献对比,识别出3种茵栀黄颗粒治疗黄疸的核心联用药物方案:(1)针对药物性肝损伤导致的黄疸,可以联用谷胱甘肽;(2)针对胆汁淤积导致的黄疸,可以联用亮菌甲素;(3)针对病毒性肝炎导致的黄疸,可以联用双环醇。 同时,本研究进一步运用网络药理学方法对上述3种核心联用药物方案的分子网络机制进行了初步探索。药物性肝损伤临床可表现为无症状的肝生化指标升高、肝细胞性黄疸、肝功能衰竭、慢性肝炎等。当出现肝细胞性黄疸时,药物性肝损伤的死亡率高达10%[23]。本研究发现,茵栀黄颗粒联用谷胱甘肽治疗药物性肝损伤可能通过干预核心靶点HMOX1、ALB、CASP3、MMP9、TLR2发挥作用,参与氧化应激、核受体元通路(nuclear receptors meta-pathway,NRM)、谷胱甘肽代谢等关键通路。因此,该方案对黄疸的干预作用主要与机体的炎症免疫、Toll样受体信号通路传导、谷胱甘肽代谢通路和细胞死亡负调控的生物过程有关。其中,HMOX1具有抗氧化作用,通过与抗氧化剂反应元件(anti-oxidant response element,ARE)结合而诱导基因表达[28];CASP3和MMP9是中成药抗药物性肝损伤的潜在核心靶点,可能与肝再生过程的正调控密切相关[29]。 胆汁淤积的标志性指标是碱性磷酸酶升高。在黄疸患者中,碱性磷酸酶升高可能代表弥漫性肝细胞功能障碍或严重的胆管阻塞,从而阻碍了足够的胆汁流动[30]。本研究发现茵栀黄颗粒联用亮菌甲素治疗胆汁淤积性黄疸,可能通过干预核心靶点HMOX1、CASP3、ALB、TLR2调控流体切应力与动脉粥样硬化、胆汁分泌等关键通路发挥作用,表明动脉粥样硬化、胆汁分泌异常可能与梗阻性黄疸的发病有一定关联。有研究证明,患有严重动脉粥样硬化的患者可能出现多个内脏假性动脉瘤,包括肝动脉假性动脉瘤出血成大血肿,从而导致梗阻性黄疸和急性胰腺炎[31]。
a-茵栀黄颗粒联合谷胱甘肽干预黄疸的GO分析气泡图 b-茵栀黄颗粒联合亮菌甲素干预黄疸的GO分析气泡图 c-茵栀黄颗粒联合双环醇干预黄疸的GO分析气泡图;气泡颜色由浅到深表示P值由大到小,颜色越深显著富集的程度越大;气泡大小表示富集的基因数量,气泡越大,富集的基因数量越多
图6 茵栀黄颗粒联用谷胱甘肽用药方案的关键信号通路
图7 茵栀黄颗粒联用亮菌甲素用药方案的关键信号通路
图8 茵栀黄颗粒联用双环醇用药方案的关键信号通路 针对病毒性肝炎所致黄疸,茵栀黄颗粒联用双环醇可能主要通过干预SRC、EGFR等核心靶点调控上皮细胞信号转导通路和癌症相关的信号通路而发挥干预作用。从病毒性肝炎到肝硬化再到肝癌的不同阶段,患者在临床上均可见黄疸。EGFR编码的酪氨酸蛋白激酶在肝细胞中充当丙型肝炎病毒的受体并促进其细胞进入[32];SRC编码原癌基因酪氨酸蛋白激酶是调节肝癌发病的重要基因,进而通过调控关键通路对黄疸的病理机制产生影响[33]。
表6 茵栀黄颗粒联合用药方案的有效成分和关键靶点的分子对接结合能 此外,本研究还通过分子对接对3种核心干预方案的分子网络机制进行了初步验证。结果显示,3种干预方案的有效成分和关键靶点构成的三维分子结构中,对接最好的组合是ALB与黄芩苷的组合。研究显示,ALB编码人体白蛋白,有助于提升氧结合活性、胆红素结合活性,还参与细胞对饥饿的反应,维持线粒体位置和凋亡过程的负调节[34];同时,其与肝胆系统癌症有关,为肝病的生物标志物。黄芩苷是黄芩的活性成分,具有抗炎、抗氧化、抗病毒、抗动脉粥样硬化、抗肿瘤等作用[35],因此黄芩苷可以对(病毒性)肝炎和黄疸有直接的干预作用。综上,通过3种茵栀黄颗粒联合用药方案共有的活性成分黄芩苷调控分子对接结果最佳的ALB靶点,可有效将胆红素从循环白蛋白中置换出来,使循环中的游离胆红素水平升高,缓解黄疸的临床症状。
图9 茵栀黄颗粒联合用药方案的有效成分与关键靶点的分子对接结合能聚类热图
绿色小分子为黄芩苷,蓝色大分子为ALB靶点,黄色虚线为氢键 在方法学方面,本研究创新性地将真实世界HIS系统数据采用Tabu搜索算法进行聚类分析,测度子群结构关系,同时融合靶点网络与分子对接对茵栀黄颗粒干预黄疸的3种干预方案的分子网络机制进行了分析及初步验证。一方面,与其他算法相比,Tabu搜索算法的优势在于可以通过迭代出的密度矩阵测度指标群之间的关系,并且能应用合理的参数设置,对指标节点进行若干次的划分,完成指标集群和群间关系测度的数据整合,避免划分过度或划分不足导致的指标节点分配不均衡的问题。另一方面,鉴于中医药临床数据的“混杂性”“整体性”和“相关关系性”,在数据挖掘的核心联合用药方案基础上,使用靶点网络和分子对接方法对3种联合用药方案的有效性作用机制进行分析和初步验证,可以更好地支撑和佐证茵栀黄颗粒临床诊疗黄疸的联合用药规律,进而探索新的研究方向并为临床实际问题的解决提供指导和参考。 在诊疗用药方面,本研究运用Tabu算法聚类得出的子群结构关系,结合现有相关指南、文献报道将黄疸划分为3类,并归纳出对应的精准茵栀黄颗粒联合用药方案,针对不同类型的黄疸进行倾向性、个体化治疗,符合中医“方对证,药对症”原创思维[36]和“态靶辨证”[37],不仅能达到更好的治疗效果,也为临床精准用药方案的制定提供参考,同时符合中医发展的历史需求。此外,临床联合用药还应关注其安全性,重视联用药物的剂量和频次。因此,临床实际应用过程中,应根据患者的疾病进展情况,合理评估临床联合用药方案的疗效及安全性,注意用药配伍禁忌。建议未来研究者基于本研究进一步开展高质量的真实世界临床研究,在科学合理的顶层设计下获得更高级别的循证证据。 本研究是基于真实世界HIS数据库的回顾性研究,运用数据挖掘技术获得的核心联用药物方案的有效性仅供临床用药参考。受限于回顾性研究的设计类型及HIS系统的样本量,结果仍需进一步前瞻性多中心、大样本的临床研究加以验证。同时,本研究的分子机制结果可能由于靶点网络数据库的权重分配和混杂性存在一定的偏倚,因此结果的查全性和准确性尚需指纹图谱研究、基础实验或生物样本的高通量测序等方法进一步验证。 利益冲突 所有作者均声明不存在利益冲突 [1] 牟春笋. 新生儿黄疸阴阳属性影响因素及Bayes概率模型初步构建 [D]. 济南: 山东中医药大学, 2014. [2] Bhutani V K, Zipursky A, Blencowe H,. Neonatal hyperbilirubinemia and Rhesus disease of the newborn: Incidence and impairment estimates for 2010 at regional and global levels [J]., 2013, 74(Suppl 1): 86-100. [3] Slusher T M, Zamora T G, Appiah D,. Burden of severe neonatal jaundice: A systematic review and meta-analysis [J]., 2017, 1(1): e000105. [4] Mwaniki M K, Atieno M, Lawn J E,. Long-term neurodevelopmental outcomes after intrauterine and neonatal insults: A systematic review [J]., 2012, 379(9814): 445-452. [5] Amiri M S, Joharchi M R, Taghavizadehyazdi M E. Ethno-medicinal plants used to cure jaundice by traditional healers of Mashhad, Iran [J]., 2014, 13(1): 157-162. [6] Zhang C, Zhang L D, Lyu J,. Effects of Yinzhihuang granules on serum liver enzymes in jaundice patients: A real-world study based on HIS data [J]., 2020, 2020: 3843752. [7] Rennie J, Burman-Roy S, Murphy M S,. Neonatal jaundice: Summary of NICE guidance [J]., 2010, 340: c2409. [8] 杜娟, 朱小琴. 茵栀黄颗粒治疗新生儿病理性黄疸 [J]. 吉林中医药, 2018, 38(9): 1046-1049. [9] 黄横, 余宇龙, 李绍锦, 等. 不同剂量茵栀黄颗粒治疗早期新生儿高胆红素血症的效果观察 [J]. 现代实用医学, 2018, 30(7): 908-910. [10] Zhang C, Zhang L D, Lyu J,. Effects of Yinzhihuang granules on serum liver enzymes in jaundice patients: A real-world study based on HIS data [J]., 2020, 2020: 3843752. [11] 赵丹丹, 高翔羽. 茵栀黄在新生儿高胆红素血症中的应用评价 [J]. 中华针灸电子杂志, 2016, 5(3): 124-129. [12] 郜明月, 谢雁鸣, 张寅, 等. 基于电子医疗数据的复方苦参注射液治疗适应症(恶性肿瘤) 真实世界临床应用特征研究[J]. 中草药, 2018, 49(13): 3143-3147. [13] 万学红, 卢雪峰. 诊断学 [M]. 北京: 人民卫生出版社, 2013: 36-39. [14] 盛蕾, 谢雁鸣, 王志飞, 等. 喜炎平注射液治疗病毒性脑炎用药方案的真实世界研究 [J]. 中草药, 2022, 53(10): 3125-3133. [15] 国家中医药管理局, 国家卫生健康委员会. 关于印发《中医病证分类与代码》和《中医临床诊疗术语》的通知[EB/OL]. (2022-08-20) [2020-11-16]. http://www.gov. cn/zhengce/zhengceku/2020-11/24/content_5563703.htm. [16] 葛均波. 内科学[M]. 第8版. 北京: 人民卫生出版社, 2013: 422-424. [17] 侯丽, 李丹亚, 李军莲, 等. ICD系列编码规则及结构体系剖析 [J]. 医学信息学杂志, 2012, 33(5): 38-43. [18] 世界卫生组织药物统计中心. 《药品的解剖学治疗学化学分类索引及规定日剂量》[M]. 北京:中国协和医科大学出版社, 2003: 122-123. [19] 国家卫生健康委员会. 《国家基本药物目录-2018年版》[EB/OL]. (2022-08-20) [2018-10-25]. http://www. nhc. gov.cn/wjw/jbywml/list.shtml. [20] 国家医保局, 人力资源社会保障部. 关于印发《国家基本医疗保险、工伤保险和生育保险药品目录(2020年)》的通知[EB/OL]. (2022-08-20) [2020-12-28]. http:// www.nhsa.gov.cn/art/2020/12/28/art_37_4220.html. [21] 中国药典 [S]. 一部. 2020. [22] 程豪, 易丹辉, 牟宗毅. 基于社会网络分析的指标群划分及群间关系研究 [J]. 世界科学技术—中医药现代化, 2018, 20(4): 505-513. [23] 王宇明, 于乐成. 肝脏炎症及其防治专家共识 [J]. 中国实用内科杂志, 2014, 34(2): 152-162. [24] 王锡钦. 亮菌甲素联合茵栀黄治疗胆汁瘀积型肝炎34例 [J]. 中国中西医结合消化杂志, 2006, 14(4): 273-274. [25] 谢雯, 于乐成. 双环醇临床应用专家共识: 2020版 [J]. 中华实验和临床感染病杂志: 电子版, 2020, 14(3): 177-185. [26] 王英强, 申建军, 孙玉梅. 口服双环醇片及小柴胡汤加减治疗急性乙型黄疸型肝炎50例分析 [J]. 山西医药杂志, 2008, 37(10): 944-945. [27] 张振英. 双环醇联合腺苷蛋氨酸治疗病毒性肝炎重度黄疸临床观察 [J]. 河南大学学报: 医学版, 2008, 27(3): 55-56. [28] Bereczki D Jr, Balla J, Bereczki D. Heme oxygenase-1: Clinical relevance in ischemic stroke [J]., 2018, 24(20): 2229-2235. [29] Huang S J, Mu F, Li F,. Systematic elucidation of the potential mechanism of Erzhi Pill against drug-induced liver injury via network pharmacology approach [J]., 2020, 2020: 6219432. [30] Gondal B, Aronsohn A. A systematic approach to patients with jaundice [J]., 2016, 33(4): 253-258. [31] Saito A, Fayad N. An unusual cause of obstructive jaundice and acute pancreatitis: Visceral artery pseudoaneurysm [J]., 2021, 13(4): e14307. [32] Lupberger J, Zeisel M B, Xiao F,. EGFR and EphA2 are host factors for hepatitis C virus entry and possible targets for antiviral therapy [J]., 2011, 17(5): 589-595. [33] 王丽萍. CLDN6通过激活Src/STAT3信号通路促进肝癌细胞的迁移及侵袭 [D]. 长春: 吉林大学, 2022. [34] National Center for Biotechnology Information. PubChem Gene Summary for Gene 213, ALB-albumin (human) [EB/OL]. [2022-08-19]. https://pubchem.ncbi.nlm.nih. gov/gene/213. [35] National Center for Biotechnology Information. PubChem Compound Summary for CID 64982, Baicalin [EB/OL]. [2022-08-19]. https://pubchem.ncbi.nlm.nih.gov/compound/ 64982. [36] 王琦. 中医原创思维模式研究 [J]. 世界中医药, 2013, 8(1): 1-4. [37] 张莉莉, 仝小林, 赵林华, 等. 态靶结合辨治多囊卵巢综合征高雄激素血症 [J]. 世界中医药, 2021, 16(22): 3372-3375. Combination medication regimen and molecular mechanism analysis of Yinzhihuang Granule in treatment of jaundice based on real world and target network clustering CUI Xin1, ZHANG Cheng1, XI Jun-yu1, XIE Yu-ting2, LIU Yi1, XIE Yan-ming1 1. Institute of Clinical Basic Medicine of Traditional Chinese Medicine, China Academy of Chinese Medical Sciences, Beijing 100700, China 2. School of Statistics, Renmin University of China, Beijing 100872, China To mine the clinical application rules of Yinzhihuang Granule (茵栀黄颗粒) combined with drug regimen in the treatment of jaundice, so as to provide reference for exploring different clinical diagnosis and treatment ideas, medication experience and improving the evidence-based level of clinical evidence of traditional Chinese medicine.Based on the medication data of jaundice patients from 39 hospital information system (HIS) in China, the Tabu search algorithm was used to retrospectively analyze the combination medication of Yinzhihuang Granule in the treatment of jaundice in the real world. At the same time, the molecular network mechanism of the core drug combination regimen was analyzed by the target network, and the mechanism was verified by molecular docking technology.According to the results of Tabu search algorithm cluster analysis, combined with liver disease related guidelines and literature, three core combined drug schemes for Yinzhihuang Granule in the treatment of jaundice were identified: (1) For jaundice caused by drug-induced liver injury, glutathione could be combined; (2) For jaundice caused by cholestasis, armillarisin A could be combined; (3) For jaundice caused by viral hepatitis, bicyclol could be combined. The molecular network mechanism of the three regimentsall had the characteristics of multi-component, multi-target and multi-pathway. The molecular network mechanism of Yinzhihuang Granule combined with glutathione in the treatment of jaundice was mainly related to the body’s inflammation and immunity, Toll-like receptor signaling pathway, glutathione metabolism pathway and the biological process of negative regulation of cell death. The molecular network mechanism of Yinzhihuang Granule combined with armillarisin A in the treatment of jaundice was mainly related to key pathways such as atherosclerosis and bile secretion. The molecular network mechanism of Yinzhihuang Granule combined with bicyclol in the treatment of jaundice was mainly related to epithelial cell signal transduction pathway and cancer related signal pathway.The core drug combination regimen of Yinzhihuang Granule in this study basically conforms to the relevant guidelines and diagnosis and treatment norms, and its mechanism was explored, which provides certain guidance and reference for optimizing clinical drug combination and rational drug use. It is suggested that the efficacy and safety of clinical combined drug regimen should be reasonably evaluated according to the disease progression of jaundice in clinical practice, and the contraindications of medication compatibility should be paid attention. Yinzhihuang Granule; jaundice; real world study; combination of drugs; glutathione; armillarisin A;bicyclol; baicalin; gardenin; hydroxy-ethyl ketone; chlorogenic acid R285.64 A 0253 - 2670(2023)01 - 0210 - 12 10.7501/j.issn.0253-2670.2023.01.023 2022-08-21 国家重点研发计划项目(2018YFC1707400) 崔 鑫,博士研究生,研究方向为中医药临床评价方法学研究。E-mail: [email protected] 通信作者:刘 毅,医师,研究方向为中医药临床评价方法学研究。E-mail: [email protected] 谢雁鸣,首席研究员,研究方向为中医药临床评价方法学研究。E-mail: [email protected] [责任编辑 潘明佳] 猜你喜欢 双环谷胱甘肽黄疸 新生儿黄疸治疗箱常见故障处置及预防性维护实践现代仪器与医疗(2022年3期)2022-08-12鲁晓岚:黄疸肝博士(2022年3期)2022-06-30双环磺草酮与吡嘧磺隆混用对稻稗的防治效果试验安徽农学通报(2022年8期)2022-05-06谷胱甘肽:防治中风改善帕金森症状现代养生·上半月(2021年10期)2021-09-24碳氧血红蛋白在新生儿ABO溶血性黄疸中的临床意义昆明医科大学学报(2021年5期)2021-07-22谷胱甘肽的研究进展中国药剂学杂志(网络版)(2019年4期)2019-07-17新生儿出现母乳性黄疸可以继续喂母乳吗?益寿宝典(2018年14期)2018-01-27模仿到底家用汽车(2016年12期)2017-02-09蚯蚓谷胱甘肽转硫酶分离纯化的初步研究天然产物研究与开发(2016年6期)2016-06-05瑞替普酶联合还原型谷胱甘肽治疗急性ST段抬高型心肌梗死疗效分析中国继续医学教育(2015年3期)2016-01-06
|
【本文地址】









 中草药2023年1期
中草药2023年1期