《自然》子刊:釜底抽薪,中国科学家做到了!科学家发现首个PUS7特异性抑制剂,有望成为靶向脑胶质瘤表观修饰的新疗法丨科学大发现 |
您所在的位置:网站首页 › 胶质瘤有望治愈 › 《自然》子刊:釜底抽薪,中国科学家做到了!科学家发现首个PUS7特异性抑制剂,有望成为靶向脑胶质瘤表观修饰的新疗法丨科学大发现 |
《自然》子刊:釜底抽薪,中国科学家做到了!科学家发现首个PUS7特异性抑制剂,有望成为靶向脑胶质瘤表观修饰的新疗法丨科学大发现
|
首先,研究人员在多个GBM相关数据库和临床样本中,分析比较了GBM组织和正常组织中的所有PUS酶的表达水平,发现 PUS7在GBM组织中高表达,并且与预后不良有关。 另外,研究还发现 PUS7蛋白在胶质瘤干细胞中的表达水平显著高于他类型细胞。基于胶质瘤干细胞的“特殊性”,研究人员认为PUS7对于GBM的发展有重要作用。
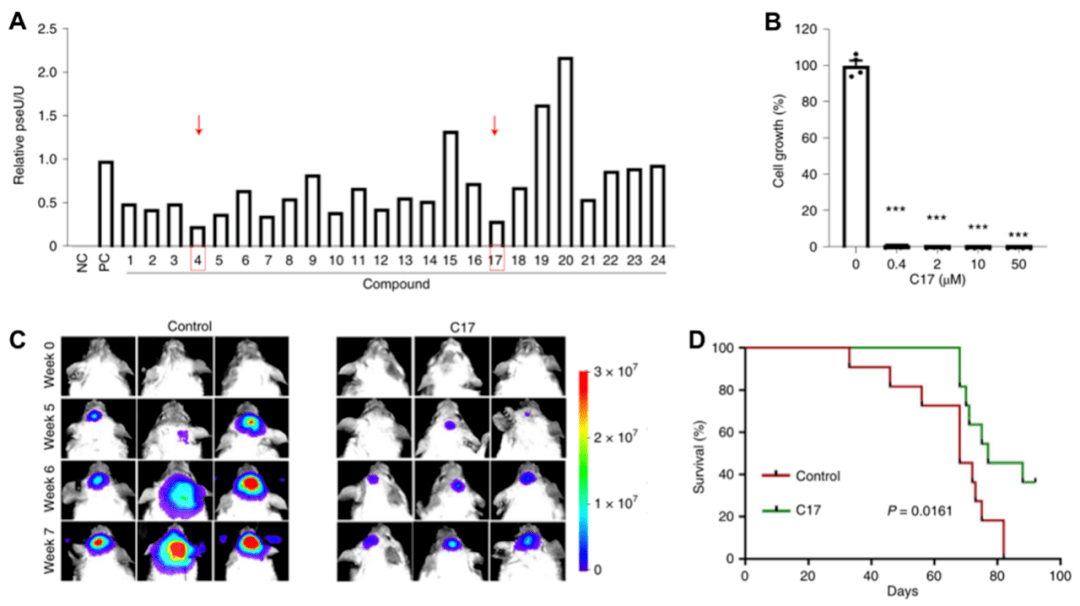
PUS7在GBM患者和胶质瘤干细胞中高表达 为了弄清PUS7在胶质瘤干细胞中的作用,研究者们通过基因编辑的方法,调控胶质瘤干细胞中PUS7的表达水平,结果发现:当 下调胶质瘤干细胞中PUS7表达后,胶质瘤干细胞的干性和生长速度 会显著降低 ,并导致小鼠体内GBM的发展受限。 只有恢复PUS7的表达水平和催化功能,方可抵消此前PUS7敲除导致胶质瘤干细胞的生长劣势,以及恢复GBM在体内进展速度。这说明, 胶质瘤干细胞的生长和自我更新过程依赖于PUS7的催化活性。 PUS7的表达水平影响胶质瘤干细胞生长和干性 为了解直接抑制PUS7功能对GBM的治疗效果,研究人员采用了将基于结构的虚拟筛选与体外PUS7酶活性测定相结合的方法,从 国家癌症研究所发展治疗计划(NCI-DTP)的27万种化合物和 FDA批准的4086种药物库中,筛选得到两个目标化合物。 随后,研究人员结合C17治疗小鼠GBM的效果,再次证明: 抑制PUS7催化假尿苷修饰功能,确实能够显著延缓GBM进展。
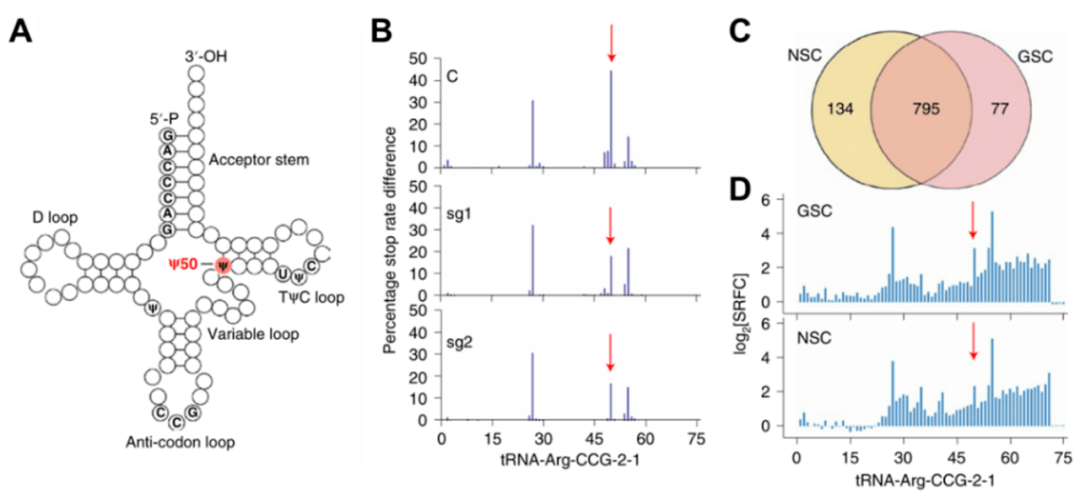
PUS7靶向抑制剂C17可显著延缓胶质瘤干细胞生长和体内GBM肿瘤进展 那么PUS7又是如何调控胶质瘤干细胞的生长的呢? 为了搞清楚PUS7影响胶质瘤干细胞生长的机制,研究人员采用一种先进的RNA测序方法 (DM-Ψ-seq), 在tRNA上找到受PUS7调控的特定修饰位点。 通过与正常干细胞测序结果对比发现, 该位点在胶质瘤干细胞中的假尿苷修饰水平明显高于正常干细胞,这就表明该位点的修饰差异可能是PUS7特异性调控胶质瘤干细胞生长的关键原因。 我们都知道,tRNA是翻译机器的重要组成部分,需要经过复杂的修饰加工后才能成熟。而RNA修饰在控制RNA功能和调节基因表达方面发挥关键作用,因此, PUS7介导的tRNA假尿苷修饰程度的改变,可能影响到胶质瘤干细胞内关键信号蛋白翻译。
PUS7特异性调控胶质瘤干细胞中tRNA特定位点的假尿苷修饰 为了弄清PUS7的敲除改变了细胞内哪类信号通路,研究人员又进行了RNA-Seq检测,并经通路富集发现 PUS7负调控胶质瘤干细胞干扰素途径。 将这个发现结合蛋白组检测,研究人员发现此前鉴定的胶质瘤干细胞内tRNA特定位点处假尿苷修饰情况,恰好 影响酪氨酸激酶2 (TYK2)蛋白的翻译效率。 基于以上研究成果不难看出, PUS7会改变tRNA特定位点的假尿苷修饰程度,继而影响到受TYK2控制的干扰素刺激基因表达;而干扰素介导的抗肿瘤效应和免疫调节,在癌症进展和治疗中起着至关重要的作用[9]。这就是PUS7调控胶质瘤干细胞生长和GBM发展的机制。 PUS7通过改变TYK2翻译下调IFN途径并调节胶质瘤干细胞生长 总的来说,基于测序技术的进步,本研究发现了假尿苷修饰与肿瘤之间的紧密联系,弥补了RNA修饰的研究空白。 此外,本研究既探索出有效治疗GBM的表观修饰相关新的靶点,又筛选、鉴定了针对该靶点的首例PUS7的选择性抑制剂,为新靶点PUS7对GBM的治疗价值提供了强有力的证据。 不过,本研究发现的C17作为极具前景的先导化合物,在走向临床、成为药物之前,还需要经历多重检验和进一步的优化改造。 道阻且长,行则将至,行而不辍,未来可期。
奇点上新 这次的课程,我们 用10讲系统梳理了晚期肺癌治疗20年的风云变幻。 细致盘点了靶向治疗的最新进展,也全面展现了罕见靶点研究的勃勃生机。 当然免疫治疗也是重中之重,我们会带你再次洞察免疫治疗的深层机制,深入免疫治疗最前线,探讨迈入无化疗时代的治疗选择,一起见证辅助和新辅助治疗开疆拓土的战绩。 除此之外,我们还会和你一起凝视纷繁复杂的生物标志物研究,探究免疫治疗新靶点的无限潜力。 当然,深度不意味着晦涩,复杂不等同于繁复。我们竭尽全力将这些庞杂的知识点融汇成精湛的音频课程,让你听得轻松、顺畅,不头大,让这些知识快速整合到我们的认知体系,成为下一步进阶的土壤。 参考文献: [1] Stupp R, Hegi ME, Mason WP, et al. Effects of radiotherapy with concomitant and adjuvant temozolomide versus radiotherapy alone on survival in glioblastoma in a randomised phase III study: 5-year analysis of the EORTC-NCIC trial. Lancet Oncol. 2009;10(5):459-466. doi:10.1016/S1470-2045(09)70025-7. [3] Bao S, Wu Q, McLendon RE, et al. Glioma stem cells promote radioresistance by preferential activation of the DNA damage response. Nature. 2006;444(7120):756-760. doi:10.1038/nature05236. [5] Li X, Ma S, Yi C. Pseudouridine: the fifth RNA nucleotide with renewed interests. Curr Opin Chem Biol. 2016;33:108-116. doi:10.1016/j.cbpa.2016.06.014. [6] Schwartz S, Bernstein DA, Mumbach MR, et al. Tranome-wide mapping reveals widespread dynamic-regulated pseudouridylation of ncRNA and mRNA. Cell. 2014;159(1):148-162. doi:10.1016/j.cell.2014.08.028. [8] Waalkes TP, Dinsmore SR, Mrochek JE. Urinary excretion by cancer patients of the nucleosides N-dimethylguanosine, 1-methylinosine, and pseudouridine. J Natl Cancer Inst. 1973;51(1):271-274. doi:10.1093/jnci/51.1.271.返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |