EAS2022 |
您所在的位置:网站首页 › 胰岛b细胞的生理作用 › EAS2022 |
EAS2022
|
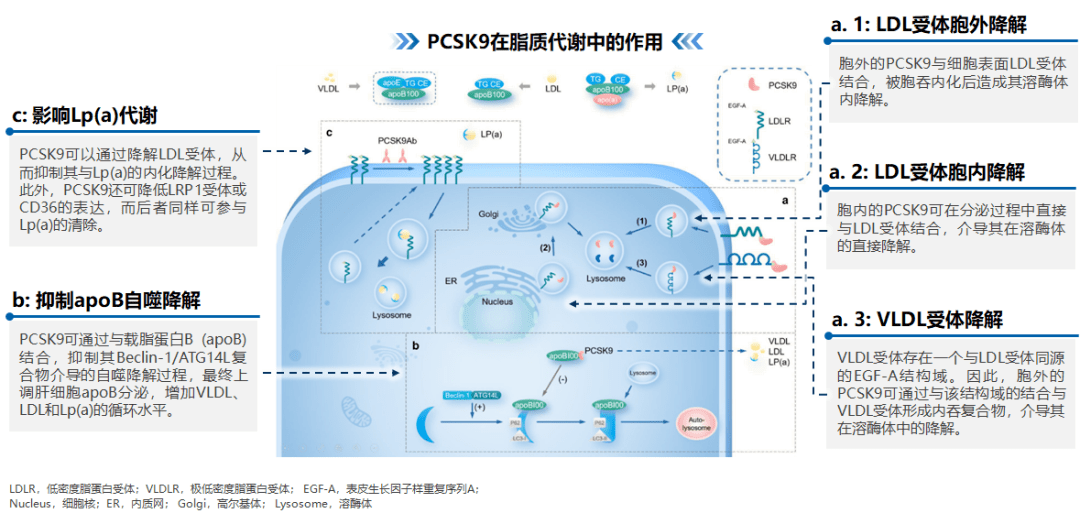
LDL受体降解: 目前认为存在两条途径,其一为经典的 胞外途径,即分泌至胞外的PCSK9与细胞表面LDL受体结合,被胞吞内化后造成其溶酶体内的降解;其二为新近研究提示的 胞内途径,即胞内的PCSK9可在合成分泌过程中直接与LDL受体结合,介导其在溶酶体的直接降解 。 VLDL受体降解: PCSK9可调控极低密度脂蛋白(VLDL)受体表达,从而影响VLDL颗粒的清除。其原理在于VLDL受体存在一个与LDL受体同源的EGF-A结构域,因此胞外PCSK9可通过与该结构域的结合,和VLDL受体形成内吞复合物,介导其在溶酶体中的降解。 抑制载脂蛋白B(apoB)自噬降解: PCSK9可通过与apoB结合,抑制其Beclin-1/ATG14L复合物介导的自噬降解过程,最终上调肝细胞apoB分泌,增加循环VLDL、LDL和Lp(a)水平。 影响Lp(a)代谢: 目前PCSK9影响Lp(a)代谢的途径尚未完全阐明,有观点认为PCSK9可通过降解LDL受体,从而抑制其与Lp(a)的内化降解过程。此外,PCSK9还可降低LRP1受体或CD36的表达,而后者同样可参与Lp(a)的清除 [4] 。
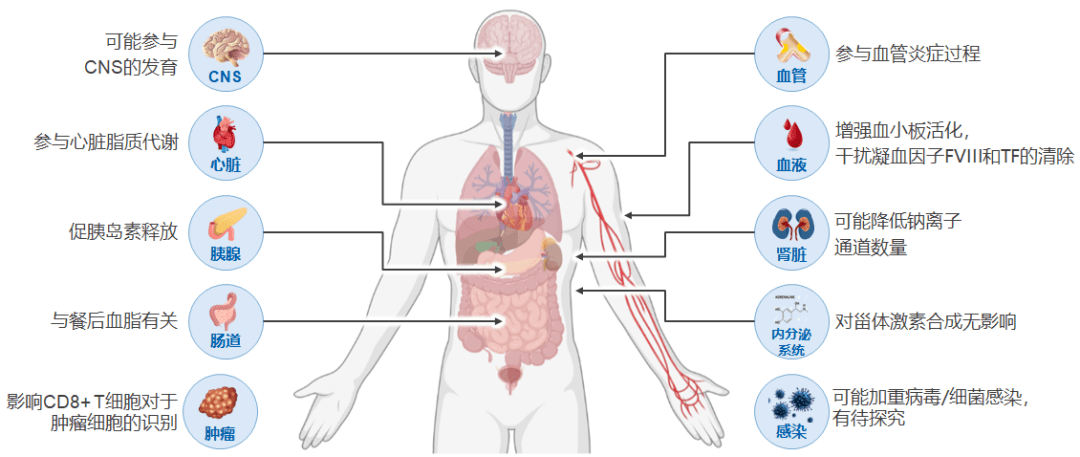
图1. PCSK9的肝内作用:通过多途径调节肝脏脂质代谢 02 肝外作用 多项基础或临床研究表明,PCSK9可参与肝脏外的多项生理病理过程,涉及心血管、消化、神经、泌尿、内分泌等多个系统(图2) [5] :
图2. PCSK9的肝外作用:参与多项生理病理过程 血管炎症: 炎症是动脉粥样硬化重要的发病机制之一,PCSK9通过增加LOX受体和Toll样受体4(TLR4)表达这两个途径来 参与血管炎症,从而激活NF-κB通路,上调IL-6、IL-1、TNF、IFN和MCP-1等基因表达,最终促进动脉粥样硬化斑块的进展 [6] 。既往动物和临床研究表明,抑制PCSK9可减轻系统和局部的血管炎症 [6-7] 。 血栓: 斑块破裂血栓形成可导致急性心血管事件。PCSK9通过激活血小板的CD36和LOX-1受体来 增强血小板活化[8-9] ,研究结果显示,ACS患者中PCSK9水平增加与血小板反应性增加存在显著相关性 [10] 。PCSK9还可 干扰体内凝血因子FVIII和组织因子的清除[8-9] ,研究发现,冠心病合并糖尿病患者中PCSK9水平与血浆组织因子水平存在明显的正相关 [11] 。以上作用均提示PCSK9可促进血栓形成。 心脏: PCSK9在 心脏脂质代谢中起重要作用。近年一项发表在 EHJ 的研究发现PCSK9缺失可导致小鼠心肌细胞中脂滴蓄积、线粒体嵴密度降低,进而导致射血分数保留的心力衰竭(HFpEF)。值得注意的是, 仅敲除肝脏PCSK9(即循环PCSK9缺失)并不影响心脏脂质代谢,局部PCSK9的缺失可能才是造成心脏代谢异常的关键 [12] 。 胰腺: PCSK9与 胰岛β细胞胰岛素释放相关。同样是近年发表于 EHJ 的一项研究显示,PCSK9缺失会导致胰岛β细胞内出现胆固醇过载,进而抑制葡萄糖介导的胰岛素释放过程。进一步实验显示, 仅敲除肝脏PCSK9(即循环PCSK9缺失)不会导致上述效应,胰岛δ细胞产生的PCSK9可能才是关键 [13] 。而一项针对多种PCSK9靶向药物(依洛尤单抗、阿利西尤单抗、英克西兰)的Meta分析结果显示, PCSK9单抗和PCSK9 siRNA在新发糖尿病风险上和安慰剂相比并无显著差异[14] 。 中枢神经系统: 虽然有动物实验结果显示PCSK9 可能参与CNS发育与重塑[15] ,但目前临床研究尚未证实其具体的临床意义。孟德尔随机化研究显示,PCSK9功能缺失性(loss of function,LOF)突变导致的低LDL-C水平, 不会导致阿尔兹海默病、血管性痴呆及其他痴呆、帕金森病风险的升高[16] 。而以认知功能为主要终点的大型RCT EBBINGHAUS研究显示,与安慰剂相比,PCSK9单抗治疗 并未带来额外的不良认知功能影响[17] 。 肠道: 有观点认为,抑制PCSK9可通过增加富含甘油三酯脂蛋白颗粒的清除和减少apoB48的分泌来 影响餐后甘油三酯水平[5] 。在动物实验中,肝脏产生的循环PCSK9而非肠道局部的PCSK9能够影响餐后血脂 [18] 。而临床试验中,PCSK9单抗仅能降低糖尿病患者餐后血脂中运输胆固醇的脂蛋白颗粒(VLDL 2 、IDL和LDL),对运输甘油三酯的脂蛋白颗粒影响较小(CM、VLDL 1 ) [19] 。 肾脏: 目前认为PCSK9 可能与肾脏钠离子通道表达有关,但结果并不一致。细胞实验发现PCSK9可降低肾脏HEK293细胞表面的钠离子通道表达,提示其在机体血压调节中的潜在作用 [20] ,但动物研究发现PCSK9缺乏并不影响高血压小鼠的血压 [21] 。 内分泌系统/甾体激素: 现有临床研究 尚未发现PCSK9会影响激素水平,包括促肾上腺皮质激素、皮质醇、雌二醇、睾酮等 [22] 。 感染: PCSK9水平升高 可能加重病毒/细菌感染,但其在感染性疾病中的角色有待进一步发掘 [23] 。 综上所述,PCSK9虽然主要由肝脏合成,但是能够参与肝内及肝外的多项生理病理过程,涉及机体多个器官系统,同时有些过程主要由局部PCSK9介导。进一步的,PCSK9作为新型降脂药物重要的干预靶点,深入了解其生物学功能更有助于理解不同PCSK9靶向药物在作用机制上的区别,以及与之对应的临床效应特点。
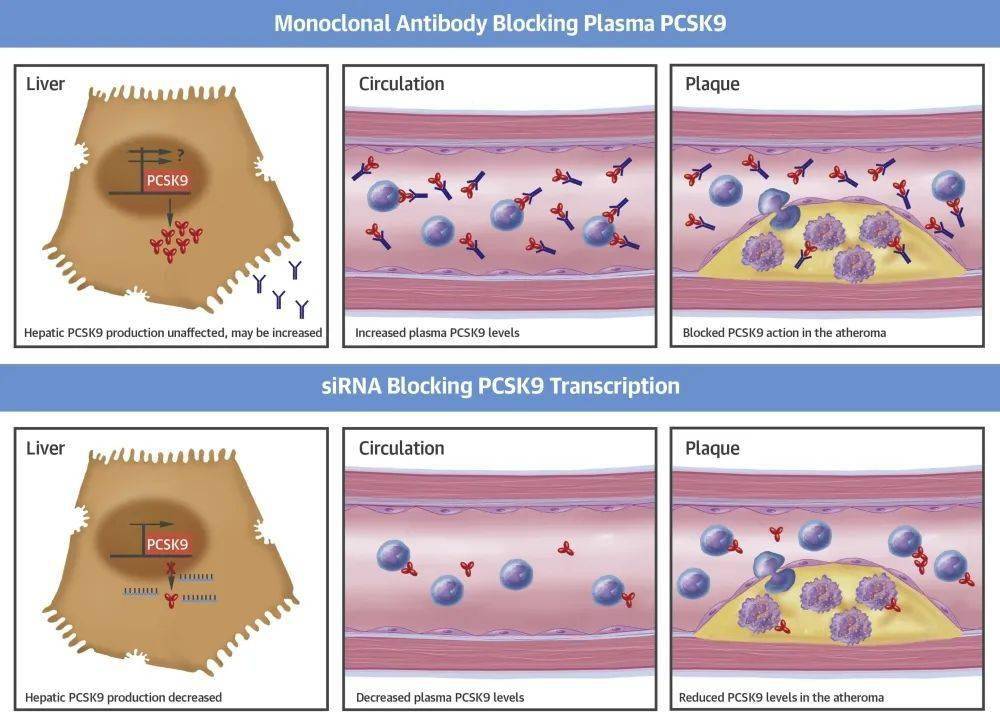
二、PCSK9靶向药物: 作用机制分类及其相关效应的思考 01 PCSK9靶向药物作用机制分类 PCSK9靶向药物的基本原理是通过干预PCSK9蛋白功能,从而提高肝细胞表面LDL受体表达,增加血浆中LDL颗粒的清除,最终降低LDL-C水平。目前现有的PCSK9靶向药物大体可分为两类(图3) [25-26] : 抑制PCSK9蛋白/LDL受体作用(如单克隆抗体): 单抗药物主要通过 结合循环PCSK9蛋白,抑制其与肝细胞表面LDL受体的相互作用发挥效应;同时也能抑制动脉粥样硬化斑块中的PCSK9。但其并不能减少、甚至可能负反馈增加肝脏PCSK9的合成分泌,同时导致血浆中总的PCSK9水平升高(~10倍) 。 抑制PCSK9蛋白合成(如小干扰RNA,即siRNA): PCSK9 siRNA直接在mRNA层面 干预肝脏PCSK9蛋白合成,可在源头上降低循环PCSK9水平,动脉粥样硬化斑块中PCSK9水平也随之减少 。
图3. PCSK9靶向药物的两种主要作用机制 (引自Rosenson RS, et al. J Am Coll Cardiol. 2018) 02 PCSK9单抗和PCSK9 siRNA的异同 从上述PCSK9多效性以及实现干预PCSK9的两种思路来看,PCSK9 siRNA存在几个特点:首先,PCSK9 siRNA能够 干预肝脏PCSK9胞内和胞外功能,但目前尚未有临床研究证实其额外获益 [4] ;其次,PCSK9 siRNA通过特殊递送系统靶向肝脏, 不影响肝外其他器官PCSK9的表达,安全性良好;再者,PCSK9 siRNA 不会引起肝脏PCSK9的负反馈调节和血浆总PCSK9水平的积蓄;最后,PCSK9 siRNA拥有特殊的药代/药效动力学特征,能够 超长效干预PCSK9功能,解决临床上依从性带来的相关问题 。
三、 结语 自2003年被发现以来,PCSK9一直被视为降脂新兴靶点而成为研究热点。近年来越来越多的研究表明:PCSK9的生物学功能并未局限于LDL-C调控,它不仅通过多种途径调节肝脏脂质代谢,同时还能参与肝外多个脏器的生理病理过程,其循环水平的升高可能与血管炎症、血栓形成、餐后血脂有关,而其局部的缺失又可能影响心脏脂质代谢、胰腺胰岛素分泌,更有研究发现其在肿瘤治疗中的潜在价值。 正是基于对PCSK9机制了解的不断更新,引发了对于PCSK9靶向药物更深层次的思考。PCSK9单抗与PCSK9 siRNA在机制上存在异同,而后者作为一类崭新机制的药物,拥有许多值得关注的特点,也期待未来更多的研究能够带来更多的证据! 参考文献 (上下滑动可查看) 1. Abifadel M, et al. Nat Genet. 2003; 34(2): 154-156. 3. Tang Y, et al. Cardiovasc Diabetol. 2020; 19(1): 33. 4. Shapiro MD, et al. Cir Res. 2018; 122(10): 1420-1438. 5. Stoekenbroek RM, et al. Nat Rev Endocrinol. 2018; 15(1): 52-62. 7. Momtazi-Borojeni AA, et al. Eur Heart J Cardiovasc Pharmacother. 2019; 5(4): 237-245. 8. Paciullo F, et al. Thromb Haemost. 2019; 119(3): 359-367. 9. Puteri MU, et al. Life (Basel). 2022; 12(2): 190. 10. Navarese EP, et al. Int J Cardiol. 2017; 227: 644-649. 11. Wang M, et al. J Geriatr Cardiol. 2016; 13(4): 312-315. 13. Da Dalt L, et al. Eur Heart J. 2019; 40(4): 357-368. 14. Talasaz AH, et al. Pharmacotherapy. 2021; 41(12): 1009-1023. 15. Seidah NG, et al. Proc Natl Acad Sci U S A. 2003; 100(3): 928-933. 16. Benn M, et al. BMJ. 2017; 357: j1648. 17. Giugliano RP, et al. N Engl J Med. 2017; 377(7): 633-643. 18. Garcon D, et al. Arterioscler Thromb Vasc Biol. 2020; 40(9): 2084-2094. 19. Taskinen MR, et al. Arterioscler Thromb Vasc Biol. 2021; 41(2): 962-975. 21. Berger JM, et al. Atherosclerosis. 2015; 239(1): 252-259. 22. Blom DJ, et al. Circ Res. 2015; 117(8): 731-741. 23. Seidah NG, Prat A. Endocr Rev. 2021: bnab035. 24. Liu X, et al. Nature. 2020; 588(7839): 693-698. 25. Rifai MA, et al. Nat Rev Cardiol. 2021; 18(12): 805-806. 26. Rosenson RS, et al. J Am Coll Cardiol. 2018; 72(3): 314-329.
专家简介 李建军 教授 中国医学科学院阜外医院
国家心血管中心、中国医学科学院阜外医院原冠心病与心内管委会副主任,血脂异常与心血管病诊断中心主任暨51B病区主任,主任医师,博士研究生导师,国际动脉粥样硬化中国分会常务理事,欧洲和美国心血管病学会会员(FESC/FACC),亚太代谢与心血管疾病联盟理事。 国内外30余种心血管专业杂志副主编、编委,在 Circ Res 、 Diabetes Care 、 Clin Chem 、 ATVB 、 Hypertension 等SCI源期刊发表论文300余篇,影响因子总积分900余分。完成省部级课题20余项,获省部级科技成果奖4项(第一完成人)。 (来源:《国际循环》编辑部) 版 权 声 明 凡原创文章版权属《国际循环》所有。欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有之内容须在醒目位置处注明“转自《国际循环》” 点分享 点收藏 点点赞 点在看返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |