肠癌新辅助治疗如何选择?MMR / MSI检测告诉你! |
您所在的位置:网站首页 › 结肠癌mmr检测 › 肠癌新辅助治疗如何选择?MMR / MSI检测告诉你! |
肠癌新辅助治疗如何选择?MMR / MSI检测告诉你!
|
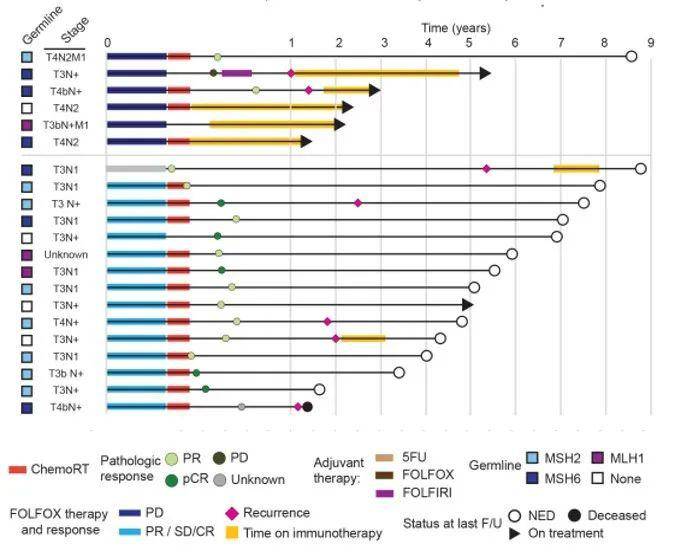
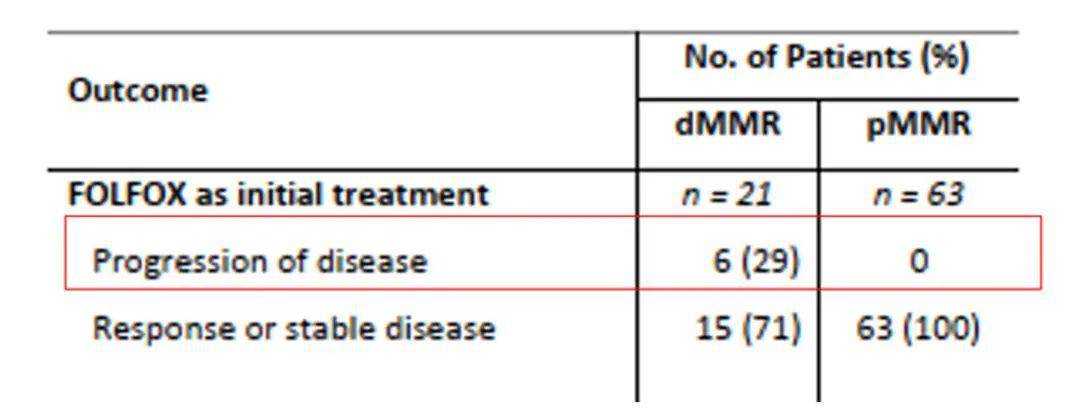
在本研究分析的50例患者中,初始治疗为新辅助化疗的患者有21例,同步放化疗的患者有16例,另有13例患者直接接受了手术。 dMMR/MSI状态显著影响直肠癌新辅助化疗的疗效 21例接受新辅助化疗的 dMMR直肠癌患者 中,有6例(29%)出现疾病进展(PD),其中5例为林奇综合征患者(图1)。在配对的 63例pMMR直肠癌患者中,则 未发现新辅助化疗后PD的现象,患者疾病稳定(SD)/缓解(PR)的比例更高(图2)。
图1. 新辅助化疗dMMR直肠癌患者分期,诊疗过程及结局
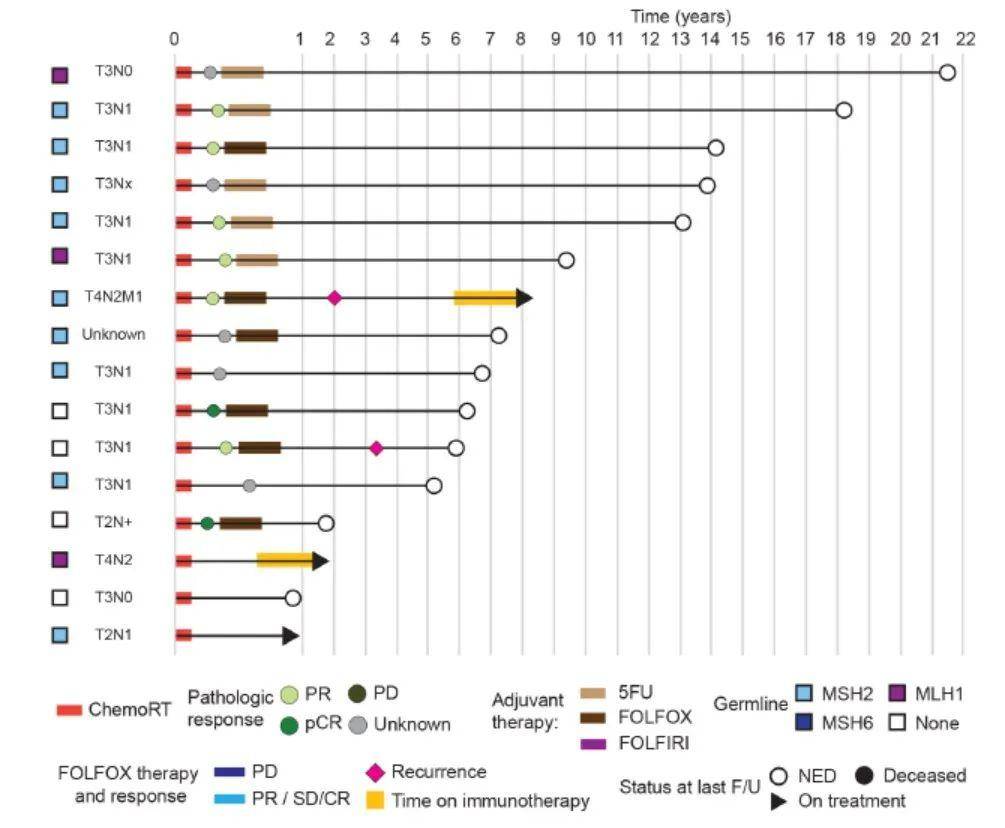
图2. dMMR和pMMR直肠癌患者初始接受新辅助化疗疗效比较 不同MMR状态的患者初始接受放化疗的疗效相似 对于新辅助治疗最初即接受同步放化疗的16例患者, 13例(93%)经历了肿瘤临床分期降低,其中2例(14%)患者达到病理完全缓解(图3)。
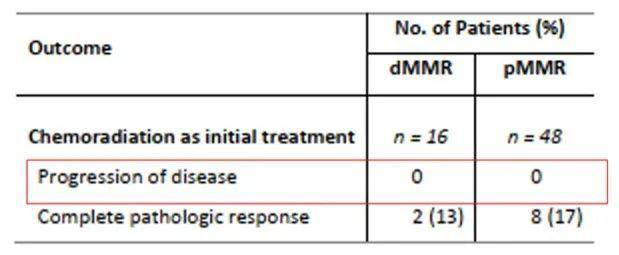
图3. 新辅助同步放化疗dMMR直肠癌患者分期,诊疗过程及结局 与48例配对的pMMR直肠癌患者相比,两组接受同步术前放化疗的患者中, 都没有出现治疗后PD,两组pCR比例相近,术前同步放化疗的获益相似(图4)。 因此对于直肠癌患者,在治疗前通过检测了解肿瘤的dMMR/MSI状态,对于患者治疗策略的制定以及临床获益非常有帮助。
图4. dMMR和pMMR直肠癌患者初始接受新辅助化疗的疗效比较 dMMR结肠癌患者100%可从新辅助免疫治疗中获益 除了新辅助化疗及放化疗外, 将免疫治疗应用于早期肠癌新辅助治疗中也是近期临床上关注的热点。新辅助免疫治疗旨在术前激活患者的免疫系统对肿瘤发生免疫应答,从而提高患者的肿瘤缓解率。 今天第二篇分享的就是来自荷兰的首个关于结肠癌新辅助免疫治疗的临床研究——NICHE研究,其结果于近日发表在 Nature Medicine杂志上, 影响因子30.641。
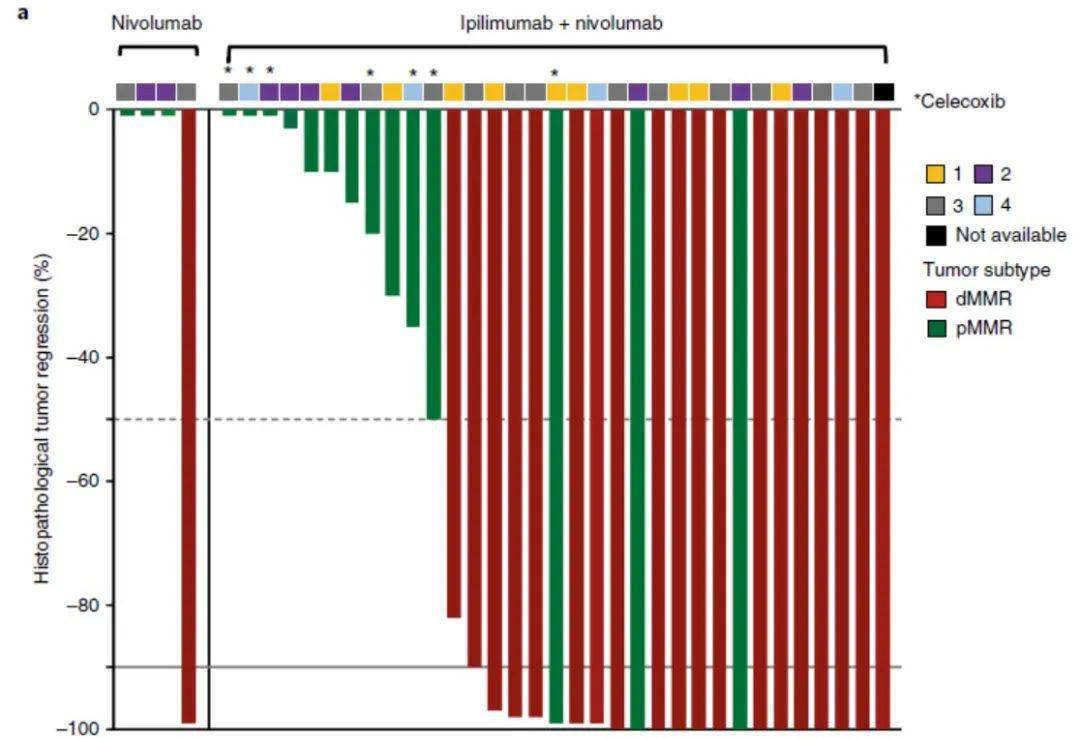
(图片来源:Nature网站) 患者基本信息 本研究 共纳入40例结肠癌患者,其中21例为dMMR,20例为pMMR(其中一例患者同时为pMMR和dMMR型)。81%的dMMR型患者和40%的pMMR型患者为临床III期结肠癌。最终有15例pMMR(7例还接受COX-2抑制剂celecoxib治疗)和20例dMMR患者接受了 伊匹木单抗联合纳武利尤单抗的治疗,并进行了疗效评估。 dMMR结肠癌患者新辅助免疫治疗效果令人激动 研究结果显示, dMMR型结肠癌患者接受新辅助免疫治疗的客观缓解率高达100%,而部分pMMR型(27%)的结肠癌患者也在免疫治疗下产生了良好的 应答[4] 。这一结果提示,无远处转移的结肠癌患者或许可以在等待手术的过程中从短程的免疫治疗中获益,其中 dMMR/MSI的患者可能获益更明显。
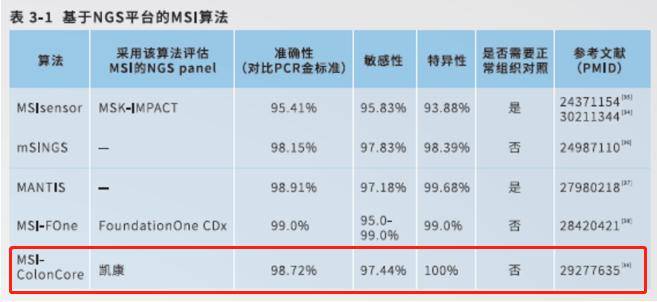
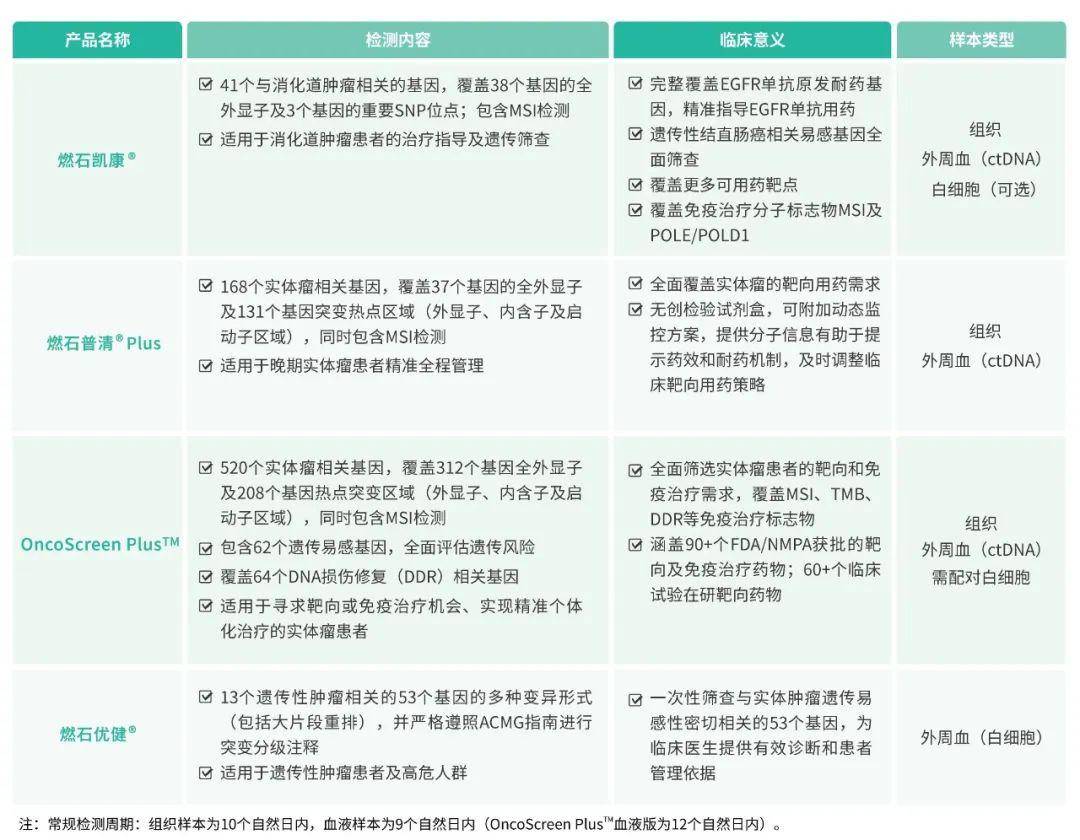
图5. dMMR结肠癌患者新辅助免疫治疗后病理缓解明显 小结与启发 以上两项研究中虽然纳入的总样本量不多,仍然给我们带来了不可思议的结果,提示MMR/MSI状态可能与不同新辅助治疗方式的疗效和选择有相关性,当然未来仍需要更大规模的研究和更长期的随访来证实。 我们有理由相信,无论是直肠癌还是结肠癌,在 初诊时进行肿瘤MMR/MSI状态的检测,对患者治疗方式的选择以及预测预后有着重要的提示和指导意义。 NCCN指南已经推荐使用NGS的方法对MSI进行检测。 NGS相比传统的PCR或IHC方法具有明显的临床应用优势: (1)使用NGS方法进行MSI检测,可 同时对肿瘤进行基因分型以及驱动基因变异的检出,为患者提供更多的治疗选择,并为治疗疗效预测提供坚实的证据;极大提高分子诊断效率,降低样本用量; (2) 经过验证的 NGS检测平台,MSI检测与传统检测方法一致性高,且相比传统方法无需额外准备患者正常组织作为对照,更加经济可行; (3)IHC方法受判读人员的主观影响较大,存在蛋白表达错判可能,而 NGS检测正好可以弥补这一不足,从检测方法学上来讲, 患者可能获益更明显; (4) 外周血循环肿瘤DNA(ctDNA)也可以检测MSI,为肿瘤组织取样困难或不足的晚期实体瘤患者提供MSI检测机会。 在结直肠癌的检测方面,燃石有着丰富的产品线布局—— 燃石凯康 ® 、OncoScreen Plus TM 和燃石普清 ® Plus panel, 均可检测组织或血液中的肿瘤相关基因变异,并且同时覆盖MSI的检测,其中 凯康®的检测结果与传统PCR方法比较的吻合度高达99% [5], 被《微卫星不稳定性(MSI)检测中国专家共识》推荐用于临床MSI检测。
(图片来源:微卫星不稳定(MSI)检测中国专家共识) 燃石医学在血浆ctDNA样本的MSI检测方面也有重大突破。近日,燃石医学“一种微卫星生物标志物组合、检测试剂盒及其用途”产品 获得国家发明专利,这是国家知识产权局发出的 首个用于血浆样本中的微卫星稳定状态(bMSI)检测的发明专利 。相对于组织MSI检测,bMSI的检测具有无创性、实时性、非组织特异性等特征,可以在ctDNA含量很低的血浆样本中完成微卫星状态的检测,从而填补了通过血浆样本检测微卫星状态的空白。 燃石验证数据显示, 燃石bMSI检测方法对ctDNA含量高于0.4%的样本可以达到很高的正确率,检测速度快,不依赖匹配白细胞样本,实现高灵敏度高特异性地判断样本的微卫星稳定性状态,相关文章已于近期在线发表 [6](详情讲解请持续关注燃石微信公众号哦)。目前,燃石产品中 凯康®、OncoScreen Plus TM 和燃石普清 ® Plus panel的血液版均可对bMSI进行检测。
参考文献 [1] M. A. Merok, T. Ahlquist, E. C. Røyrvik, K. F. Tufteland, M. Hektoen, O. H. Sjo, T. Mala, A. Svindland, R. A. Lothe, A. Nesbakken, Ann. Oncol. 2013, DOI 10.1093/annonc/mds614. [2] D. J. Sargent, S. Marsoni, G. Monges, S. N. Thibodeau, R. Labianca, S. R. Hamilton, A. J. French, B. Kabat, N. R. Foster, V. Torri, et al., J. Clin. Oncol. 2010, DOI 10.1200/JCO.2009.27.1825. [3] A. Cercek, G. Dos Santos Fernandes, C. S. Roxburgh, K. Ganesh, S. Ng, F. Sanchez-Vega, R. Yaeger, N. H. Segal, D. L. Reidy-Lagunes, A. M. Varghese, et al., Clin. Cancer Res. 2020, clincanres.3728.2019. [4] M. Chalabi, L. F. Fanchi, K. K. Dijkstra, J. G. Van den Berg, A. G. Aalbers, K. Sikorska, M. Lopez-Yurda, C. Grootscholten, G. L. Beets, P. Snaebjornsson, et al., Nat. Med. 2020, 26, 566–576. [5] L. Zhu, Y. Huang, X. Fang, C. Liu, W. Deng, C. Zhong, J. Xu, D. Xu, Y. Yuan, J. Mol. Diagnostics 2018, DOI 10.1016/j.jmoldx.2017.11.007. [6] Z Cai, Z Wang, C Liu, D Shi, D Li, M Zheng, H Han-Zhang, A Lizaso, J Xiang, et al., J. Mol. Diagnostics 2020, DOI 10.1016/j.jmoldx.2020.04.210返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |