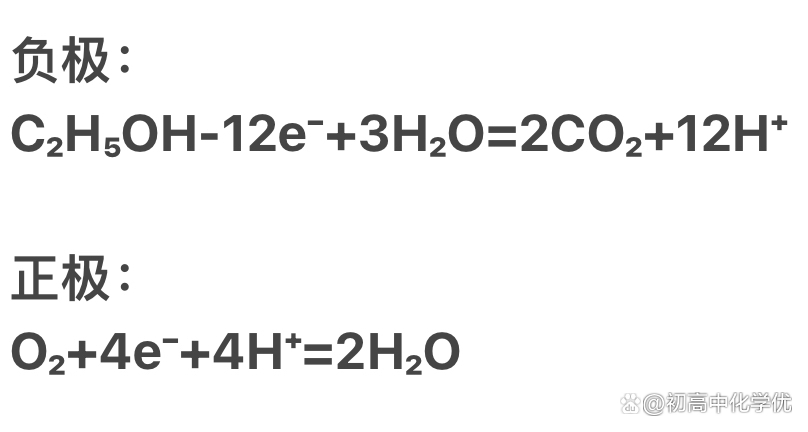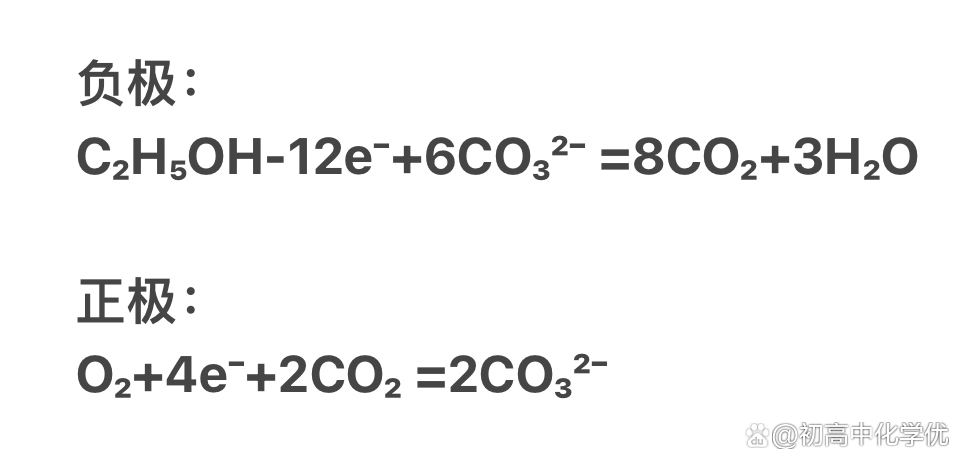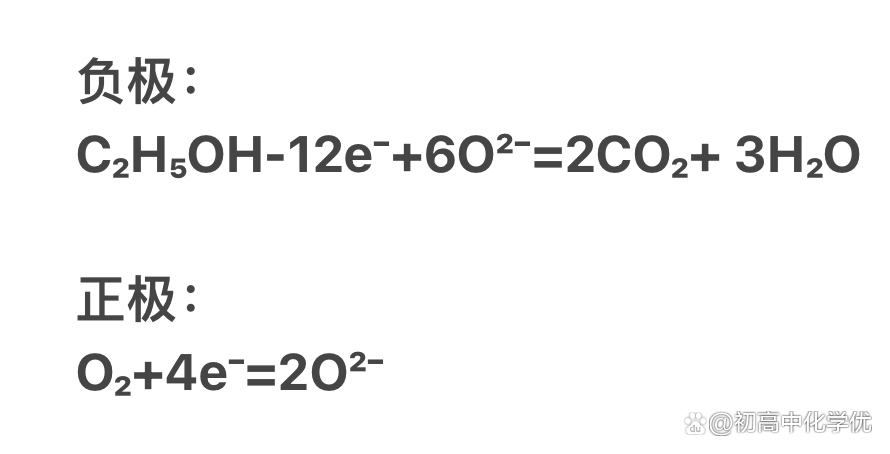高中化学‖电化学 |
您所在的位置:网站首页 › 石材款式 › 高中化学‖电化学 |
高中化学‖电化学
|
高中化学‖电化学_原电池知识点/燃料电池书写
2022-12-07 21:01:14 0原电池知识梳理 1.原电池:把 化学能 转化为 电能 的装置。 2.原电池的形成条件: ①能自发进行的氧化还原反应; ②两个活泼性不同的电极; ③电解质溶液或熔融态离子化合物; ④形成闭合回路。 3.电极 ①正极:化合价降低,得电子,还原反应 ②负极:化合价降低,失电子,氧化反应 4.电流/电子流动方向 ①电流:正极_延外电路到_负极 ②电子:负极_延外电路到_正极 5.溶液中阴阳离子定向移动 ①阳离子向 正极 移动 ②阴离子向 负极 移动
燃料电池的书写 以乙醇燃料电池为例,写出它在四种环境电解质中的电极方程式: 首先,考虑总反应方程式,乙醇在氧气中点燃生成二氧化碳和水。 1.负极: 乙醇中碳的化合价为-2价,生成二氧化碳中碳为+4价,一个碳失了6个电子,有两个碳转移12个电子。 2.正极: 氧气中氧由0价降至-2价,得到2个电子,氧气中两个氧,所以一个氧气分子,得4个电子。 ①酸性水溶液中电极方程式 电荷调平补氢离子/水
②碱性水溶液中的电极方程式: 电荷调平补氢氧根离子和水
③熔融碳酸盐做电解质 用碳酸根调平电荷
④固体电解质(存在氧离子) 用氧离子调平电荷
以上是电化学中原电池的基础知识点,和燃料电池电极方程式的书写,喜欢收藏,分享给需要的人~ 特别声明:本文为人民日报新媒体平台“人民号”作者上传并发布,仅代表作者观点。人民日报提供信息发布平台。 分享到:
0 
写下你的评论 评论 热门评论{{item.content}} 最新评论{{cell.content}} {{item.content}} 已加载全部内容 |
【本文地址】
公司简介
联系我们
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |
 初高中化学迷
初高中化学迷