蛋白质的糖基化修饰(二) |
您所在的位置:网站首页 › 溶酶体中的酶需要高尔基体加工吗 › 蛋白质的糖基化修饰(二) |
蛋白质的糖基化修饰(二)
|
O-糖基化的分类一般根据第一个与肽链相连的糖基进行。人体的O-聚糖有7种主要类型,其中最常见的是粘蛋白型(mucin-type),第一个糖基是N-乙酰半乳糖胺(-GalNAc- 1–Ser / Thr)。
Mucin即粘蛋白,在消化道、呼吸道、生殖道等处分泌粘液中含量丰富。粘蛋白中的大量短链O-聚糖使其溶液具有粘性。例如在胃和肠的粘膜表明都有一层粘蛋白凝胶构成物理屏障,以隔绝消化液对消化道粘膜的降解破坏。
大多数O-糖基化从内质网开始,不过粘蛋白型是在高尔基体开始的。人类的高尔基体中有20种N-乙酰半乳糖胺转移酶(GalNAc-T),彼此功能重叠,但有细微的底物特异性差异。这导致某种酶的缺陷只造成轻微的表型,与其它糖基化酶缺陷的严重后果形成鲜明对比。
引入第一个糖基后,可继续由其它糖基转移酶添加糖基,将糖链延长和分支,形成各种类型的糖链。根据第二个糖基的种类和连接方式,粘蛋白的糖链可进一步分为8种核心结构,具有不同的组织特异性和生理功能。 对粘蛋白来说,添加唾液酸、岩藻糖等是终止信号。例如,ST6GalNAc-1对第一个GalNAc的过早唾液酸化会导致癌症相关结构STn。
O连接的半乳糖主要出现在胶原蛋白中,连接在羟赖氨酸上。赖氨酰羟化酶(EC1.14.11.4)催化-X-Lys-Gly-序列中赖氨酸的羟化,反应需要二价铁离子、α-酮戊二酸、O2和抗坏血酸。 胶原蛋白螺旋结构域中的一些羟赖氨酸可以进行O-糖基化,产生G-Hyl(半乳糖基羟赖氨酸)和GG-Hyl(葡糖基半乳糖基羟赖氨酸)。这些反应分别由GT(EC 2.4.1.50)和GGT(EC 2.4.1.66)催化,以UDP活化的单糖为供体。这些反应都发生在内质网,在胶原三股螺旋形成之前。这与粘蛋白正好是两个极端。
羟赖氨酸的糖基化与骨骼钙化有关,糖基化缺陷可导致成骨不全、骨质疏松等疾病。此外还有人认为糖基化与胶原的交联、重塑、胶原-细胞相互作用等生物过程相关。胶原糖基化的具体情况在不同组织及生理、病理情况下变动很大,还有很多机制尚未阐明。 更为重要的是O-GlcNAc修饰,参与多种代谢和基因表达调控,与多种重要生理过程相关。这方面内容将在下一篇文章中介绍。 参考文献: 1. Mitsuo Yamauchi, et al. Lysine post-translational modifications of collagen. Essays Biochem. 2012; 52: 113–133. 2. Pamela Stanley. Golgi Glycosylation. Cold Spring Harb Perspect Biol. 2011 Apr; 3(4): a005199. 3. Eric P Bennett, et al. Control of mucin-type O-glycosylation: A classification of the polypeptide GalNAc-transferase gene family. Glycobiology. 2012 Jun; 22(6): 736–756. 4. Anthony Corfield. Eukaryotic protein glycosylation: a primer for histochemists and cell biologists. Histochem Cell Biol. 2017; 147(2): 119–147.返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |
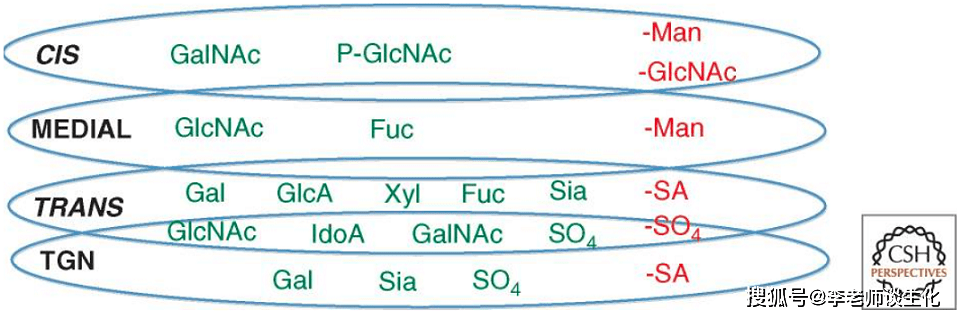 高尔基体各区室的糖基转移酶和糖苷酶。Cold Spring Harb Perspect Biol. 2011 Apr
高尔基体各区室的糖基转移酶和糖苷酶。Cold Spring Harb Perspect Biol. 2011 Apr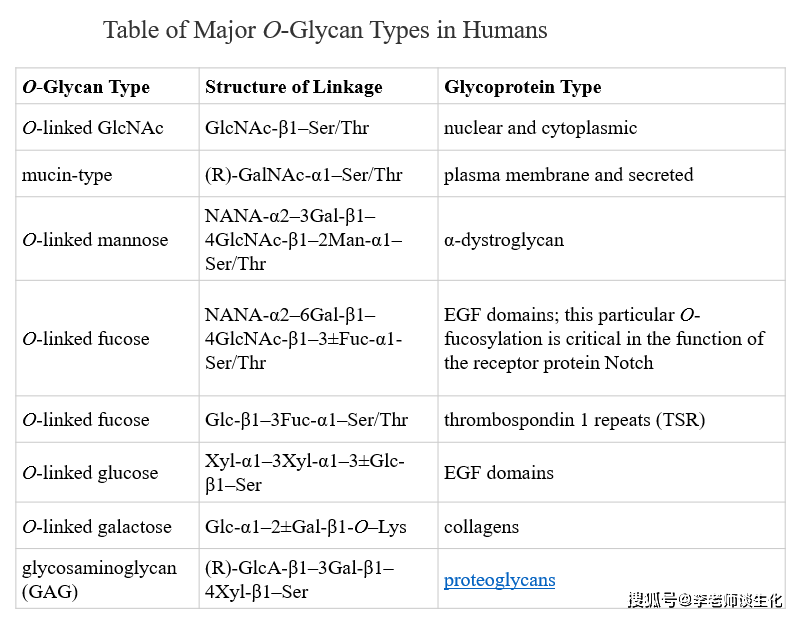 人体主要O-聚糖类型。Themedicalbiochemistrypage
人体主要O-聚糖类型。Themedicalbiochemistrypage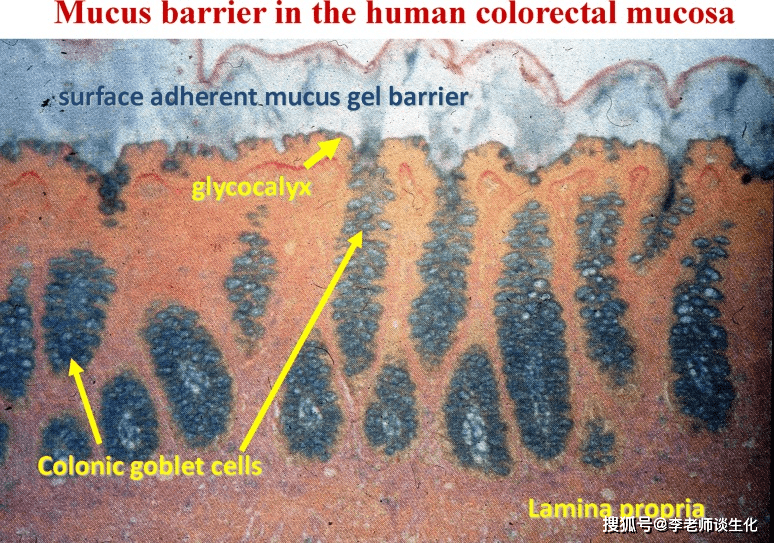 肠粘膜的组织化学染色,显示粘蛋白的屏障作用。Histochem Cell Biol. 2017; 147(2)
肠粘膜的组织化学染色,显示粘蛋白的屏障作用。Histochem Cell Biol. 2017; 147(2)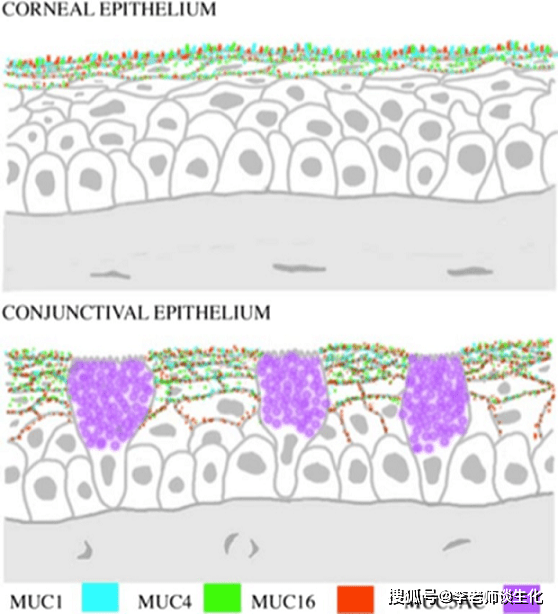 粘蛋白在人角膜和结膜中的表达。Histochem Cell Biol. 2017; 147(2): 119–147.
粘蛋白在人角膜和结膜中的表达。Histochem Cell Biol. 2017; 147(2): 119–147.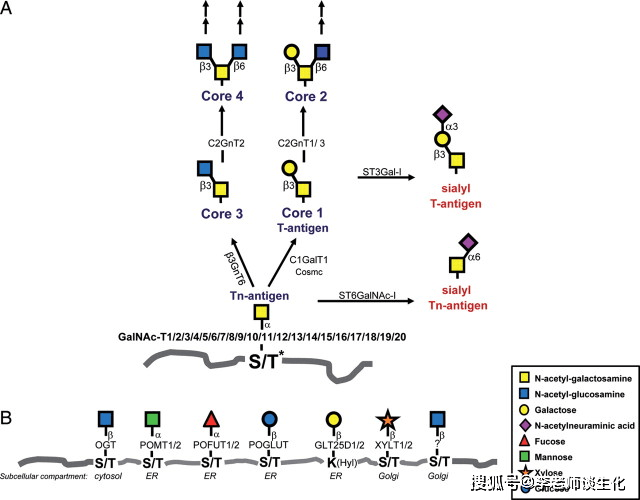 哺乳动物蛋白O-糖基化途径。Glycobiology. 2012 Jun; 22(6): 736–756.
哺乳动物蛋白O-糖基化途径。Glycobiology. 2012 Jun; 22(6): 736–756.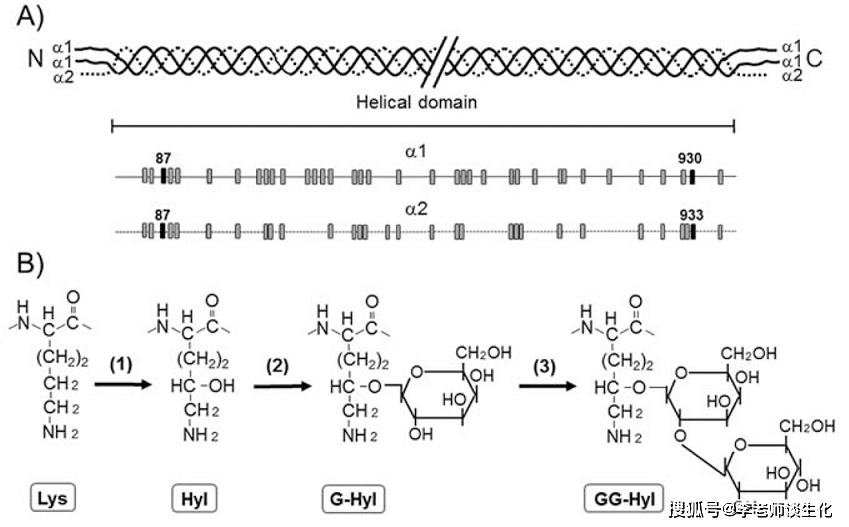 人I型胶原螺旋结构域中Lys的分布和糖基化。Essays Biochem. 2012; 52: 113–133.
人I型胶原螺旋结构域中Lys的分布和糖基化。Essays Biochem. 2012; 52: 113–133.