肼(N2H4)为二元弱碱,在水中的电离方式与NH3相似。25℃时,水合肼(N2H4·H2O... |
您所在的位置:网站首页 › 小学一年级小组名字及口号 › 肼(N2H4)为二元弱碱,在水中的电离方式与NH3相似。25℃时,水合肼(N2H4·H2O... |
肼(N2H4)为二元弱碱,在水中的电离方式与NH3相似。25℃时,水合肼(N2H4·H2O...
|
肼(N2H4)为二元弱碱,在水中的电离方式与NH3相似。25℃时,水合肼(N2H4·H2O)的电离常数K1、K2依次为9.55×10-7、1.26×10-15。下列推测或叙述一定错误的是 A.N2H4易溶于水和乙醇 B.N2H4分子中所有原子处于同一平面 C.N2H6Cl2溶液中:2c(N2H D.25°C时,反应H++N2H4⇌N2H 高二化学多选题中等难度题查看答案及解析 联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。 I、(1)联氨分子的电子式为______________, (2)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的方程式_______________。联氨与盐酸反应生成的正盐的化学方程式为__________________ II、某探究小组利用下列反应制取水合肼(N2H4·H2O):CO(NH2)2+2NaOH+NaClO===Na2CO3+N2H4·H2O+NaCl
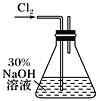
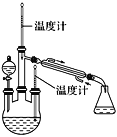
实验一:制备NaClO溶液(实验装置如上图所示) (1)配制30%NaOH溶液时,所需的玻璃仪器除量筒外,还有________(填标号)。 A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒 实验二:制取水合肼(实验装置如右图所示)。
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114 ℃馏分。(已知:N2H4·H2O+2NaClO===N2↑+3H2O+2NaCl) (2)分液漏斗中的溶液是________(填标号)。 A.CO(NH2)2溶液 B.NaOH和NaClO混合溶液 选择的理由是__________________________________________________ 实验三:测定馏分中水合肼的含量。 称取馏分5.000 g,加入适量NaHCO3固体,加水配成250 mL溶液,移取25.00 mL,用0.100 0 mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5 左右。(已知:N2H4·H2O+2I2===N2↑+4HI+H2O) (3)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是_____________________。 (4)本实验用____________做指示剂,当滴定达到终点时的现象为_____________________。 (5)实验测得消耗I2溶液的平均值为18.00 mL,馏分中水合肼(N2H4·H2O)的质量分数为________。 高二化学填空题中等难度题查看答案及解析 联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。 (1)联氨分子的电子式为______________, (2)联氨为二元弱碱,在水中的电离方式与氨相似。写出在水中联氨第一步电离反应的方程式______________________________________________________。 (3)已知12.8 g的液态高能燃料联氨在氧气中燃烧,生成气态N2和液态水,放出248.8kJ的热量。写出表示液态联氨燃烧热的热化学方程式___________________。 (4)已知①2O2(g)+N2(g)=N2O4(l) ;ΔH1 ②N2(g)+2H2(g)=N2H4(l) ;ΔH2 ③O2(g)+2H2(g)=2H2O(g) ; ΔH3 ④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ;ΔH4 上述反应热效应之间的关系式为ΔH4=_________________,联氨和N2O4可作为火箭推进剂的主要原因为____________________________________________ (至少答2点)。 高二化学综合题简单题查看答案及解析 氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题: (1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因 。 (2)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s)
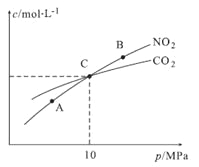
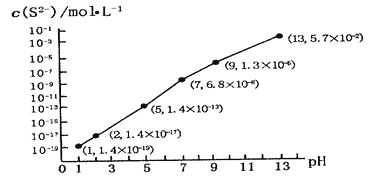
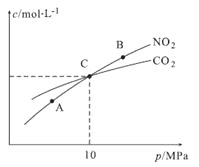
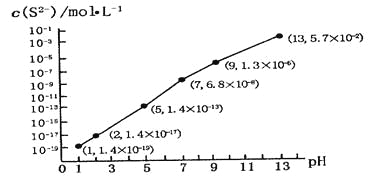
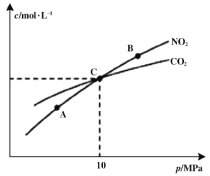
①A、B两点的浓度平衡常数关系:Kc(A) Kc(B)(填“<”或“>”或“=”)。 ②A、B、C三点中NO2的转化率最高的是 (填“A”或“B”或“C”)点。 ③计算C点时该反应的压强平衡常数Kp= (列出表达式并计算结果。Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。 (3)亚硝酸的电离平衡常数Ka=5.1×10-4(298K)。它的性质和硝酸很类似。 ①已知298K 时,H2CO₃的Ka1=4.2×10-7;Ka2=5.61×10-11。向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小是 。 ②将10mL0.1mol/L的亚硝酸溶液加入到10mL0.1mol/L氨水(已知在25℃时,一水合氨的Ki= 1.8×10-5)中,最后所得溶液为________(填“酸性”、“碱性”或者“中性”)。 (4)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下: ①CaSO4(s)+CO(g) ②CaSO4(s)+ 4CO(g) 反应CaO(s)+3CO(g)+SO2(g) (5)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通人HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。 ①pH=13时,溶液中的c(H2S)+c(HS-)=__________mol·L-1; ②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=______时,Fe2+开始沉淀。(已知:KSP(FeS)=1.4×10-19) 高二化学综合题中等难度题查看答案及解析 氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题: (1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因 。 (2)在恒温条件下,1 mol NO2和足量C发生反应:2NO2(g)+2C(s)
①A、B两点的浓度平衡常数关系:Kc(A) Kc(B)(填“<”或“>”或“=”)。 ②A、B、C三点中NO2的转化率最高的是 (填“A”或“B”或“C”)点。 ③计算C点时该反应的压强平衡常数Kp= (列出表达式并计算结果。Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。 (3)亚硝酸的电离平衡常数Ka=5.1×10-4(298K)。它的性质和硝酸很类似。 ①已知298K 时,H2CO₃的Ka1=4.2×10-7;Ka2=5.61×10-11。向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小是 。 ②将10mL0.1mol/L的亚硝酸溶液加入到10mL0.1mol/L氨水(已知在25℃时,一水合氨的Ki= 1.8×10-5)中,最后所得溶液为________(填“酸性”、“碱性”或者“中性”)。 (4)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下: ①CaSO4(s)+CO(g) ②CaSO4(s)+ 4CO(g) 反应CaO(s)+3CO(g)+SO2(g) (5)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol·L-1H2S溶液中,通人HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。 ①pH=13时,溶液中的c(H2S)+c(HS-)=__________mol·L-1; ②某溶液含0.010 mol·L-1Fe2+和0.10 mol·L-1H2S,当溶液pH=______时,Fe2+开始沉淀。(已知:KSP(FeS)=1.4×10-19) 高二化学综合题中等难度题查看答案及解析 氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题: (1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因是:____________________________________________。 (2)在恒温条件下,1 mol NO2和足量C发生反应2NO2(g)+2C(s)
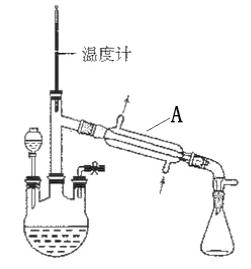
①A、B两点的浓度平衡常数关系:Kc(A) ___________Kc(B)(填“”或“=”) ②A、B、C三点中NO2的转化率最高的是___________(填“A”或“B”或“C”)点。 ③计算C点时该反应的压强平衡常数Kp=___________MPa(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。 (3)已知:亚硝酸(HNO2)性质和硝酸类似,但它是一种弱酸。常温下亚硝酸的电离平衡常数Ka=5.1×10-4;H2CO3的Ka1=4.2×10-7,Ka2=5.61×10-11。在常温下向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小的顺序是______________________。 (4)已知:常温下甲胺(CH3NH2)的电离常数为Kb,且pKb=-lgKb=3.4水溶液中有CH3NH2+H2O⇌CH3NH3++OH-。常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,则溶液pH=_______。 (5)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下: ①CaSO4(s)+CO(g) ⇌CaO(s)+SO2(g)+CO2(g) △H=+210.5kJ· mol-1 ②CaSO4(s)+4CO(g) ⇌CaS(s)+ 4CO2(g) △H=-189.2 kJ· mol-1 反应CaO(s)+3CO(g)+SO2(g) ⇌CaS(s)+3CO2(g) △H=___________ kJ· mol-1 高二化学综合题中等难度题查看答案及解析 已知25℃时有关弱酸(或弱碱)的电离平衡常数: 弱酸(或弱碱)化学式 CH3COOH NH3·H2O H2CO3 电离平衡常数(25℃) 1.8×l0–5 1.8×l0–5 K1=4.3×l0–7 K2=5.6×l0–11 在25℃时,下列有关电解质溶液的说法不正确的是( ) A. pH相等的四种溶液:a.CH3COONa b.Na2CO3 c.NaHCO3 d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d < b < c < a B. 0.1mol·L-1的NaHCO3溶液:c(Na+) > c(HCO3-) > c(CO32-)> c(H2CO3) C. 1 L 0.50 mol·L-1NH4Cl 溶液与2 L 0.25 mol·L-1NH4Cl 溶液,前者含NH4+ 物质的量多 D. 浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液中:c(CH3COO-)+c(OH-) > c(CH3COOH)+c(H+) 高二化学单选题困难题查看答案及解析 已知25℃时有关弱酸(或弱碱)的电离平衡常数: 弱酸(或弱碱)化学式 CH3COOH NH3·H2O H2CO3 电离平衡常数(25℃) 1.8×l0–5 1.8×l0–5 K1=4.3×l0–7 K2=5.6×l0–11 在25℃时,下列有关电解质溶液的说法不正确的是( ) A.pH相等的四种溶液:a.CH3COONa b.Na2CO3 c.NaHCO3 d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d < b < c < a B.0.1mol·L-1的NaHCO3溶液:c(Na+) > c(HCO3-) > c(CO32-)> c(H2CO3) C.1 L 0.50 mol·L-1NH4Cl 溶液与2 L 0.25 mol·L-1NH4Cl 溶液,前者含NH4+ 物质的量多 D.浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液中:c(CH3COO-)+c(OH-) > c(CH3COOH)+c(H+) 高二化学单选题困难题查看答案及解析 水合肼(N2H4·H2O) 是一种强还原剂,沸点118.5℃,熔点-40℃,常温下为无色透明的油状液体,属于二元弱碱,在空气中可吸收CO2而产生烟雾。水合肼的制备装置如图。
(1)装置A的名称为________________。向三颈烧瓶中加入溶液之前,应先从右侧导管中通入氮气,目的是______________________。 (2)水合肼可用含NaOH 的NaClO溶液氧化尿素[CO(NH2)2]溶液制得,反应的化学方程式为__________________。 (3)制备水合肼时,分液漏斗应盛装________(填标号)。理由是___________。 a.NaOH 和NaClO 混合溶液 b.CO(NH2)2 溶液 (4)弱酸性条件下水合肼可处理电镀废水,将Cr2O72-还原为Cr(OH)3沉淀而除去,水合肼被氧化为N2,该反应的离子方程式为_____________。常温下Ksp[Cr(OH)3]= 10-32,且当溶液中离子浓度小于10-5mol/L时可视作沉淀完全。则Cr3+沉淀完全时,溶液的pH=________。 (5)有同学认为该实验收集装置有缺陷。请你写出改进措施:______________。 高二化学实验题中等难度题查看答案及解析 氨分子中的一个氢原子被甲基取代后,所得甲胺(CH3NH2)的性质与氨相似,CH3NH2·H2O也是一元弱碱,25℃时电离常数Kb=4.0×10-5。现用0.0500mol/L的稀硫酸滴定l0mL 0.1000mol/L的甲胺溶液,溶液中c(OH-)的负对数(pOH)与所加稀硫酸的体积(V)的关系如图所示。下列说法正确的是
A. 甲胺在水中的电离方程式为:CH3NH2·H2O=CH3NH3++OH-,因此溶液呈碱性 B. C点所在溶液中 C. A、B、C、D四点溶液中,水电离出来的c(H+):C > D > B > A D. B点溶液中存在c(CH3NH2·H2O)>c(CH3NH3+)>c(H+)>c(OH-) 高二化学选择题困难题查看答案及解析 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |