复旦大学文波AS:组蛋白去甲基化酶KDM7A调控神经元中即早基因 |
您所在的位置:网站首页 › 去甲基化治疗几个疗程见效 › 复旦大学文波AS:组蛋白去甲基化酶KDM7A调控神经元中即早基因 |
复旦大学文波AS:组蛋白去甲基化酶KDM7A调控神经元中即早基因
|
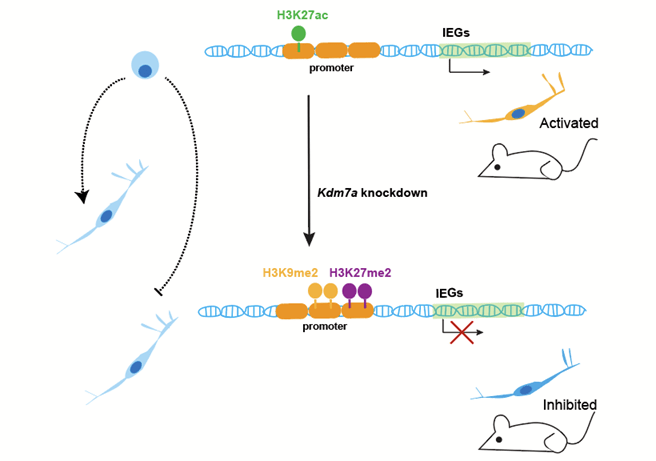
摘要:复旦大学文波课题组通过CUT&Tag-seq、RNA-seq以及小鼠模型对神经元细胞中KDM7A的功能进行了研究。N2A细胞中Kdm7a的敲低导致转录起始位点附近组蛋白修饰的改变和大量基因的表达变化。其中,维持神经系统的功能并与神经系统疾病相关的早期即刻基因,在Kdm7a敲低后显着降低。此外,通过AAV敲低小鼠海马齿状回神经元中的Kdm7a,导致 c-Fos的表达显着降低,从而导致小鼠情绪和记忆受损。该研究表明KDM7A通过调节即早基因影响神经元功能,这为理解神经系统疾病的表观遗传机制提供了新的线索。 关键词:组蛋白去甲基化酶、KDM7A、组蛋白修饰、早期即刻基因
组蛋白修饰的失调与癌症的发生发展、发育缺陷以及一些其它疾病有关,因此,对组蛋白修饰的研究已经越来越受到重视。多种组蛋白修饰在衰老以及神经系统疾病如阿尔茨海默症、亨廷顿症和帕金森症发生发展过程中的水平发生了变化,提示组蛋白的表观遗传修饰在这些生物学过程中的重要作用。这为利用药物或基因工具对大脑中的表观遗传修饰进行干预提供了可能。长期以来,组蛋白脱乙酰酶(HDAC)被认为是治疗神经退行性疾病的潜在靶标。由于目前大多数表观遗传疗法都集中在靶向组蛋白乙酰化蛋白,因此迫切需要找到新的表观遗传靶点。 KDM7A作为一个重要的去甲基化酶,已知其主要负责去除的H3K9me1/2、H3K27me1/2组蛋白修饰在基因组中分布广泛。研究者发现KDM7A在不同的小鼠组织中均有表达,包括大脑,提示其可能与哺乳动物的大脑功能有关。在这项研究中,研究者通过Cut&Tag-seq和ChIP-seq实验首次发现内源的KDM7A主要结合在基因的启动子区域,相较于KDM7A结合在基因其它位置或者没有结合的基因,有KDM7A结合在启动子的基因整体呈现出较高的转录水平。KDM7A作为组蛋白去甲基化酶调控了数千个基因启动子区域的H3K9me2和H3K27me2,并可能与转录因子合作调节关键即早基因(例如Egr1和Atf3)的表达。同时,敲低Kdm7a还会使得抑制性组蛋白修饰H3K9me3在启动子区域增加,而启动子区域活性组蛋白修饰H3K27ac减少,这些结果提示了KDM7A调控基因表达机制的复杂性。 该研究的体内实验发现,通过AAV敲低小鼠海马齿状回神经元中的Kdm7a,同样导致即早基因的表达显着降低。即早基因的失调影响了小鼠的神经元活动,从而导致情绪和记忆障碍。即早基因对于神经元的增殖、分化、突起的形成以及神经环路相关蛋白的形成十分重要。即早基因参与维持神经系统正常功能,在一些神经系统疾病如抑郁症、精神分裂症中已经发现即早基因表达的失常。 展开全文总而言之,该研究探讨了KDM7A在哺乳动物神经系统中的作用,部分阐明了KDM7A的相关调控机制,为神经系统疾病研究以及利用表观遗传手段治疗神经系统疾病的提供了可能的新思路。 复旦大学文波课题组长期致力于表观遗传学和三维基因组研究,本项成果不仅拓展了目前对神经系统中表观遗传修饰的认知,也为神经系统疾病治疗引入了新的思路。博士研究生王轶凡、福建省立医院副研究员洪琴为本文的共同第一作者,文波教授和张朝青年研究员为该文的通讯作者。 WILEY 论文信息: The Lysine Demethylase KDM7A Regulates Immediate Early Genes in Neurons Yifan Wang, Qin Hong, Yueyue Xia, Zhao Zhang*, and Bo Wen* Advanced Science DOI: 10.1002/advs.202301367 Advanced Science 期刊简介 Advanced Science 是Wiley旗下创刊于2014年的优质开源期刊,发表材料科学、物理化学、生物医药、工程等各领域的创新成果与前沿进展。期刊为致力于最大程度地向公众传播科研成果,所有文章均可免费获取。被Medline收录,PubMed可查。最新影响因子为17.521,中科院2021年SCI期刊分区材料科学大类Q1区、工程技术大类Q1区。 AdvancedScienceNews Wiley旗下科研资讯官方微信平台 分享前沿资讯|聚焦科研动态 发表科研新闻或申请信息分享,请联系:[email protected]返回搜狐,查看更多 责任编辑: |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |