Grignard反应(格氏反应) |
您所在的位置:网站首页 › 卤代烃生成 › Grignard反应(格氏反应) |
Grignard反应(格氏反应)
|
通常情况下,当卤代化合物不太活泼时,也可以用活性较高的格式试剂通过交换来制备。
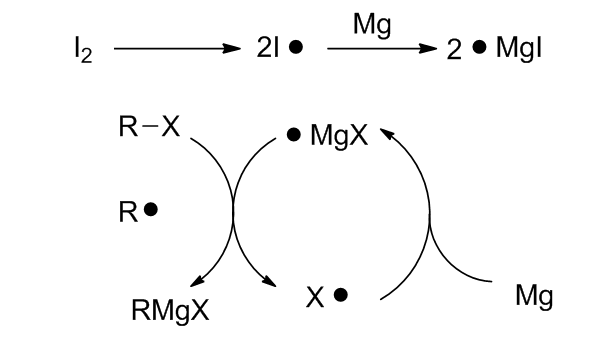
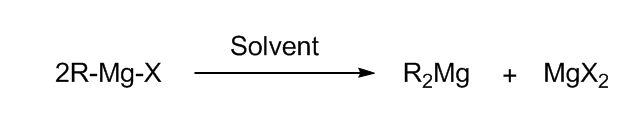
在格氏试剂制备的过程中,无水是最重要的反应条件,否则会使生成的格氏试剂水解而失活,所以要用无水溶剂,反应体系应该用惰性气体保护。镁的使用也要注意。一般采用纯Mg条或者镁屑以减少副反应的发生,纯度低的Mg会降低格氏试剂的产率长期放置的镁条要先用稀盐酸除去表面的氧化膜,然后依次用乙醇与乙醚洗涤后干燥,用量一般为过量5%-10%。格氏试剂也可以与氧气、CO2反应,所以也应该避免。 格氏反应中常见的副反应:一、制备格氏试剂时,生成的试剂会和卤代物进行Wurtz反应 进行偶联(减慢滴加卤代物的速度,控制温度不要太高);二、格氏反应中无水无氧条件不严格时,会和水反应生成烷烃,和氧气反应生成烷氧化物;三、羰基化合物含有α-H时,底物会进行烯醇化;四、含有β-H的格氏试剂和位阻较大的羰基化合物进行反应时,有可能发生分子间的氢转移,将羰基化合物还原。 在反应液中格氏试剂不只是以RMgX的形式单独存在,而是R:Mg,MgX ,(RMgx)n等多种物质的混合物,各物质在溶液中存在动态平衡。通常情况下,大部分的格氏试剂在溶剂中以四面体和三角双锥分子结的形式存在。
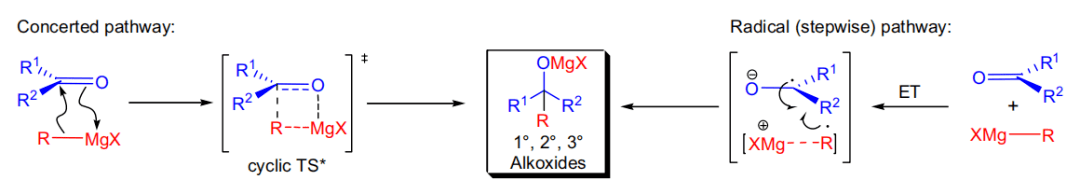
格氏试剂的制备机理是通过单电子转移(SET)过程实现的,反应是在镁金属表面实现的。格氏试剂和羰基化合物的反应,可能是通过两种机理实现:协同反应机理和自由基单电子转移机理。低电子亲核力的底物和格氏试剂反应是通常是经过环状过渡态进行协同反应机理进行。空间位阻较大的底物和大位阻格氏试剂(CMg键较弱)更倾向于进行自由基机理,格氏试剂向底物进行电子转移引发反应。
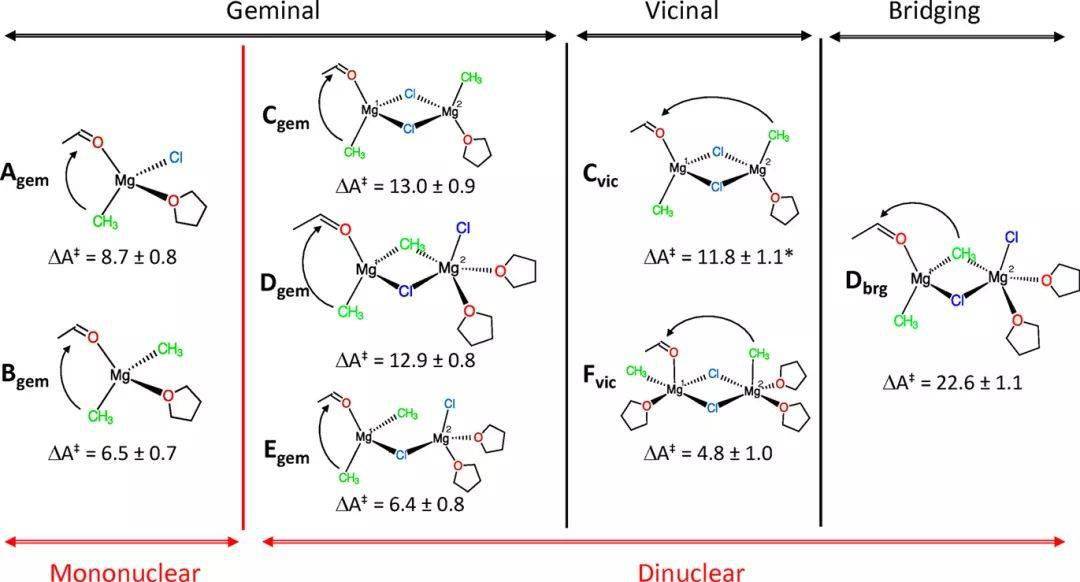
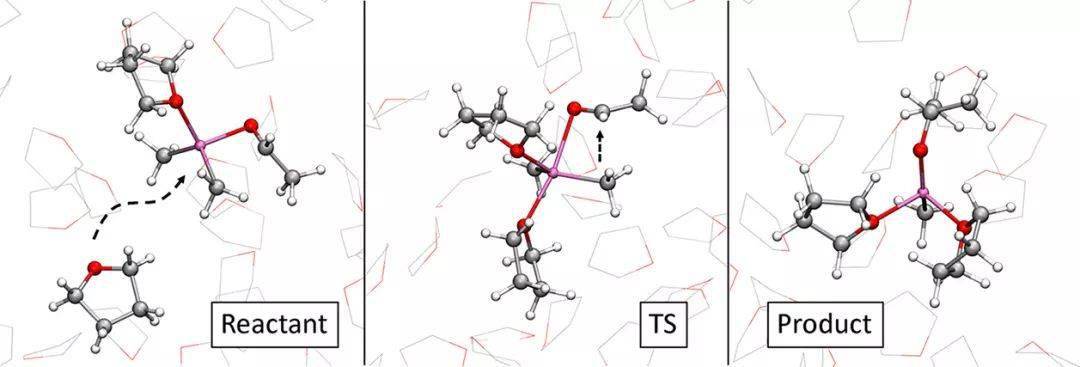
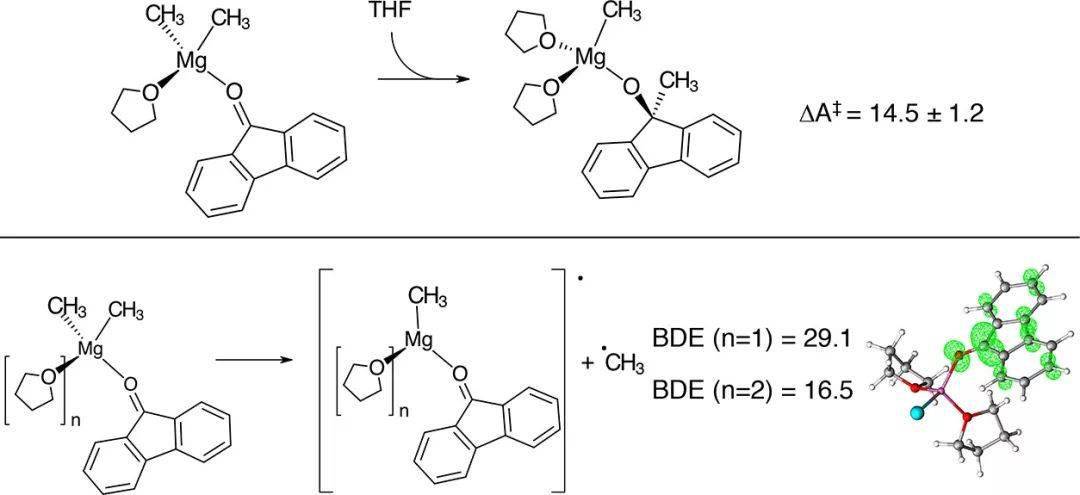
近期,挪威奥斯陆大学的Odile Eisenstein教授和Michele Cascella教授合作,使用量子化学计算和从头算的分子动力学模拟研究了四氢呋喃中的甲基格氏试剂(CH3MgCl)与乙醛和芴酮的加成反应。发现溶剂THF也作为底物参与了反应,对于反应的进行起到至关重要的作用【 J. Am. Chem. Soc. 2020, 142, 2984–2994】。
图3. 化合物B gem的偕位反应过程。 镁为淡紫色,氧为红色,碳为灰色,氢为白色。 格氏试剂的纯溶液中无法形成烷基自由基。当格氏试剂与底物配合后,其解离能降低,降低的程度受到底物结构的影响。还原电位越低的底物,解离能越低。具有较低π*(CO)轨道的底物在与Mg中心配位时,可以稳定Mg-CH3键发生均裂所产生的自由基。同时,该种底物的取代基通常较为庞大,不利于亲核反应途径。稳定自由基的电子效应与阻碍亲核加成的空间效应相结合,解释了仅在还原电位低的底物(如芴酮)存在下才能检测到自由基机理的原因。
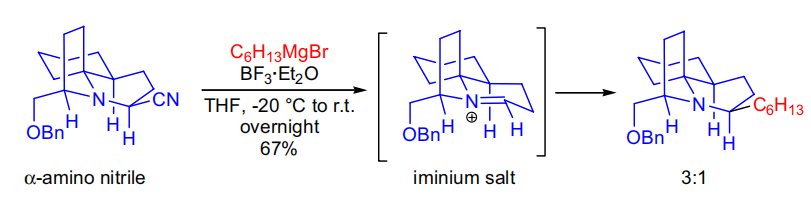
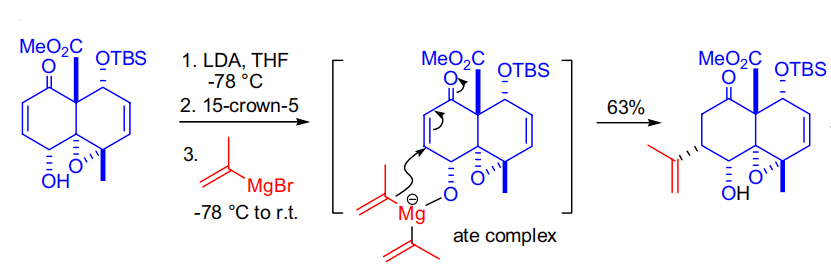
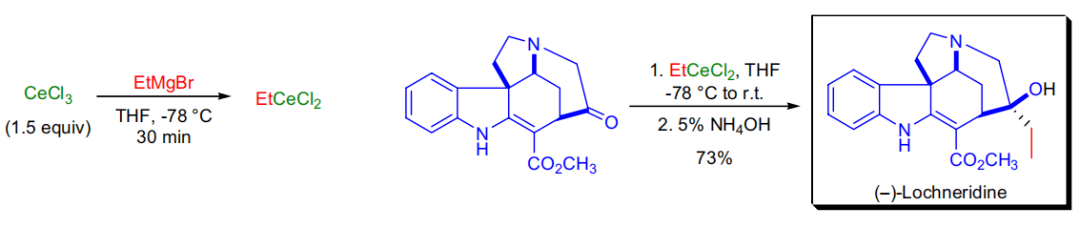
常见反应
【 J. Org. Chem. 2002, 67, 4337-4345】
【 J. Am. Chem. Soc. 1997, 119, 2404-2419】
【 J. Org. Chem. 1998, 63, 9434-9439】
【 J. Am. Chem. Soc. 1996, 118, 10412-10422】
Hoch–Campbell aziridine synthesis 【 Heterocycles 1978, 11, 235-242】
【 Tetrahedron Lett. 2008, 50, 66-67】
【 Synlett 2008, 405-409】
【 Org. Lett. 2013, 15, 286-289】 参考资料 一、Strategic Applications of Named Reactions in Organic Synthesis, LászlóKürti and Barbara Czakó, Grignard reaction , page 188-189。 二、 Name Reactions (A Collection of Detailed Reaction Mechanisms), Jie Jack Li, Grignard reaction,page 291-292。 三、cheminfographic Schlenk技术及无水无氧操作中物料的转移 返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |