热点还不卷,冷门还有文章的方向:内质网应激 |
您所在的位置:网站首页 › 内质网的应激反应 › 热点还不卷,冷门还有文章的方向:内质网应激 |
热点还不卷,冷门还有文章的方向:内质网应激
|
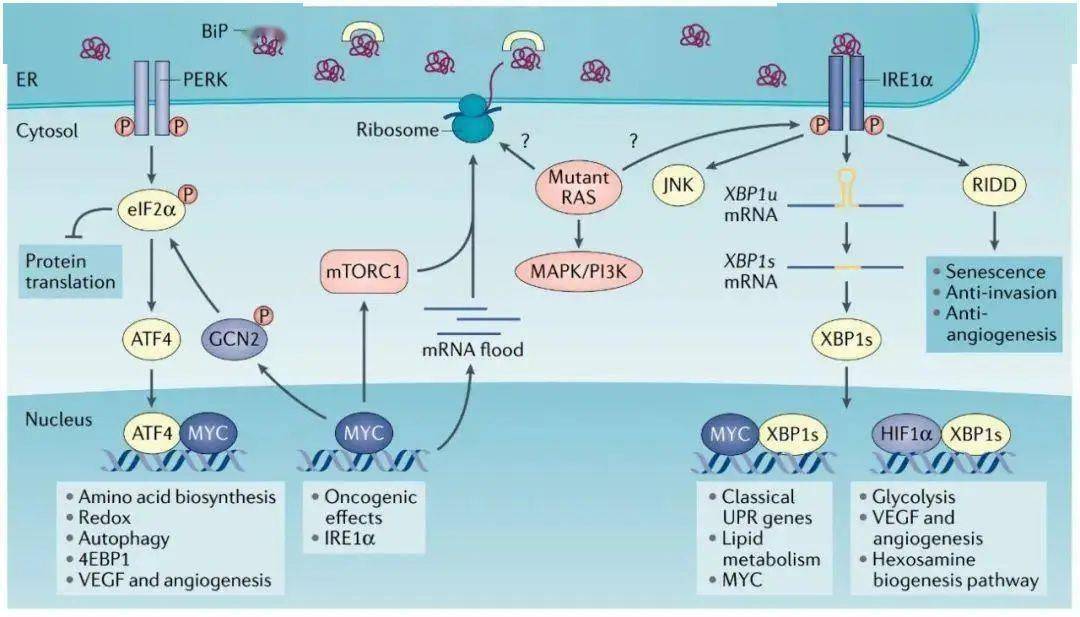
肿瘤细胞中致癌程序和内质网应激反应的整合 致癌MYC通过多种机制激活UPR:MYC诱导的全局转录和翻译的上调增加了内质网中的核糖体生物合成和蛋白质负载,从而激活了UPR的所有分支;MYC还可以与激活的转录因子4(ATF4)相互作用以调节氨基酸转运蛋白和生物合成、抗氧化途径和自噬;MYC还可以与细胞核中的X-box结合蛋白1s(XBP1s)形成异源二聚体,调节经典的UPR基因和脂质代谢基因。mTOR复合物1(mTORC1)激活诱导蛋白质合成和ER超载,从而激活UPR。RAS突变以context-specific方式整合UPR过程。
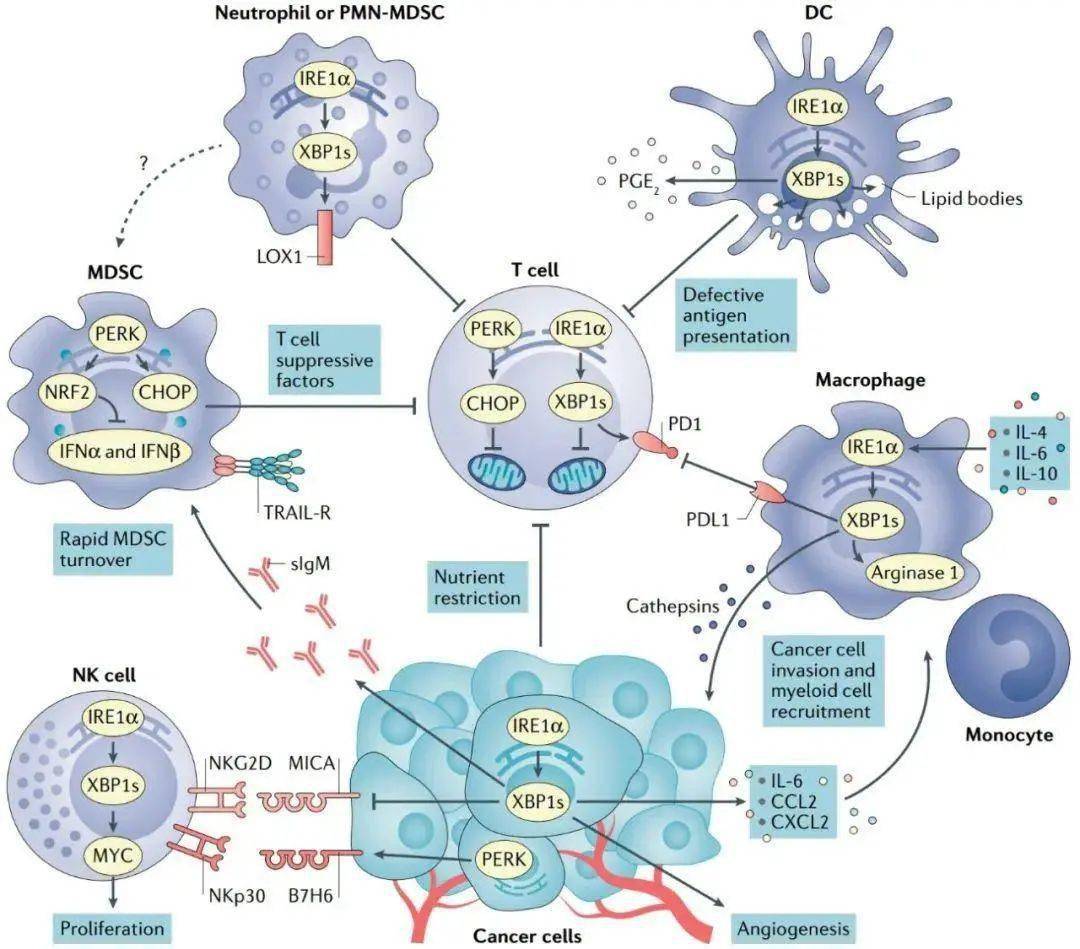
癌内免疫细胞UPR反应 癌细胞在肌醇需要蛋白1α(IRE1α)或PRKR样ER激酶(PERK)激活下调节 自然杀伤细胞(NK)对肿瘤细胞的识别,同时分泌能促进血管生成和髓样细胞类型募集到肿瘤部位的介质。IRE1α和PERK都可以很好地调节血管生成。 髓源性抑制细胞(MDSCs)利用PERK来控制抗肿瘤免疫,MDSC中的内质网应激也与肿瘤坏死因子相关的凋亡诱导配体受体(TRAIL-Rs)的表达升高和TME中的快速周转有关。 内质网应激的中性粒细胞获得免疫抑制特性并通过IRE1α激活过度表达LOX1。ROS积累会促进 肿瘤相关树突细胞(DC)中的ER和持续的IRE1α–XBP1激活,而抑制它们将局部抗原呈递给肿瘤内T细胞的能力。已经证明通过IRE1α-XBP1激活过度产生免疫抑制脂质介质PGE2,可能有助于癌症中的免疫逃逸。在 巨噬细胞中,IRE1α–XBP1分支已被证明可促进组织蛋白酶、PD1配体1(PDL1)和精氨酸酶1的表达,进一步促进TME中的癌细胞侵袭和免疫抑制。
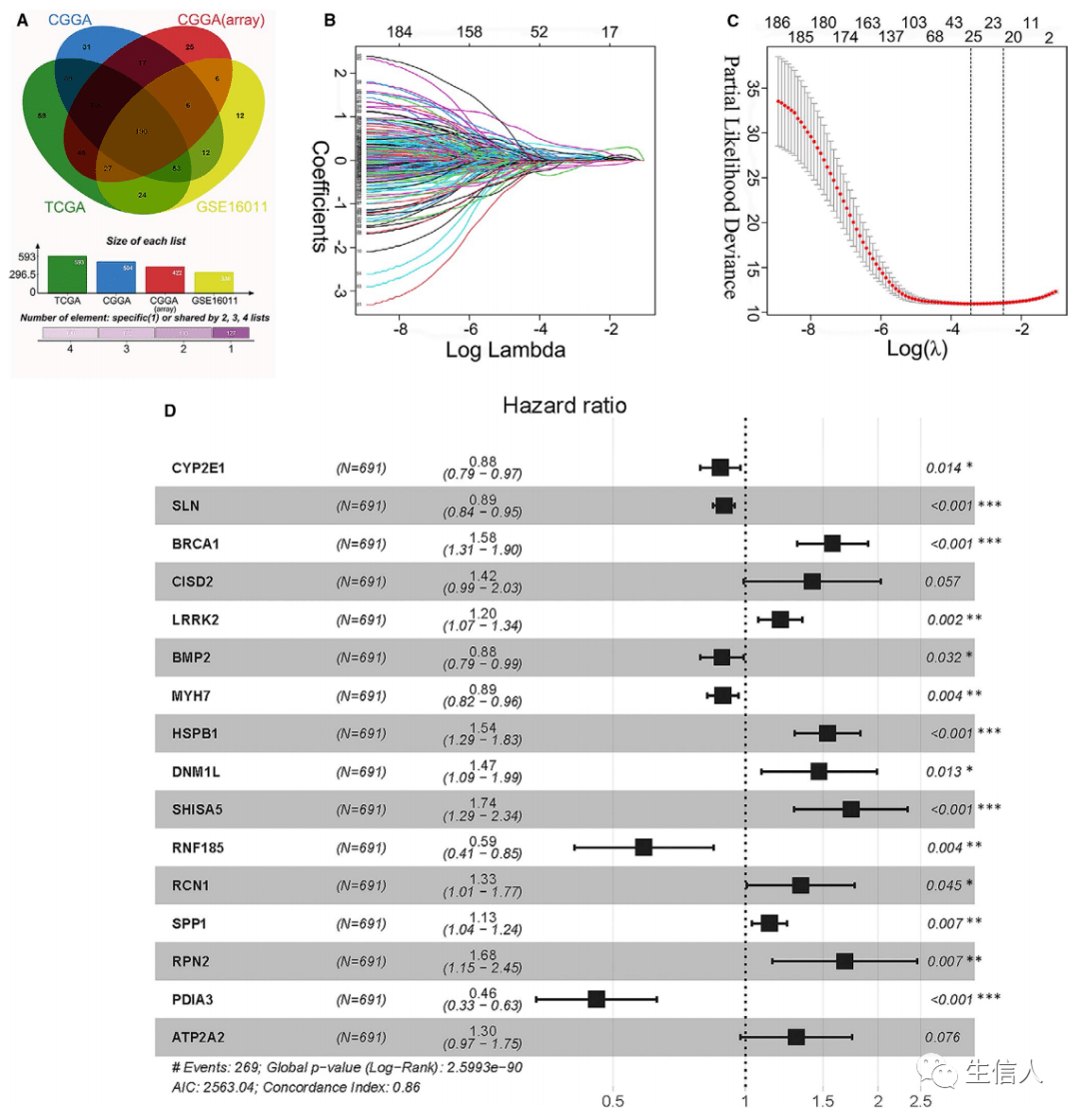
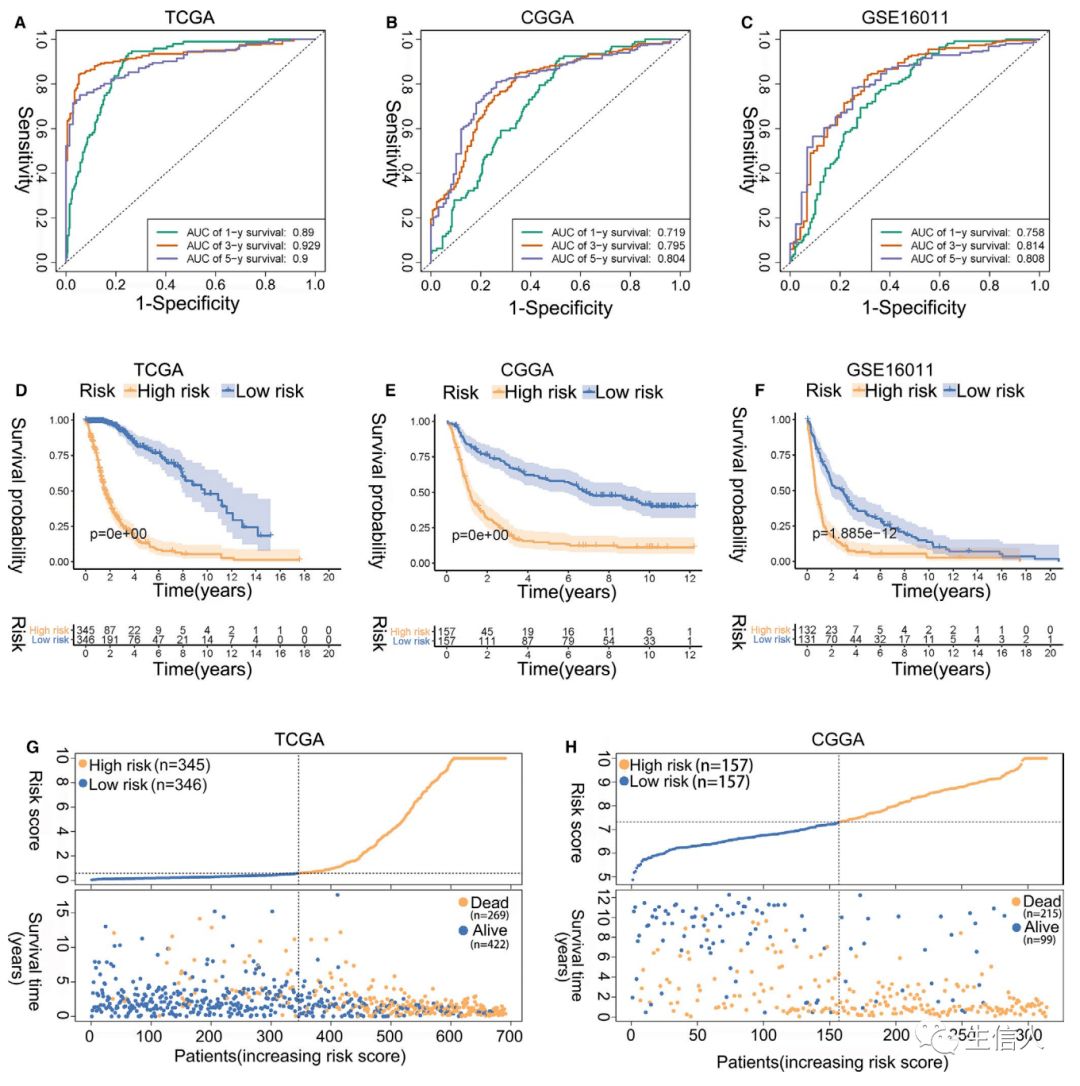
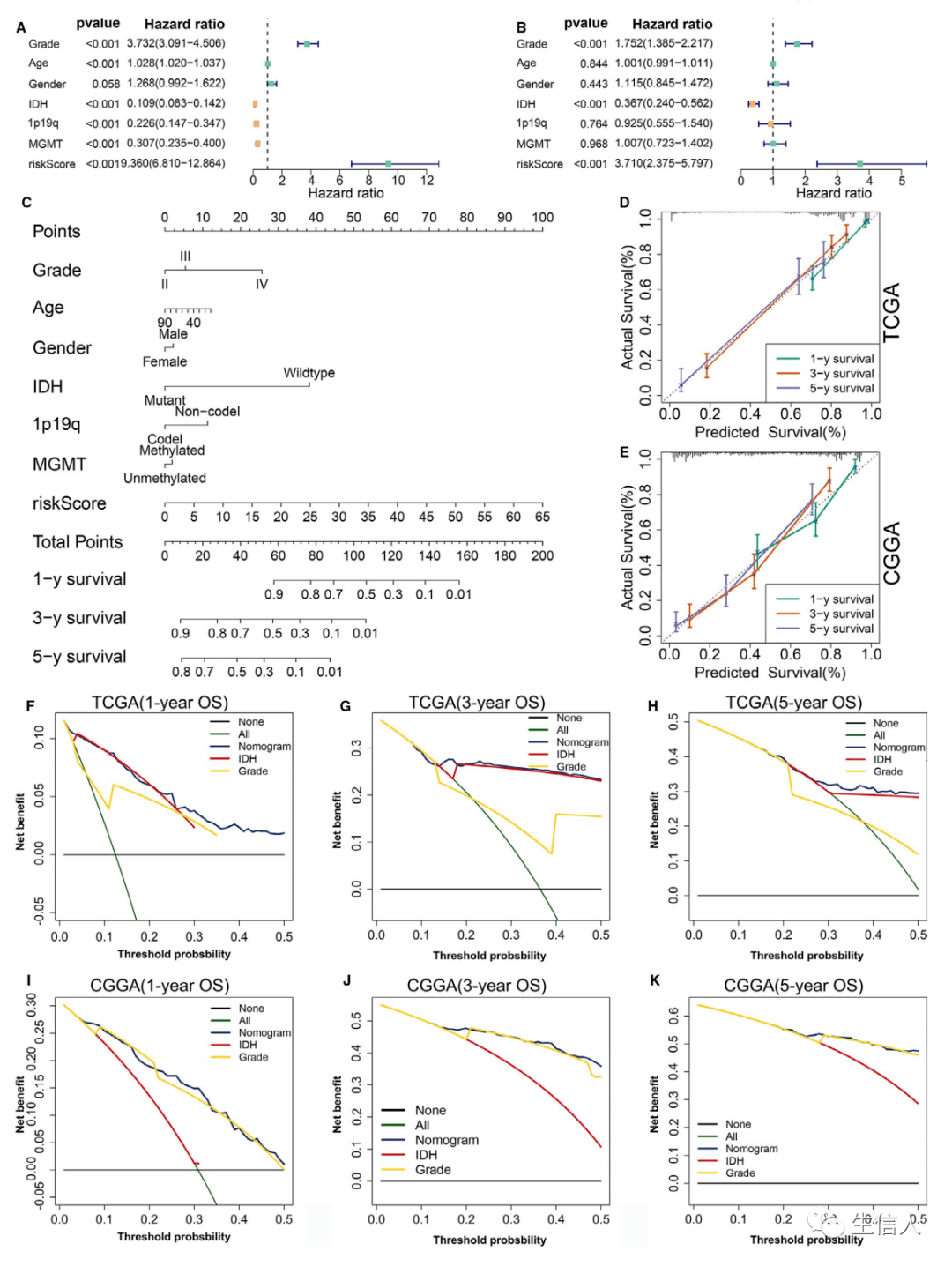
UPR的药理学调节 诱导未解决的或致命的内质网应激,或抑制上调素驱动的细胞保护功能,可用来抑制肿瘤的生长。此外,多种标准的护理疗法干扰内质网稳态,并在癌细胞中触发适应性内质网应激反应,促进肿瘤生长并介导对治疗的耐药。标准疗法与UPR调节器相结合的方法在临床前癌症模型中显示出了显著的疗效,因此值得未来在癌症患者中考虑。 调节内质网应激的药物/UPR在其他地方已经被广泛地综述。如IRE1α抑制剂,PERK抑制剂,eIF2α抑制剂以及BiP抑制剂。 综上所述,持续性内质网应激是癌症的新特征,它是由TME的多种代谢和致癌异常所驱动的,这些异常扰乱了恶性细胞和浸润性免疫细胞的蛋白质折叠稳态,构成活跃的ER应激反应使恶性细胞适应致癌和环境挑战,同时协调各种免疫调节机制,促进恶性进展。 通过上面的内容,相信大家已基本了解了内质网应激,看看别人是怎么开展研究的吧。 内质网应激 生信分析实例 关键图展示
综合整理自:健康界、生信人返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |