综述: 肿瘤及其微环境中的内质网应激信号 |
您所在的位置:网站首页 › 内质网应激反应名词解释 › 综述: 肿瘤及其微环境中的内质网应激信号 |
综述: 肿瘤及其微环境中的内质网应激信号
|
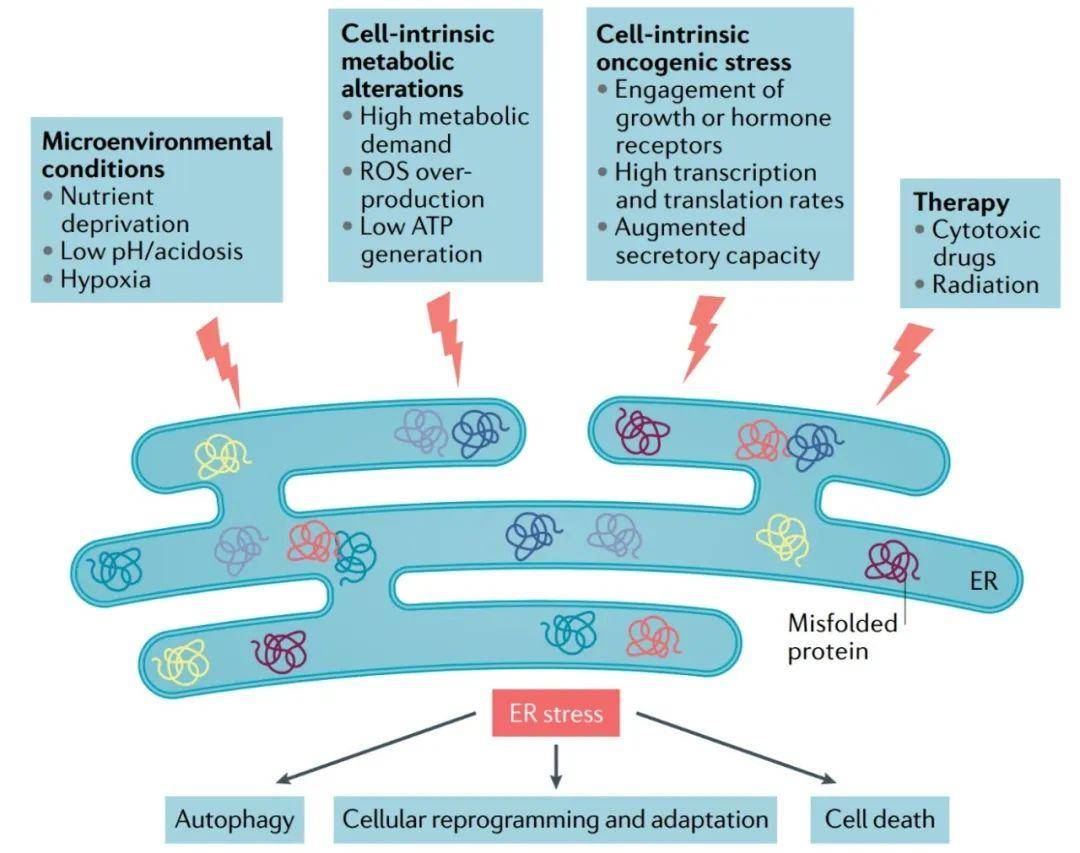
营养有效性 与正常细胞能量需求相比,代谢应激的特征是营养供应不足或过量,很容易破坏内质网的内稳态。葡萄糖和谷氨酰胺利用率与内质网应激在多个方面密切相关。葡萄糖或谷氨酰胺的缺乏中断了己糖胺生物合成途径(HBP),该途径利用这两种营养素生成尿苷二磷酸盐-N-乙酰氨基葡萄糖胺(UDP-GlcNAc),这是内质网中N-链糖基化和蛋白质折叠所必需的。 细胞内活性氧的积累 ER中的蛋白质折叠在很大程度上依赖于这个细胞器的氧化还原状态。细胞内活性氧(ROS)的积累是对外界条件的反应,或由各种信号事件引起的,可极大地扰乱细胞内的蛋白质稳定。例如,通过干扰谷胱甘肽的产生和改变内质网腔内的氧化还原环境,限制谷氨酰胺的水平会加重内质网的压力。大量的ROS作为电子传递链(ETC)的副产物,也可在线粒体内膜产生,特别是在脂肪酸氧化(FAO)过程中。 低PH 癌细胞利用好氧糖酵解作为中心代谢途径,从而产生乳酸,降低周围微环境的pH值。在检测到低PH时激活质子感应受体,可能通过破坏细胞内钙稳态和/或诱导ROS过量产生,在各种细胞类型中触发UPR的三臂。
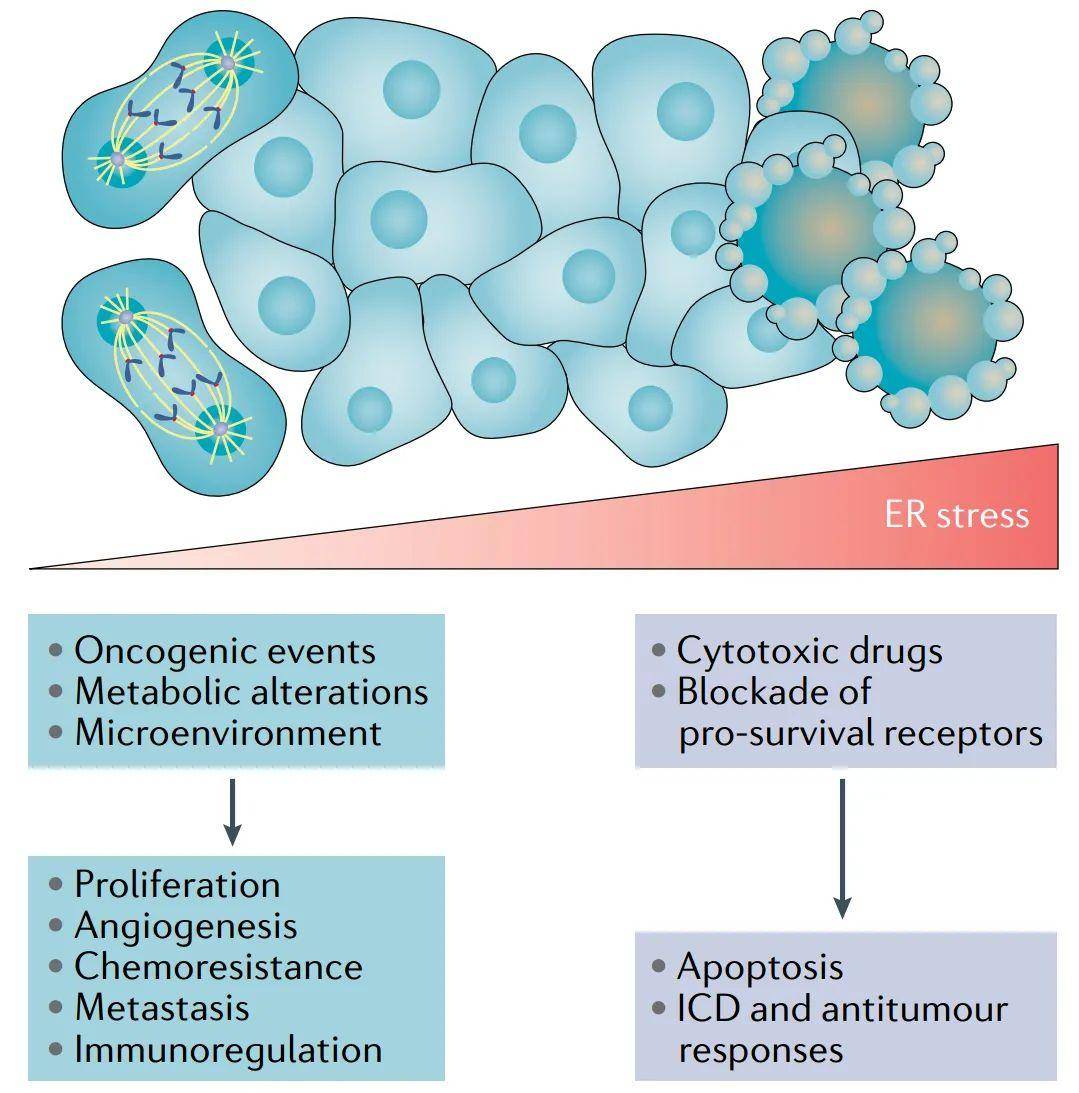
图1:内质网应激诱导物在肿瘤微环境中的作用。 癌细胞中内质网应激反应。 UPR在肿瘤转化和肿瘤生长中的作用 除了肿瘤产生的不利环境条件外,癌细胞的基因改变还会加剧内质网应激,促进UPR通路的持续激活。例如,肿瘤抑制因子的丢失和癌基因的过度激活容易增加蛋白质合成,以满足肿瘤发生期间增加的代谢需求。此外,增殖的癌细胞需要快速的ER扩张来分裂和分配到子细胞。协调内质粒应激反应是一个高度动态的过程,可能会导致促生存和促凋亡的输出。事实上,细胞命运的决定似乎取决于UPR的强度和持续时间。
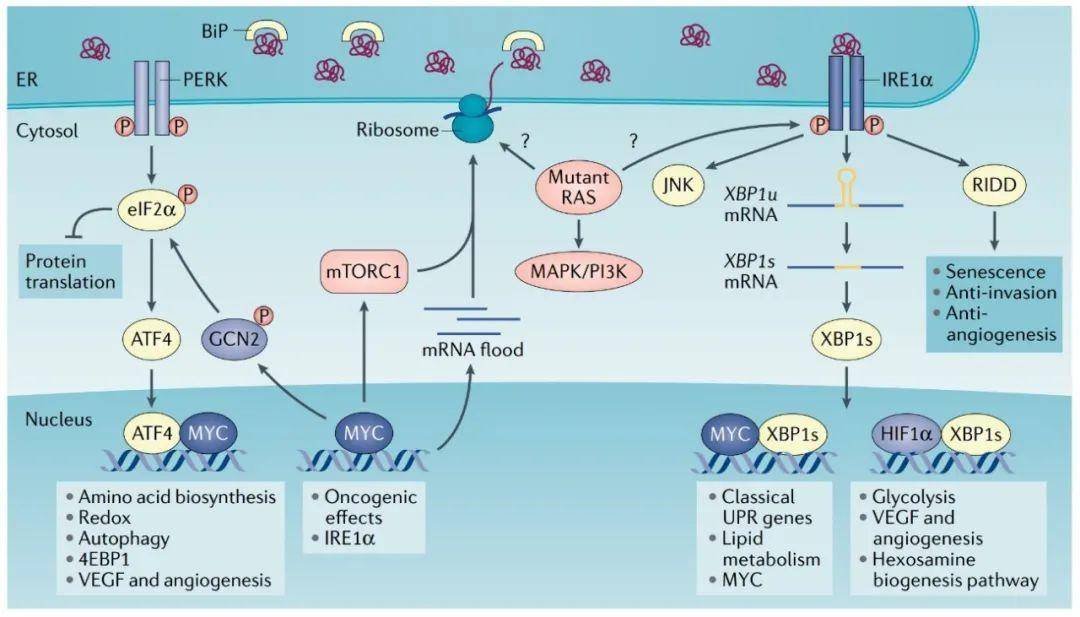
图2:恶性细胞内质网应激的大小及其分化结果。 转移和休眠的癌细胞中的UPR 尽管UPR在原发性肿瘤进展中的作用已被广泛研究,但它在多步骤转移方案中的作用仍未完全确定。癌细胞可以重新规划远端器官微环境来促进转移细胞的定植和存活,这一过程被称为转移前微环境(PMN)的形成。在雌激素受体阴性的乳腺肿瘤中,低氧可上调赖氨酸氧化酶(LOX),促进骨中PMN的形成。有趣的是,XBP1与LOX启动子结合并调控其表达,这增加了IRE1α–XBP1通过该因子参与PMN的可能性。在转移过程中,癌细胞在失去与细胞外基质(ECM)和邻近细胞的接触后,会发生失巢凋亡现象,这是一种程序性细胞死亡的形式。
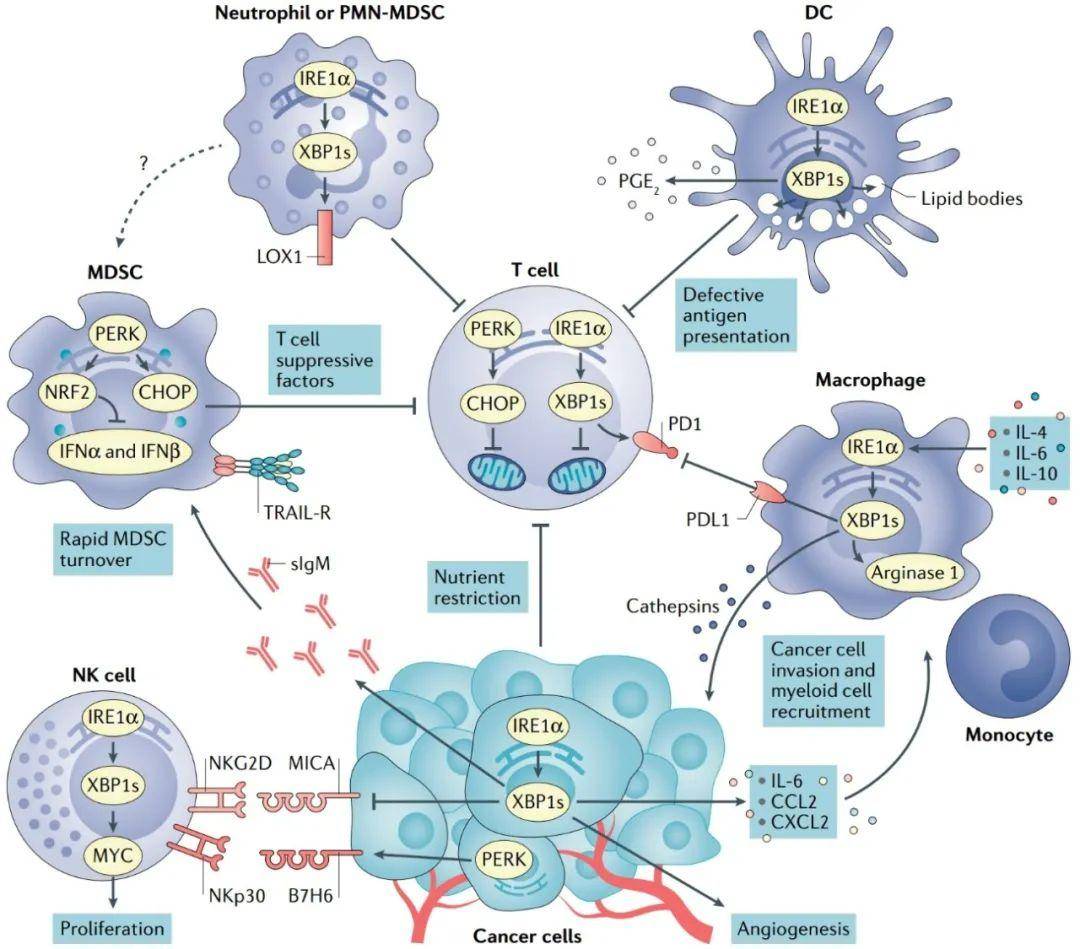
图3:癌基因计划和癌细胞内质网应激反应的整合。 细胞内质网应激对肿瘤免疫微环境的调节 大量研究表明,癌细胞内源性内质网应激反应可以通过改变共存于TME中的免疫细胞的功能来影响恶性进展。早期研究表明,ER应激的诱导和UPR的激活可抑制主要组织相容性复合体I (MHC-I)分子的表面表达,可能是通过XBP1s和ATF6的过表达。棕榈酸盐暴露或葡萄糖缺失在小鼠EL4淋巴瘤细胞中引发ER应激,被发现会导致eIF2α介导的蛋白合成抑制,进而损害MHC-I蛋白上的最佳肽负荷,损害其稳定性和正常的表面定位。此外,ER-应激上皮细胞表现出XBO1依赖的miR-346诱导,转录后抑制了参与抗原处理1 (TAP1)的ER转运体的表达,TAP1与ER肽的最佳内流和MHC-I抗原负载有关。 癌细胞ER应激反应被认为可以改变自然杀伤细胞(NK)介导的对肿瘤的识别。IRE1α-XBP1轴抑制了NK组2D (NKG2D)配体和MHC I类多肽相关序列A (MICA)在人黑素瘤细胞系经体外诱导ER应激中的表达,以及人类黑色素瘤样本中MICA表达减少与同一样本中固有的XBP1s水平呈负相关。在恶性细胞中抑制IRE1α-XBP1是否可以促进NK细胞驱动的抗肿瘤反应目前尚不清楚。但另一项研究表明,在接受药物性ER应激的黑色素瘤细胞中,激活UPR的PERK-eIF2 α轴可诱导B7H6(是NK细胞受体NKp30的配体)的表达。
图4:肿瘤微环境中内质网应激信号的免疫调节作用。 UPR的药物性调节 诱导未解决的或致命的内质网应激,或抑制上调素驱动的细胞保护功能,可用来抑制肿瘤的生长。此外,多种标准的护理疗法干扰内质网稳态,并在癌细胞中触发适应性内质网应激反应,促进肿瘤生长并介导对治疗的耐药。标准疗法与UPR调节器相结合的方法在临床前癌症模型中显示出了显著的疗效,因此值得未来在癌症患者中考虑。调节内质网应激的药物和(或)UPR在其他地方已经被广泛地综述。如IRE1α抑制剂,PERK抑制剂,eIF2 α抑制剂以及BiP抑制剂。 结论和展望: 持续性ER应激是癌症的一个新特征,它是由TME的多种代谢和致癌异常所驱动的,这些异常扰乱了恶性细胞和浸润性免疫细胞的蛋白质折叠稳态。构成活跃的ER应激反应使恶性细胞适应致癌和环境挑战,同时协调各种免疫调节机制,促进恶性进展。未来应系统地消除UPR对TME中个别细胞类型的精确影响,特别是对体内癌细胞代谢重编程的影响。虽然已有多项研究阐明了UPR在肿瘤发生过程中各阶段的作用和机制,但对于ER应激在肿瘤转移和治疗耐药中的作用,仍需进一步研究。 仅针对ER应激反应可以破坏癌细胞的一些攻击特性,同时增强抗肿瘤免疫,但这可能不会导致优于标准干预的治疗效果。然而,越来越多的证据表明,ER应激传感器或上调电位相关因素的调节造成了易感性,使侵袭性肿瘤对细胞毒性药物、靶向治疗和免疫治疗显着敏感。使用PDXs和免疫能力小鼠模型再现人类肿瘤异质性的更大规模的临床前研究,以及对临床试验标本的回顾性分析,可能有助于发现有效的超敏感药物靶向联合治疗,从而引发持久的反应,防止癌症进展和/或患者复发。 原文链接:https://www.nature.com/articles/s41568-020-00312-2 参考文献: 1. Chen X, Cubillos-Ruiz JR: Endoplasmic reticulum stress signals in the tumour and its microenvironment. Nat Rev Cancer 2020. 综述: 肿瘤及其微环境中的内质网应激信号 本文来自生物医学科研之家,作者DOC zhu。返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |