如何检测MET异常?首部《非小细胞肺癌MET临床检测中国专家共识》规范指导! |
您所在的位置:网站首页 › met检测板 › 如何检测MET异常?首部《非小细胞肺癌MET临床检测中国专家共识》规范指导! |
如何检测MET异常?首部《非小细胞肺癌MET临床检测中国专家共识》规范指导!
|
那么,随着MET抑制剂的研发成功,如何精准检测MET异常显得尤为重要。然而,由于MET异常形式多样,检测方法多种,临床检测中仍面临诸多问题和挑战。本次《共识》的出台,为MET检测提供了规范指导。 哪些人群需要检测MET? 【共识4】晚期NSCLC患者强烈推荐进行MET 14跳突检测;晚期初治和EGFR-TKI耐药后NSCLC患者推荐进行MET基因扩增检测。 用什么样本检测MET? 用于MET检测的样本类型主要包括肿瘤组织样本、细胞学样本以及液体样本等。MET 14 跳突可用 RNA 进行检测,相关样本应注意及时固定以及样本保存条件,以防RNA降解。 用什么方法检测MET? MET 14跳突 【共识5】MET 14跳突可使用RT-qPCR、DNA二代测序或RNA二代测序进行检测,不同检测方法各有其优缺点,必要时可相互验证或补充检测。MET 14 跳突位点形式多样,临床检测和判读中需特别注意。 MET 14跳突常见的突变位点分布区域较广,且突变形式多样,是临床检测和判读中面临的挑战。 非小细胞肺癌MET14号外显子跳跃突变常见检测方法 MET扩增 【共识 6】 MET 基因扩增可采用 FISH 和二代测序进行检测,FISH 是检测 MET 基因扩增的金标准,二代测序检测 MET 基因扩增尚需进一步优化和验证。 非小细胞肺癌MET基因扩增常见检测方法 ME基因扩增是指该基因拷贝数(gene copy number,GCN)增加,包括局部扩增(focal amplification)和多体(polysomy)2种形式。局部扩增是指 MET基因(或合并周围区域)的拷贝数增加,而位于染色体其他区域的基因的拷贝数没有明显变化;多体是指整条染色体(或染色体较大区段)的拷贝数增加。2 种形式都可能导致 MET mRNA水平上调,进一步增加 MET 蛋白表达,从而增加激活状态的 MET通路信号。 MET基因扩增可作为原发性肿瘤驱动基因变异之一,多种实体肿瘤中都有发现,NSCLC 中原发MET基因扩增发生比例为1%~5% 。MET基因扩增更常继发于其他驱动基因阳性NSCLC患者靶向治疗后,是EGFR-TKI耐药的重要机制之一。不同代EGFR-TKI 耐药后出现 MET 基因扩增比例不尽相同,根据文献数据,第一、二代EGFR-TKI 耐药后MET基因扩增的比例为 5%~22%,第三代 EGFR-TKI 奥希替尼一线耐药后MET基因扩增比例为7%~15%,二线耐药后为5%~50%。 除EGFR-TKI 外,MET 基因扩增也是ALK-TKI 耐药机制之一,第二、三代 ALK-TKI 耐药后 MET 基因扩增的比例约为13%。 临床研究中目前多采用 FISH 方法入组 MET 基因扩增患者,已有报道组织二代测序(肿瘤细胞比例≥10%,测序深度≥ 500×)与FISH 检测 MET基因扩增的阳性一致性约为62.5%,二代测序检测MET基因扩增有待进一步优化和验证。 MET蛋白过表达 MET蛋白过表达检测方法为IHC,利用抗原与抗体特异性结合的原理,通过化学反应使标记抗体的显色剂(荧光素、酶、金属离子、同位素等)显色来确定组织细胞内抗原(多肽和蛋白质),对其进行定位、定性及相对定量的方法。目前国内外检测MET的抗体已有多个获得国产医疗器械产品(备案),涉及多个克隆号,不同抗体的染色性能存在差异,尚没有统一的判读标准。 现阶段临床研究中,建议IHC检测结果应至少包括所使用的抗体信息、肿瘤细胞中阳性百分比和染色强度。
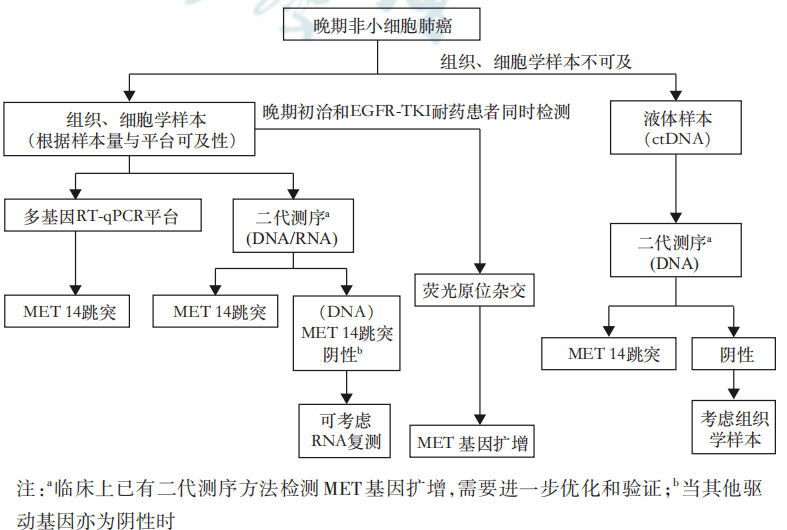
非小细胞肺癌MET检测路径 MET异常的精准检测是指导用药的基础,本次《共识》的发布推动临床MET检测的规范化,提高MET检测的准确性,从而为MET精准治疗提供指导。目前国内仍有多款MET抑制剂正在开展临床试验,针对MET14跳突、MET扩增和MET蛋白过表达,我们期待更多的MET抑制剂获批上市,给MET患者带来长生存期。 点击加入基因俱乐部 成就行业精英 目前已有500+行业精英加入基因俱乐部 返回搜狐,查看更多 |
【本文地址】
今日新闻 |
点击排行 |
|
推荐新闻 |
图片新闻 |
|
专题文章 |