| 高中化学选择性必修1知识点总结(1 | 您所在的位置:网站首页 › 高二数学选择性必修一知识点总结 › 高中化学选择性必修1知识点总结(1 |
高中化学选择性必修1知识点总结(1
|
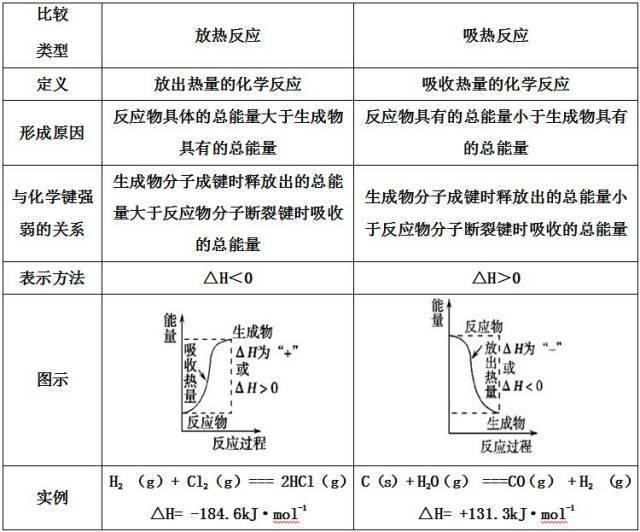
原标题:高中化学选择性必修1知识点总结(1-4章),高二期中考必看! 今天化学姐给大家整理了高中化学选择性必修1《化学反应原理》知识点总结(1-4章),高二的同学们看过来,期中考试前过一遍,提高期中考试复习效率, 如需下载打印版,请直接拉到文末查看。 01 第一章 化学反应的热效应 考点1:吸热反应与放热反应 1、吸热反应与放热反应的区别
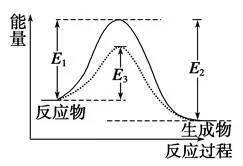
特别注意:反应是吸热还是放热与反应的条件没有必然的联系,而决定于反应物和生成物具有的总能量(或焓)的相对大小。 2、常见的放热反应 ①一切燃烧反应; ②活泼金属与酸或水的反应; ③酸碱中和反应; ④铝热反应; ⑤大多数化合反应(但有些化合反应是吸热反应,如:N2+O2=2NO,CO2+C=2CO等均为吸热反应)。 3、常见的吸热反应 ①Ba(OH)2·8H2O与NH4Cl反应; ②大多数分解反应是吸热反应 ③ 等也是吸热反应; ④水解反应 考点2:反应热计算的依据 1.根据热化学方程式计算 反应热与反应物各物质的物质的量成正比。 2.根据反应物和生成物的总能量计算 ΔH=E生成物-E反应物。 3.根据键能计算 ΔH=反应物的键能总和-生成物的键能总和。 4.根据盖斯定律计算 化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关。即如果一个反应可以分步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的。 温馨提示: ①盖斯定律的主要用途是用已知反应的反应热来推知相关反应的反应热。 ②热化学方程式之间的“+”“-”等数学运算,对应ΔH也进行“+”“-”等数学计算。 5.根据物质燃烧放热数值计算:Q(放)=n(可燃物)×|ΔH|。 02 第二章 化学反应速率与化学平衡 考点1:化学反应速率 1、化学反应速率的表示方法___________。 化学反应速率通常用单位时间内反应物浓度和生成物浓度的变化来表示。表达式:___________ 。 其常用的单位是__________ 、 或__________ 。 2、影响化学反应速率的因素 1)内因(主要因素) 反应物本身的性质。 2)外因(其他条件不变,只改变一个条件) 3、理论解释——有效碰撞理论 (1)活化分子、活化能、有效碰撞 ①活化分子:能够发生有效碰撞的分子。 ②活化能:如图
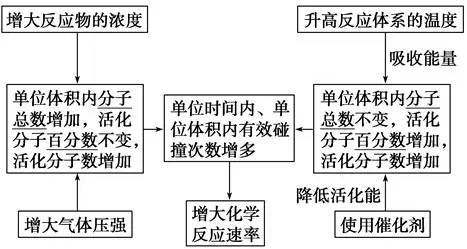
图中:E1为正反应的活化能,使用催化剂时的活化能为E3,反应热为E1-E2。(注:E2为逆反应的活化能) ③有效碰撞:活化分子之间能够引发化学反应的碰撞。 (2)活化分子、有效碰撞与反应速率的关系
考点2:化学平衡 1、化学平衡状态:一定条件(恒温、恒容或恒压)下的可逆反应里,正反应和逆反应的速率相等,反应混合物(包括反应物和生成物)中各组分的浓度保持不变的状态。 2、化学平衡状态的特征
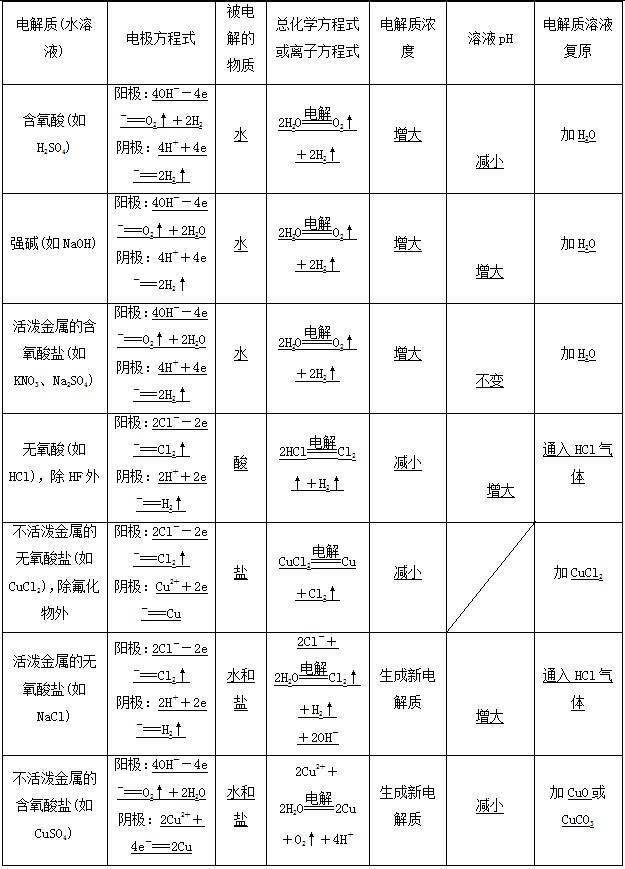
3、判断化学平衡状态的依据 考点3:化学平衡的移动 1、概念 可逆反应中旧化学平衡的破坏、新化学平衡的建立,由原平衡状态向新化学平衡状态的转化过程,称为 化学平衡的移动。 2、化学平衡移动与化学反应速率的关系 (1)v正>v逆:平衡向正反应方向移动。 (2)v正=v逆:反应达到平衡状态, 不发生平衡移动。 (3)v正b+c,则A的转化率增大;③若a< b+c,则A的转化率增大。 (2)若反应物不只一种,如 。则: 若只增加反应物A的量,平衡向正反应方向移动,则反应物B的转化率增大,但由于外界因素占主要方面,故A的转化率减小。 考点6:等效平衡 在一定条件(恒温恒容或恒温恒压)下,同一可逆反应体系,不管是从正反应开始,还是从逆反应开始,在达到化学平衡状态时,任何相同组分的百分含量(体积分数、物质的量分数等)均相同,这样的化学平衡互称等效平衡(包括“相同的平衡状态”)。 Ⅰ:恒温恒容条件下 ①恒温恒容时,对一般的可逆反应,不同的投料方式如果根据化学方程式中计量系数比换算到同一边时,反应物(或生成物)中同一组分的物质的量完全相同,则互为等效平衡。此时一般不考虑反应本身的特点,计算的关键是换算到同一边后各组分要完全相同。 ②恒温恒容时,对于反应前后 气体分子数不变的可逆反应,不同的投料方式如果根据化学方程式中计量系数比换算到同一边时,只要 反应物(或生成物)中各组分的物质的量的成比例,即互为等效平衡。此时的反应特点是无体积变化,计算的关键是换算到同一边后各组分只需要物质的量之比相同即可。 Ⅱ:恒温恒压条件下 在恒温恒压时,可逆反应以不同的投料方式进行反应,如果根据化学方程式中计量系数比换算,到同一边时,只要反应物(或生成物)中各组分的物质的量的成比例,即互为等效平衡。 03 第三章 水溶液中的离子反应与平衡 考点1:弱电解质的电离 1.弱电解质是指只部分电离的化合物,一般包括________、________ 和________ 三类物质。 2.弱电解质电离程度一般都很小,故弱电解质溶液中溶质的主要存在形式是________ ,弱电解质的电离程度决定对应弱酸(或弱碱)的强弱。 3.弱酸的电离分步书写,且电离程度一步比一步弱,弱碱的电离书写一步到位。 4.能够促进弱电解质电离的外界因素有________________________ 。 5.如果比较不同的酸与锌反应的速率,应该比较________浓度的大小;如果比较与锌反应产生氢气的多少,应该比较________浓度的大小;如果比较消耗氢氧化钠的多少,应该比较________ 浓度的大小。 6.水是极弱的电解质,能发生自身电离且简写为:。任何温度下的水溶液中一定满足:。 7.水的离子积,为一定值,只与________有关。在常温下的任何水溶液中一定满足=________。 8.若升高温度,将________水的电离,pH________,但与始终相等,故仍呈 性。100℃时中性溶液的pH等于________。 9.向水中加入任何酸或碱都会________水的电离。 考点2:溶液的酸碱性 1.计算pH的公式:,或。 2.pH=7的溶液不一定呈中性,除非是常温下,只有当时,才能肯定溶液呈中性。 3.计算pH值首先必须判断混合后的酸碱性,若呈酸性,则求混合后的;若呈碱性,则求混合后的;若溶液呈中性,则说明。 4.强酸pH=a,加水稀释10 n 倍,则pH=________;弱酸pH=a,加水稀释10 n 倍,则________Br - >Cl - >OH - >含氧酸根离子。 (2)阴极产物判断 阳离子放电顺序:Ag + >Fe 3+ >Cu 2+ >H + (酸)>Fe 2+ >Zn 2+ >H + (水)>Al 3+ >Mg 2+ >Na + >Ca 2+ >K + 。 7、电解不同溶液的情况对比
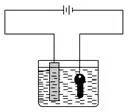
8、电解池的应用 1)电解饱和食盐水 (1)电极反应 阳极反应式:2Cl - -2e - ===Cl 2 ↑(氧化反应) 阴极反应式:2H + +2e - ===H 2 ↑(还原反应) (2)总反应方程式: 离子反应方程式: (3)应用:氯碱工业制烧碱、氯气和氢气。 2)电镀 下图为金属表面镀银的工作示意图,据此回答下列问题:
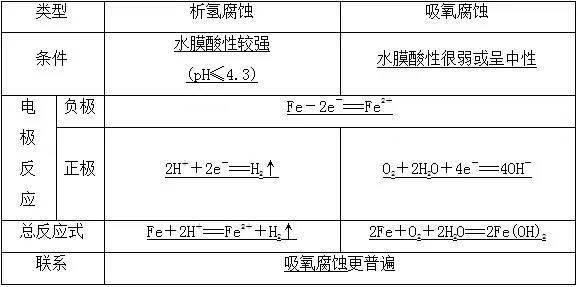
(1)镀件作阴极,镀层金属银作阳极。 (2)电解质溶液是AgNO 3 溶液等含镀层金属阳离子的盐溶液。 (3)电极反应: 阳极:Ag-e - ===Ag+ ; 阴极:Ag + +e - ===Ag。 (4)特点:阳极溶解,阴极沉积,电镀液的浓度不变。 3)电解精炼铜 (1)电极材料:阳极为粗铜;阴极为纯铜。 (2)电解质溶液:含Cu 2+ 的盐溶液。 (3)电极反应: 阳极:Zn-2e - ===Zn 2+ 、Fe-2e - ===Fe 2+ 、Ni-2e - ===Ni 2+ 、Cu-2e - ===Cu 2+ ; 阴极:Cu 2+ +2e - ===Cu。 4)电冶金 利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。 (1)冶炼钠 电极反应: 阳极:2Cl - -2e - ===Cl 2 ↑;阴极:2Na + +2e - ===2Na。 (2)冶炼铝 电极反应: 阳极:6O 2- -12e - ===3O 2 ↑;阴极:4Al 3+ +12e - ===4Al。 考点3:金属的腐蚀和保护 1.金属腐蚀的本质 金属原子 失去电子变为 金属阳离子,金属发生 氧化反应。 2.金属腐蚀的类型 (1)化学腐蚀与电化学腐蚀 (2)析氢腐蚀与吸氧腐蚀 以钢铁的腐蚀为例进行分析:
3.金属的防护 (1)电化学防护 ①牺牲阳极的阴极保护法—原电池原理 a.负极:比被保护金属活泼的金属; b.正极:被保护的金属设备。 ②外加电流的阴极保护法—电解原理 a.阴极:被保护的金属设备; b.阳极:惰性金属。 (2)改变金属的内部结构,如制成合金、不锈钢等。 (3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。 领 取 资 料 电子版领取方式: 【第1步】点击下面公众号名片,进入高中化学公众号首页 ▼ 【第2步】在高中化学公众号首页,点击右上方的“发消息”发送 11月资料,即可获得电子版资料。 ▎编辑:化学姐 ▎标签:高中化学 ▎版权:本文内容来源于网络,版权归相关权利人所有,如有侵权请联系我们。更多内容请关注高中化学。商务合作请在后台回复“商务合作”。 23条高中化学知识顺口溜,5分钟记住高中3年全部知识点~ 高中化学必修一新人教版基础知识填空(1-4章),期中考试必备! 高中化学课本全册每一页考试重难点提炼(预复习必备手册) 高中化学三年知识思维导图(高清版),学习重点全在里面! 高中化学一轮复习必备知识点总结,每天背一点,基础掌握牢! 高中化学300个知识盲点汇总! 高中化学实验题答题模板归类总结! 如何领取电子版资料?→扫描上方二维码关注 高中化学公众号,发送消息 【11月资料】即可领取资料返回搜狐,查看更多 责任编辑: |
【本文地址】