| 【糖尿病学术前沿】重新认识GLP | 您所在的位置:网站首页 › 脑神经生长素的作用是什么 › 【糖尿病学术前沿】重新认识GLP |
【糖尿病学术前沿】重新认识GLP
|
GLP-1的来源只有肠道吗?
GLP-1的受体分布有什么新进展吗?
GLP-1对靶器官的作用只能通过受体配体途径吗?
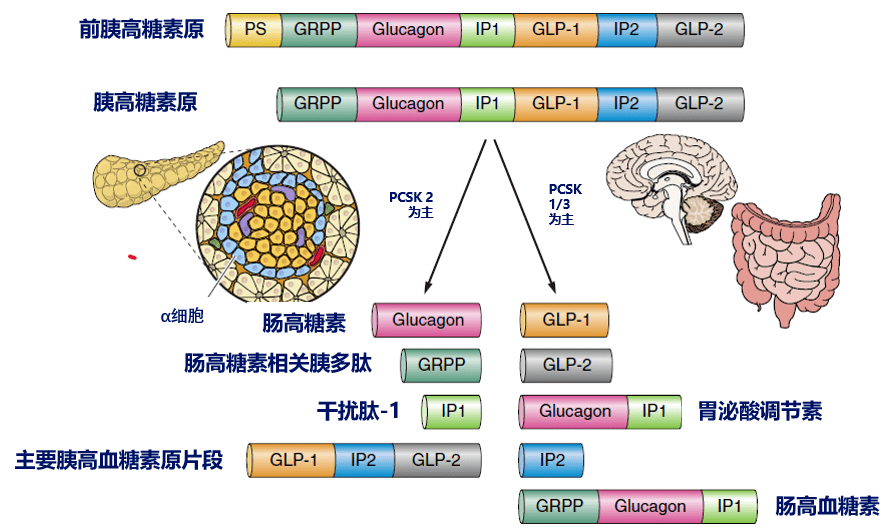
GLP-1的来源只有肠道吗 ? 在经典观念中,远端肠道受进餐刺激分泌GLP-1,即主要分布在回肠和结肠的L细胞分泌GLP-1。而近些年的研究有了新的发现,人类不仅有肠源性的GLP-1,还有胰源性GLP-1和脑源性GLP-1 3,4 。这背后的逻辑是,我们的GLP-1来自于由前胰高血糖素原(preproglucagon, Gcg )基因编码的胰高血糖素原,胰高血糖素原需要被PCSK 1/3进一步剪切加工后才能产生GLP-1,与之相对的是PCSK 2无法剪切出GLP-1。曾经我们认为胰腺中只有PCSK2,即无法产生GLP-1。但近年来的研究发现,胰腺α细胞和某些神经元内也存在PCSK 1/3(图3)。
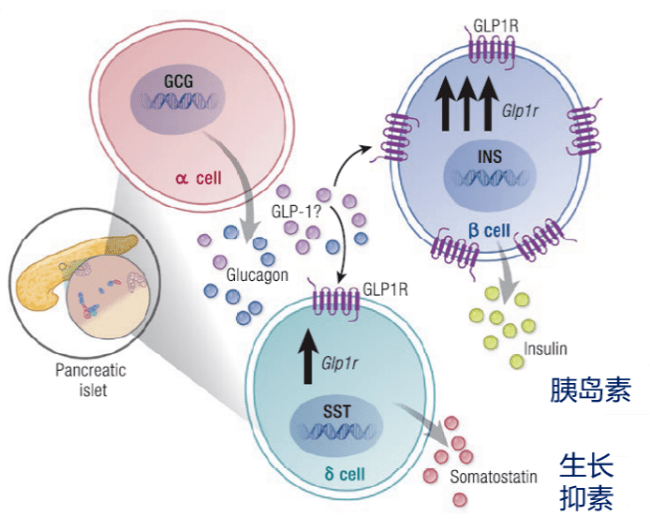
图3 胰高血糖素前原的转录后加工(剪切),神经元和胰腺均存在PCSK 1/3 我们所熟知的肠源性GLP-1构成了循环系统中活性GLP-1的大部分,那么胰源性和脑源性的GLP-1 与肠源性GLP-1是一样的吗? 首先介绍胰腺,早期研究证实,胰腺损伤或实验性诱导胰腺炎症时,α细胞应答性地增加PCSK1表达,提示α细胞可能是胰源性GLP-1合成的位点。而在特异性敲除肠 Gcg 基因的小鼠中,几乎无法在血液循环中检测到GLP-1,提示胰源性GLP-1并不是通过进入循环系统起效的。进一步的研究提示,胰源性GLP-1是通过旁分泌信号结合胰岛β细胞和δ细胞的GLP-1受体,进而发挥如:刺激胰岛素分泌、增加生长抑素分泌、抑制胰高糖素分泌、抑制β细胞凋亡等作用(图4) 5 。
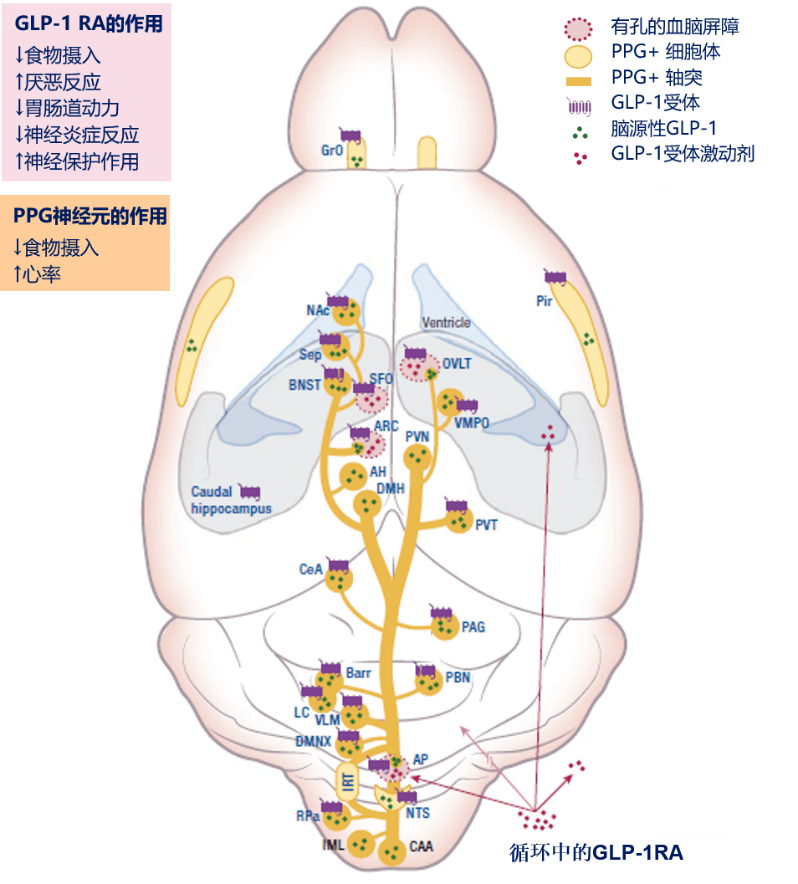
图4 胰岛内GLP-1的可能来源及其旁分泌信号途径 (胰腺α细胞可能合成并分泌GLP-1,并作用于β细胞与δ细胞) 其次再论述神经系统。目前的研究发现,脑源性GLP-1由前胰高血糖素原(preproglucagon, PPG)神经元产生。中枢神经系统内的PPG神经元大部分位于脑干后端的孤束核(NTS)和中间网状核(IRT),除此之外还有嗅球的颗粒细胞层(GrO)、梨状皮质(Pir)和腰骶段脊髓(图5)5 。
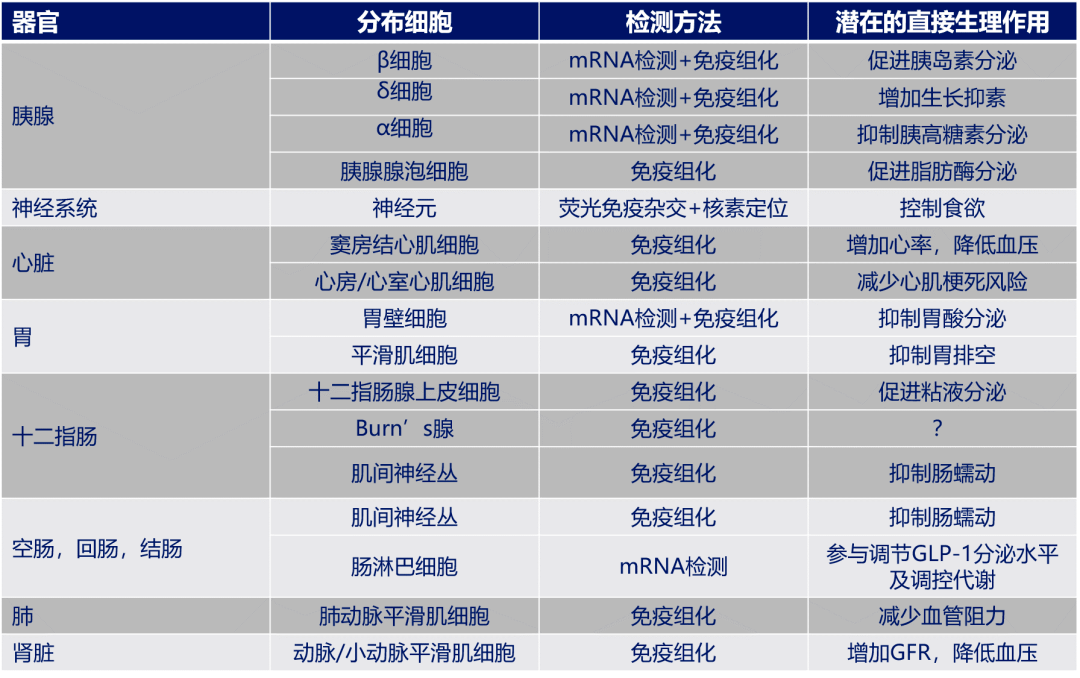
图5 脑源性的GLP-1和中枢神经系统中的GLP-1受体 那么PPG神经元产生的GLP-1和循环中的GLP-1功能一样吗?通过敲除小鼠的PPG神经元,Marie K等人发现,小鼠的糖耐量并不受到影响,也不影响他们的进食,但是如果对小鼠进行应激诱导或直接激活PPG神经元都会导致进食减少,提示PPG神经元产生的GLP-1参与应激时的食欲调节 6 。而循环中的GLP-1因为无法直接透过血脑屏障,它们需要在缺少血脑屏障的脑区,如脑干极后区(AP)、下丘脑弓状核(ARC)等区域,与GLP-1受体结合从而起到抑制食欲的作用(图5) 5 。以上机制也能解释:为什么Daniel I Brierley等人同时对小鼠激发孤束核的PPG神经元和给予外源性GLP-1受体激动剂司美格鲁肽后,在72小时内观察到小鼠的摄食量受到了叠加抑制作用 7 。 综上所述,胰源性GLP-1可能来自胰岛α细胞,主要通过旁分泌途径起效。而脑源性GLP-1主要由PPG神经元产生,它在大量进食或应激状态下释放并产生抑制食欲的作用,但不参与糖耐量调节。 GLP-1的受体分布有什么新进展吗? 聊完GLP-1的合成位点,我们再来看看GLP-1的受体分布有什么新进展。如下表所示,除了我们最早发现的胰岛β细胞和中枢神经系统,GLP-1受体在心血管、胃和肾脏等部位广泛分布(表1) 5 。 表1 表达GLP-1受体的主要部位
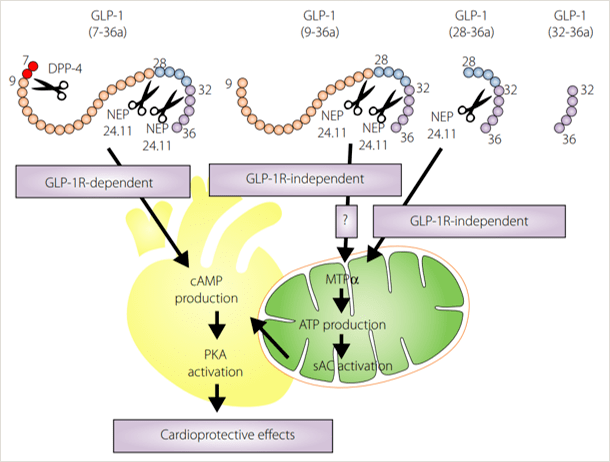
看起来GLP-1受体的分布工作已经非常详尽,那么现有的结果能让学者们满意吗?答案是否定的。回顾GLP-1的多重作用(图1),仍有一些是无法通过以上靶器官解释的作用。如在临床和动物试验中,GLP-1受体激动剂能减少心肌梗死面积,但是在梗死最容易发作的部位——左心室的心肌细胞处并没有检测到GLP-1受体的蛋白高表达 8 ;类似的还有,GLP-1受体激动剂能改善非酒精性脂肪性肝炎,但目前学者们对肝脏细胞的GLP-1受体表达证据的意见尚不统一。 如何解释上面的问题呢?第一种可能就是我们的检测手段受限。比如:1. 人类的某些组织细胞的mRNA表达水平过低,现有方法敏感性低;2. 运用免疫组化/荧光方法染色时,容易受到制片背景的干扰;3. 在进行抗原-抗体检测时选择试剂不准确,某些GLP-1抗体/受体激动剂/受体拮抗剂不同源,并不能结合灵长类或人源性的GLP-1受体。第二种可能就是我们下面要讨论的思路:GLP-1对靶器官的作用只有受体配体途径吗? GLP-1对靶器官的作用只能通过受体配体途径吗? 直接给出答案: GLP-1可以通过非受体配体途径作用起效。最有力的证据来源于对心血管系统的研究。 最早的证据为Kiwon Ban等人在2008年发表的一篇研究。他们发现在缺血再灌注损伤的野生型及GLP-1受体敲除小鼠的离体心脏模型中,GLP-1(7-36) 可使小鼠的动脉血管舒张,而使用GLP-1受体激动剂艾塞那肽却并无此作用;更神奇的是,经一氧化氮合酶(NOS) 抑制剂预处理后,GLP-1的血管舒张作用会被完全抵消,提示GLP-1的血管舒张作用可能与NOS依赖的 cGMP形成有关 9 。 在获得以上研究结果后,Kiwon Ban等人又再接再厉,进一步的机制研究发现:在小鼠的离体心脏模型中,GLP-1(9-36)对敲除GLP-1受体的心肌细胞仍有保护作用。此外,GLP-1(9-36)还能提高缺血再灌注损伤的人主动脉内皮细胞的存活率,该作用同样对NOS抑制剂敏感 10 。 类似的试验现象也可见于M Ahsan Siraj在2020年发表的一篇研究。他们同样发现GLP-1(28–36) 的心肌保护作用在GLP-1 受体敲除的小鼠中仍然存在。进一步的研究发现,GLP-1(28-36)通过胞吞作用进入人的冠状动脉内皮细胞,并直接作用于冠状动脉平滑肌细胞和内皮细胞,激活AC-cAMP通路,该途径还依赖于线粒体三功能蛋白-α(MTP-α) 11 。 综上所述,除了受体配体途径,GLP-1还可以通过非受体依赖途径作用于心血管系统(图6) 12 。
图6 GLP-1可以通过受体配体途径和非受体配体途径发挥心血管保护作用的分子机制 总 结 除了肠道,GLP-1的合成位点还有胰腺α细胞和中枢神经系统PPG神经元。 目前已经发现许多组织器官中存在GLP-1受体,但是受检测水平影响,GLP-1受体的版图很可能还是不完整的。 除了受体配体途径,GLP-1也可以通过非受体配体途径作用起效,如AC-cAMP通路。 除了肠道,GLP-1的合成位点还有胰腺α细胞和中枢神经系统PPG神经元。 目前已经发现许多组织器官中存在GLP-1受体,但是受检测水平影响,GLP-1受体的版图很可能还是不完整的。 除了受体配体途径,GLP-1也可以通过非受体配体途径作用起效,如AC-cAMP通路。 参考文献 1. Drucker D.J. Cell Met. 2016 12;24(1)15-30 2. Henquin J. Diabetes. 2000; 49:1751-60 3. Youngmi Song, et al. Cell Metab. 2019;30(5):976-986.e3 4. Llewellyn-Smith,I J et al. Neuroscience vol. 180 (2011): 111-21 5. Brent A McLean, et al. Endocr Rev. 2021 Mar15;42(2):101-132 6. Holt MK, et al. Diabetes. 2019;68(1):21-33 7. Brierley DI, et al. bioRxiv. 2020. 8. Charles Pyke, et al. Endocrinology. 2014Apr;155(4):1280-90 9. Kiwon Ban, et al. Circulation. 2008 May 6;117(18):2340-50 10. Kiwon Ban, et al.Endocrinology.2010 Apr;151(4):1520-31 11. M Ahsan Siraj, et al. J Clin Invest. 2020 Mar2;130(3):1392-1404 12. Yangyang Liu, et al. J Diabetes Investig. 2020 Nov;11(6):1422-1425 《糖尿病学术前沿》介绍: 诺和诺德医学事务团队长期关注内分泌领域新进展,共同监测20余个糖尿病领域顶级专业杂志及网站,精选其中的热点文章,总结提炼制作而成《糖尿病学术前沿》项目,旨在持续推进内分泌领域的前沿学术信息沟通。 欢迎关注 诺和诺德医学资讯,获取前沿学术信息: 1. 点击右上角↗,关注我们或分享给你的同事; 2. 也可以添加朋友→搜索诺和诺德医学资讯或者扫描下方二维码。 本资讯旨在为医学专业人士提供内分泌领域的新进展,仅供医学专业人士阅览之用。文中内容不能取代专业的医疗指导,也不应视为诊疗建议。医学专业人士在对文中涉及到的任何药品进行处方时,请严格遵循该药品在中国批准使用的说明书。诺和诺德不承担相应的有关责任。返回搜狐,查看更多 |
【本文地址】