| 孟庆华述评:深度学习虚拟压头实现纳米尺度材料硬度的快速无损测量 | 您所在的位置:网站首页 › 纳米压痕操作 › 孟庆华述评:深度学习虚拟压头实现纳米尺度材料硬度的快速无损测量 |
孟庆华述评:深度学习虚拟压头实现纳米尺度材料硬度的快速无损测量
|
原创 Cell Press CellPress细胞科学  物质科学 Physical science 作为世界领先的全科学领域学术出版社,细胞出版社特与“中国科学院青年创新促进会”合作开设“青促会述评”专栏,以期增进学术互动,促进国际交流。 2023年第十四期(总第142期)专栏文章,由来自国家纳米科学中心副研究员 中国科学院青促会会员 孟庆华,就 Matter中的论文发表述评。  硬度测量是表征材料力学性能最常用的技术。尽管如此,传统的纳米压痕实验方法仍存在诸多局限性。例如,实验测量会损坏材料样本、测量结果会受到实验设备和操作人员水平的影响、测量效率较低等。如何快速无损地测量材料硬度仍是一个悬而未决的科学问题。 人工智能已成为提升数据信息价值和揭示隐藏见解的重要技术工具。人工智能技术的不断发展为材料性能的快速表征和预测提供了有效手段。目前,人工智能模型已成功应用于材料力学领域。例如,它可以用于预测材料的断裂、屈曲及结构优化等。 长按图片扫描二维码阅读论文 在本期Matter中,美国麻省理工学院Markus J. Buehler研究团队发表题为 “Deep learning virtual indenter maps nanoscale hardness rapidly, non-destructively, revealing mechanism, and enhancing bioinspired design”研究论文。作者们将回归、对比生成和遗传算法优化三种方法相结合,提出一种人工智能模型来表征牙釉质材料的硬度。此模型将有助于深入理解材料硬度的主要影响因素以及材料结构的精准可控设计。 作者们首先通过组合不同数量和精度的数据集,获得了相对完整的牙釉质硬度图。如图1所示,该模型包括三个数据集:精准标记、估计标记和杂乱标记。这三个数据集被组合成一个含有22730对图像标记的数据集,其中材料硬度值介于2 GPa到7 GPa之间。采用深度残差神经网络架构(如图2所示),作者们训练了图像回归模型,实现了牙釉质结构图到其硬度值的定量映射。 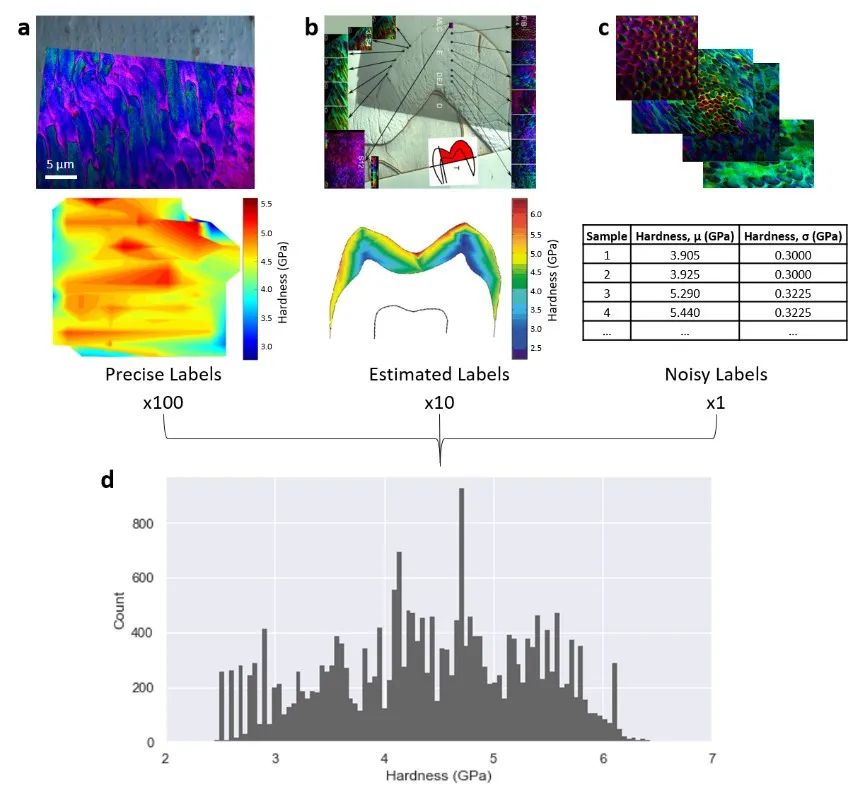 ▲图1 数据集管理 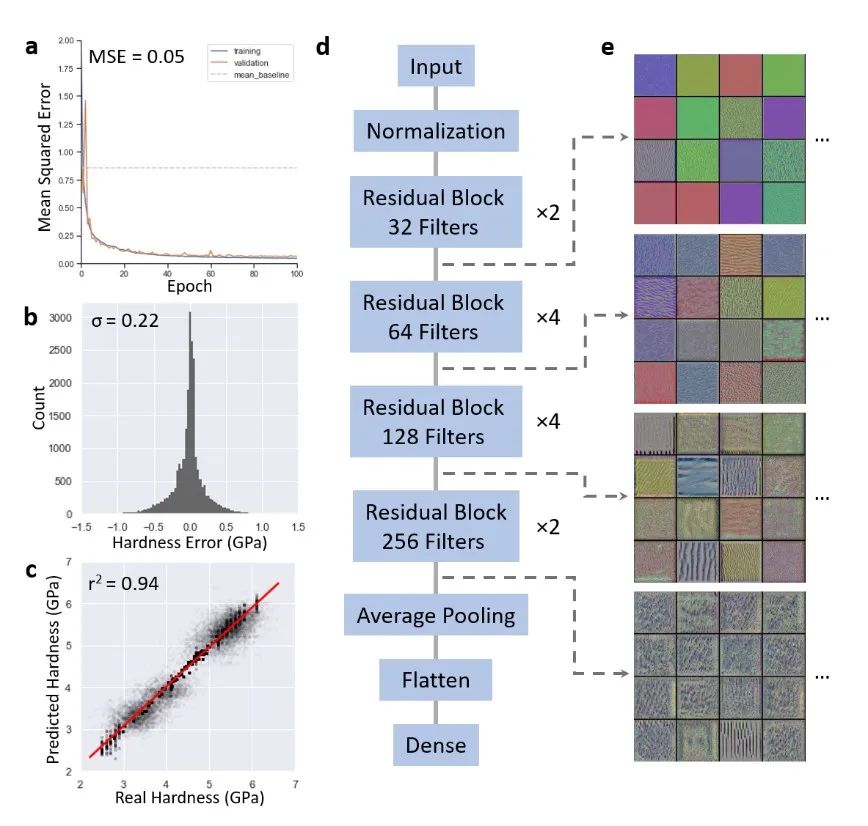 ▲图2 深度残差网络回归 为了理解取向偏差与材料硬度之间的关系,需要使用过滤器激活最大化方法来实现模型内容的可视化。模型的初始层使用不同的图像颜色来区分晶体取向,而模型的深层使用图案和纹理来识别晶体结构和尺寸。图3展示了牙釉质结构的显著可视图。它可以计算预测的空间支持度,并识别对确定输出最重要的图像局部区域。然后,将图像的色调和亮度值转换为图像平面方向和外平面方向的函数。 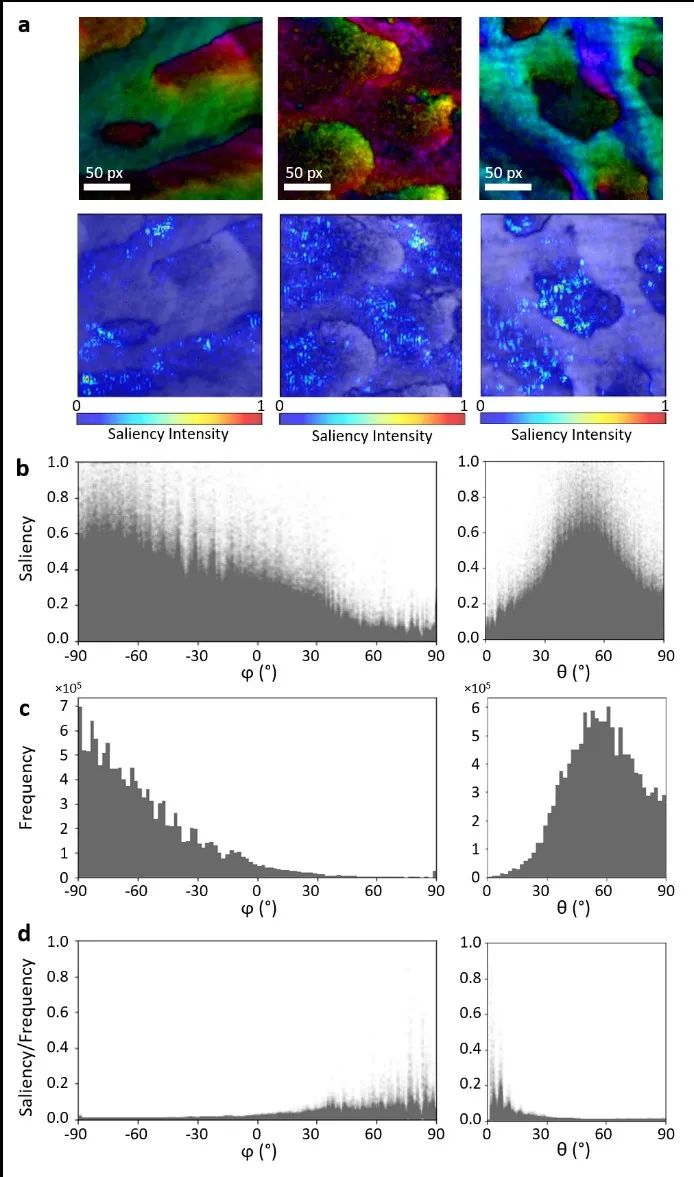 ▲图3 模型预测的理解 作者们采用深度残差网络回归模型作为高通量和高分辨率的虚拟压痕工具(图4),以识别高硬度和低硬度区域,预测牙釉质的硬度值,进而建立了一种快速无损的材料硬度测量方法。此外,使用迭代遗传算法的反向设计来快速获得具有特定硬度值的牙釉质结构(图5)。首先,将图像数据集训练为二次生成模型,并使用全局优化技术来探索结构的潜在设计空间。经过几十代的结构种群漂移,最终获得了接近期望硬度的牙釉质结构。 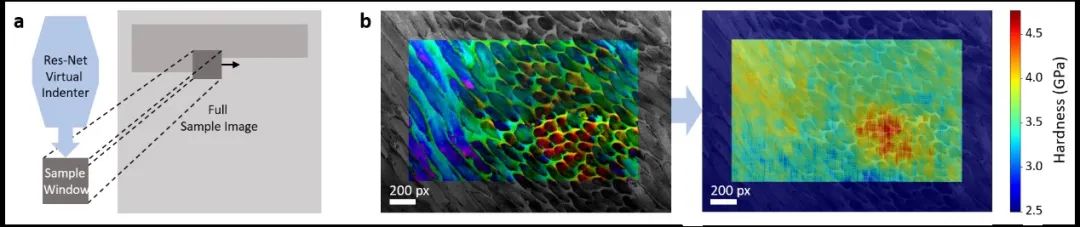 ▲图4 机器学习驱动硬度表征 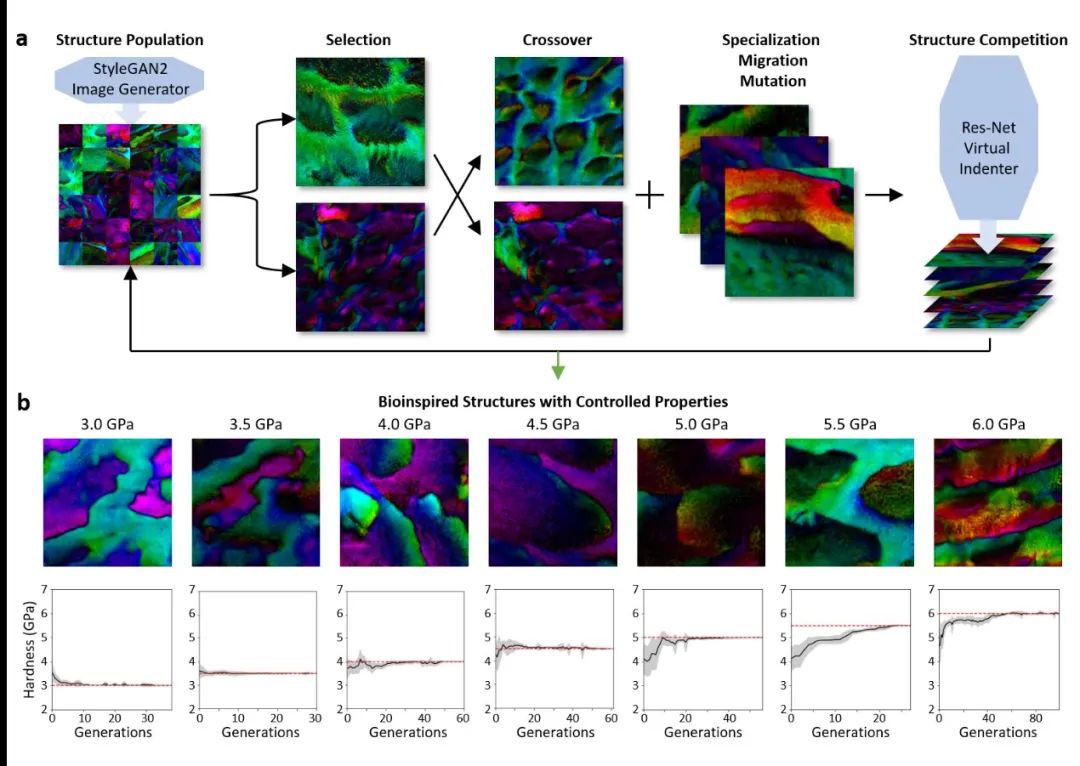 ▲图5 目标进化设计 此研究工作发展了一种人工智能模型,实现了纳米尺度材料硬度的快速无损测量。该人工智能模型打破了传统的实验测量方式,为表征材料硬度提供了革命性的新方法。人工智能模型具有非破坏性、一致性和可扩展性等优点,获取恰当、有效的数据集是其高效应用的关键。同时,它也为大规模搭建材料力学性能与结构之间的映射关系,实现材料结构的逆向设计提供了重要途径。 论文摘要 通过不断进化,生物体形成了适合其生存环境的复杂材料结构。基于这些久经考验的天然设计,人工仿生结构呈现出优越的材料配置。尽管如此,通过调控结构特征来获得理想材料性能的方式依然是重要的设计策略。本研究工作将针对人体最坚硬的生物组织——牙釉质,阐明其结构与性能之间的关系。材料硬度的实验测量方法耗时且具有破坏性,而本文提出的人工智能模型能够直接预测材料性能,实现高通量的无损表征。在模型中,将深度图像回归神经网络作为代理模型进行训练,通过梯度上升和显著图的可视化来识别硬度最高的材料结构特征。与实验硬度图相比,该模型能够提高空间分辨率和灵敏度。利用这一快速硬度测试模型,通过耦合对比生成模型和具有潜在空间的遗传算法来实现材料设计,从而精准构筑硬度可控的仿生结构。 Over evolution, organisms develop complex material structures fit to their environments. Based on these time-tested designs, human-engineered bioinspired structures offer exciting possible materials configurations. However, navigating diverse structure spaces for attaining desired properties remains nontrivial. We focus on the hardest biological tissue in humans, tooth enamel, to examine the structure-property relationship. While typical hardness measurements are time consuming and destructive, we propose that artificial intelligence models can predict properties directly and enable high-throughput nondestructive characterization. We train a deep image regression neural network as a surrogate model, and visualize with gradient ascent and saliency maps to identify structural features contributing most to hardness. This model demonstrates improved spatial resolution and sensitivity compared to experimental hardness maps. Using this rapid hardness testing model, a generative adversarial model, and a genetic algorithm that operates in latent space allows for guided materials design, yielding proposed designs for bioinspired structures with precisely controlled hardness. 向下滑动阅览摘要原文 中文内容仅供参考,请以英文原文为准 评述人简介  孟庆华 国家纳米科学中心副研究员 中国科学院青促会会员 孟庆华,国家纳米科学中心副研究员,2023年入选中国科学院青年创新促进会。主要研究方向为生物材料多尺度力学。已在J Mech Phys Solids、Appl Mech Rev、Int J Solids Struct等力学领域国际期刊发表论文20余篇。 Meng Qinghua is an associate professor at National Center for Nanoscience and Technology, China. In 2023, he was selected into the Youth Innovation Promotion Association, Chinese Academy of Sciences. His research interest focuses on the multiscale mechanics of biomaterials. He has published more than 20 papers in international journals in the field of mechanics, such as J Mech Phys Solids, Appl Mech Rev, Int J Solids Struct. 阅读原文 |
【本文地址】