| 人教版九年级化学 | 您所在的位置:网站首页 › 离子的口诀 › 人教版九年级化学 |
人教版九年级化学
|
初中化学的重点是酸碱盐,而酸碱盐的学习离不开离子共存的知识点。对于酸碱盐之间的反应,其实大部分的反应都是在溶液中以离子的形式进行的反应,而且判断两种化合物是否能够发生复分解反应的依据就是,物质中的阴阳离子相互交换结合后是否有水、气体或者沉淀生成。因此,酸碱盐的学习基础----离子共存及其重要。 首先要理解离子间不能共存的条件:即两种离子相互作用时,如果有气体、水或沉淀生成,则这两种离子不能在同一溶液共存,即不共存的离子对能够结合反应生成水、气体或者沉淀。 初中化学阶段常见的不共存离子如下: 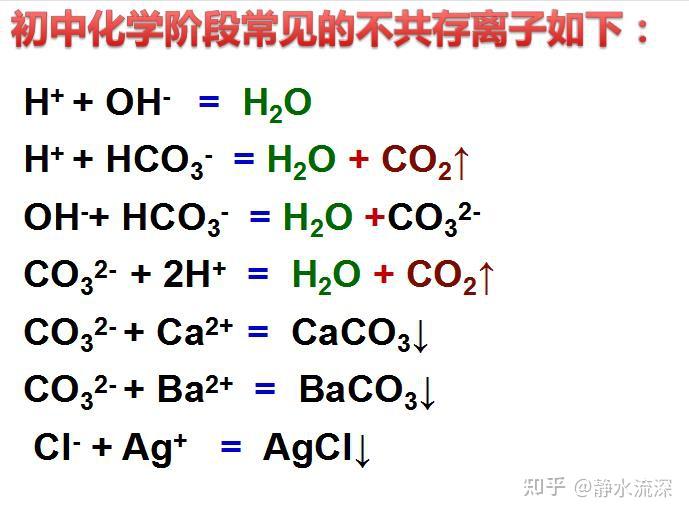  另外,在做离子共存的题目时,一定要注意题干给出的条件,比如原溶液是酸性,则溶液中还有氢离子H+,如果溶液呈碱性,则溶液中含有氢氧根离子OH-;有颜色的离子都不能在无色的溶液中存在(Fe2+浅绿色 、Fe3+浅黄色、 Cu2+蓝色 、 MnO4-紫红色)。这些条件也需要认真考虑是否符合题意。 简单的附几道例题以供练习: 1、下列离子组中,能大量共存的是:( ) A.Na+、NH4+、Cl-、OH- B.H+、Fe2+、SO4 2-、NO3- C.Cu2+、Ba2+、Cl-、SO42- D.Na+、Ca2+、NO3-、HCO3- 2、下列各组离子中,在碱性溶液里能大量共存,且溶液为无色透明的是:( ) A:K+、MnO4-、Cu2+、SO4 2- B:Na+、CO32-、NO3-、Cl- C:K+、Cu2+、SO42-、HCO3- D:K+、Na+、Cl-、SO4 2- 3、下列各组物质在溶液中能够大量共存的是:( ) A. BaCl2 NaCl H2SO4 B. H2SO4 NaCl Na2CO3 C. Na2SO4 KNO3 NaOH D. NaOH H2SO4 HCl 4、 下列各组物质在水溶液中不反应(即能共存)的是:( ) A. FeCl3、FeSO4、KOH B. HCl、HNO3、AgNO3 C. NaNO3、NaCl、NaOH D. CaCl2、BaCl2、Na2SO4. 5、下列各组物质能在NaOH溶液中共存的是:( ) A. KCl、NaNO3、Ba(NO3)2 B. SO3、BaCl2、HCl C. NaCl、MgCl2、KNO3 D. Na2SO4、K2CO3、KCl 离子对的学习,对于酸碱盐之间的化学方程式的学习也有很大的补充。根据离子之间的反应,补充搭配的阴阳离子,就可以写出对应的物质,这样就可以避免死记硬背,以不变应万变。 比如:  CO3 2-对应的物质可以是Na2CO3,Ca2+对应的物质有CaCl2和Ca(OH)2,那我们就可以联系到常考的两个化学方程式:CaCl2 + Na2CO3 = CaCO3 ↓ + 2NaCl ;---常考在粗盐提纯中。 Ca(OH)2 + Na2CO3 = CaCO3 ↓ + 2NaOH ;常考在Na2CO3和NaOH的相互转化中。 当然,像这样的例子还有很多,平时在学习的过程中,多观察,多对比记忆,会有很好的效果。 今天写在整理在这里,后续再整理关于物质的除杂问题! 码字不易,多多关注和点赞! |
【本文地址】