| 如何写一份完美的SAE报告! | 您所在的位置:网站首页 › 病例处置怎么写 › 如何写一份完美的SAE报告! |
如何写一份完美的SAE报告!
|
【本文参照的法规为2003版GCP,部分内容在2020版GCP中的规定有所变化,后续再分享给大家】 我知道不管是CRC还是CRA,对SAE都非常不待见, 看到SAE,都是  图片来源:网络 图片来源:网络但是,  图片来源:网络 图片来源:网络还是要乖乖爬起来写SAE报告!!! 好,回到正文,SAE报告类型分首次报告、随访报告、总结报告。 先上报告本体: 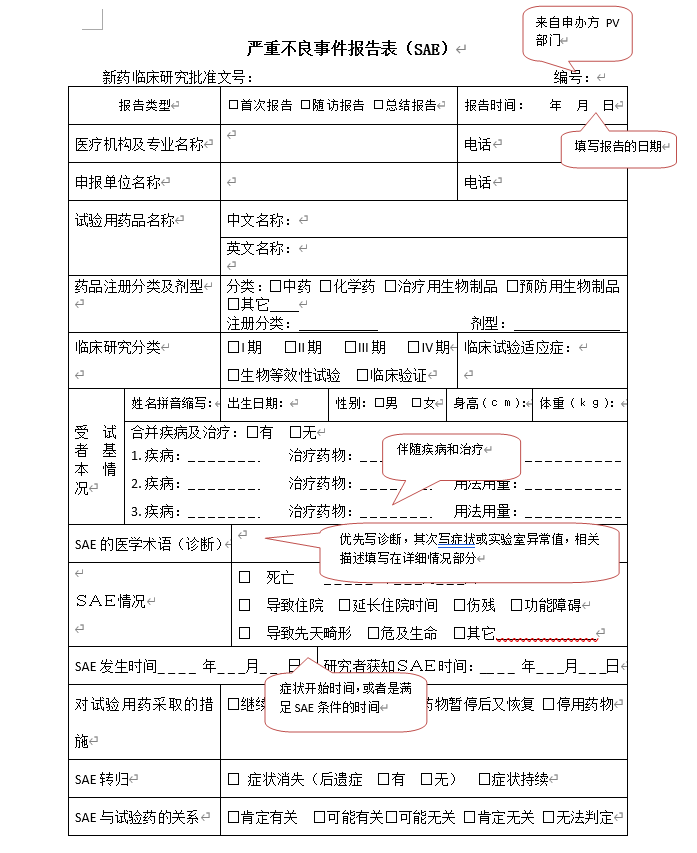 是不是看着很复杂,没错,就是很复杂。 在SAE 报告详细情况描述部分,需要包含: 1. 人口学特征 2. 临床试验剂量和服药持续时间 3. 合并用药 4. 现病史、既往史、过敏史、既往用药史 5. 不良事件及开始时间 6. 实验室检查或体格检查 7. 不良事件的记录(名称、起止时间、严重程度、相关性、转归等) 惯例给大家写了个模板~~希望能够帮到大家:  图片来源:网络 图片来源:网络段1:受试者信息、临床试验信息、试验药物信息 1001(入组号) 受试者XXX( 姓名缩写),女(性别),诊断为XXX(疾病诊断),于XXXX年XX月X日,签署知情同意书,参加“XXX(临床试验名称)”筛选,符合入组标准,不符合排除标准,XXX年X月X日分配随机号:XXX,XXX年X月X日C1D1给药,具体用药情况(XXXmg vgtt,目前为止共计用药X个周期等)。合并疾病XXX,合并用药XXX(此处指合并疾病的合并用药)。 段2:对SAE按时间线进行详细描述。 XX年X月X日,受试者出现XXX症状,XX年X月X日来院就诊,诊断为XXX。XX年X月X日实验室检查结果XXX。XX年X月X日因XXX(SAE名称,需与报告中相对应)收治入院。入院后治疗措施,入院后检查及结果等。 段3:研究者判断。 研究者XX年X月X日获知该信息(本院本科室住院的不用写了),SAE和试验药物的关系,如果和药物可能无关,考虑和XXX有关,对试验药物采取的措施(继续用药,暂停用药,减量,停药),SAE转归。 PS :几个小点需要注意的 1、症状作为SAE名称时,最好能写清楚该症状的级别,如三级呕吐。  图片来源:网络 图片来源:网络2、如果有多个诊断要分开上报SAE。 不要嫌麻烦,不然后面你会更麻烦!! 3、报告首选传真,无论成功还是失败都需要保留回执。建议无论传真是否成功,都发送邮箱并保留回执。传真失败的情况下发送EMS,保留底单。 (不过现在新版的GCP下,SAE不用再报给省局、国家局。全国各家临床试验机构已经更新了自家的SAE上报办事指南,现药研社APP已经上线“全国各家临床试验机构SAE/SUSAR要求汇总”,一键查询,让SAE上报更加顺畅。) 来6万临研人在用的药研社,一起为中国临床试验行业助力~ 
|
【本文地址】
| 今日新闻 |
| 推荐新闻 |
| 专题文章 |