| 郑海荣&刘斌 Adv. Mater.: NIR | 您所在的位置:网站首页 › 海肽光治疗系统 › 郑海荣&刘斌 Adv. Mater.: NIR |
郑海荣&刘斌 Adv. Mater.: NIR
|
(a) P1RGD NPs的制备和体内脑肿瘤光热疗法和光声成像原理; (b) P1RGD NPs的DLS和TEM图; (c) P1 NPs和P1RGD NPs的UV-vis图; (d) 1064 nm(1 W. cm-2)激发下不同浓度P1 NPs的光热加热效果; (e) P1 NPs的循环光热加热和冷却时间图。 图二、P1 NPs和P1RGD NPs的体外实验效果对比
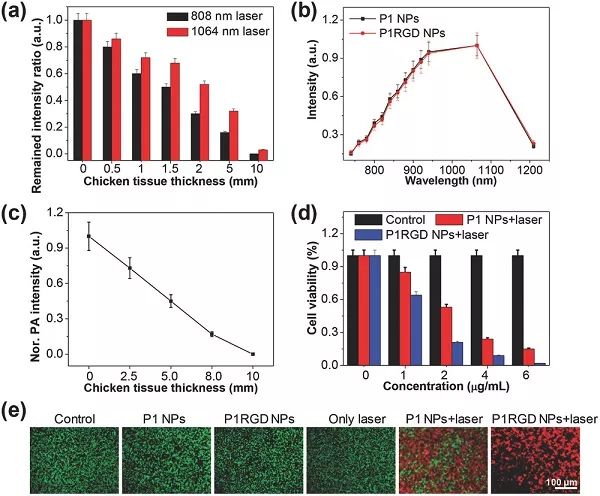
(a) 808和1064 nm在不同厚度的鸡组织的穿透效果的定量结果; (b) P1 NPs和P1RGD NPs悬浮液的体外PA光谱; (c) 1064 nm在不同厚度鸡组织中P1 NPs穿透深度实验的定量结果; (d) 1064 nm(0.8W cm-2)照射下体外光热治疗5 min的定量结果; (e) 体外光热疗法的荧光图。 图三、P1 NPs和P1RGD NPs的小鼠体内实验效果对比
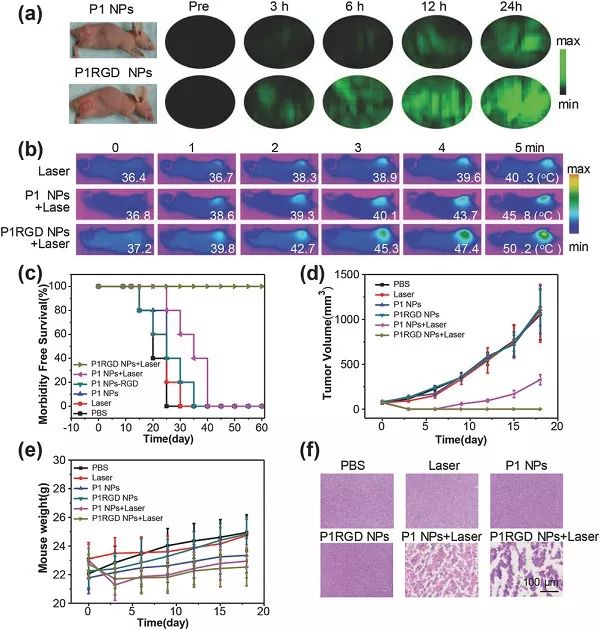
(a) P1 NPs和P1RGD NPs注射后的不同时间点,小鼠在皮下U87异种移植肿瘤模型中的体内非侵入性PA成像; (b) 光热处理5 min小鼠的红外热图像; (c) 不同组小鼠的存活曲线; (d) 肿瘤大小曲线; (e) 小鼠体重变化曲线; (f) H&E染色用PTT处理过的小鼠的肿瘤切片图。 图四、P1 NPs和P1RGD NPs治疗GBM的效果对比
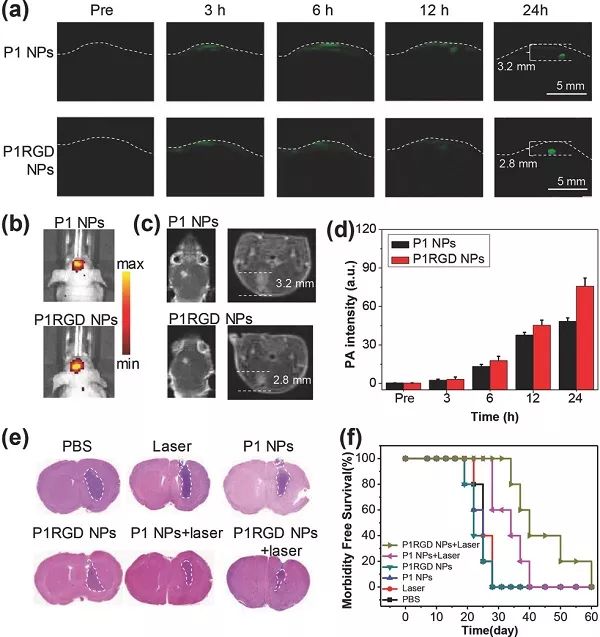
(a) NPs注射后不同时间点小鼠脑肿瘤的头皮和头颅无创PA成像; (b) 不同组进行PA成像之前,携带荧光素酶标记的神经胶质瘤细胞的小鼠的生物发光图像; (c) 小鼠脑中不同组织的MRI图像; (d) NPs给药后不同时间点肿瘤PA强度的定量结果; (e) 第19天PTT治疗后脑切片的H&E染色结果; (f) 光热处理后小鼠的存活率。 【小结】 首次研究穿过头皮和颅骨的NIR-II光热疗法并开发了一种有效的脑瘤治疗范例,使用活性靶向配体修饰的NIR-II共轭聚合物纳米颗粒进行精确的光声成像引导。纳米颗粒具有良好的光稳定性、优异的生物相容性、强光捕获能力和良好的光热转换性。与常用的808 nm PTT相比,1064 nm能更有效地穿透颅骨和头皮,有低于激光安全极限的治疗必需功率密度值。实验研究证实,与使用未修饰的纳米颗粒的情况相比,c-RGD NPs可以实现活跃的脑肿瘤靶向,进一步显着增加光声成像对比度以及信噪比高达90,改善了原位脑肿瘤模型的治疗效果。总之,具有光稳定性和良好生物相容性的NIR-II共轭聚合物纳米颗粒有望通过双光声成像和光热疗法以精确和有效的方式用于脑肿瘤治疗。 文献链接:Through Scalp and Skull NIR-II Photothermal Therapyof Deep Orthotopic Brain Tumors with Precise Photoacoustic Imaging Guidance(Adv. Mater., 2018,DOI: 10.1002/adma.201802591). 本文由材料人生物材料组小胖纸编译。 cailiaokefu返回搜狐,查看更多 |
【本文地址】