| 毛囊干细胞最新研究进展 | 您所在的位置:网站首页 › 日本毛囊技术最新消息 › 毛囊干细胞最新研究进展 |
毛囊干细胞最新研究进展
|
随后研究人员鉴别出了两种药物,当将药物作用于小鼠皮肤时,研究者发现,药物能够以不同的方式来影响毛囊干细胞从而促进乳酸生成;第一种名为RCGD423的药物能够激活名为JAK-Sat的细胞信号通路,将细胞外部的信息传输到细胞核中,研究者表示,JAK-Sat的激活能够增加乳酸的产生并且驱动毛囊干细胞激活以及头发生长;而另外一种名为UK5099的药物则能够阻断丙酮酸盐进入线粒体中,从而就能够驱动毛囊干细胞中乳酸的产生,并且加速小鼠头发的生长。 2.青岛农大新成果:防晒霜添加剂损害毛囊干细胞 doi:10.1080/17435390.2017.1310947 转眼之间天气开始炎热起来,很多爱美女士已经迫不及待地开始使用防晒霜了。近年来,“防晒霜到底对身体有没有害”一直是热门话题,不过即使是“有害论”持有者,一般认为的害处也只是“对皮肤刺激较大、容易堵塞毛孔、容易滋生暗疮粉刺、容易出现过敏症状”等。 近日,青岛农业大学教授沈伟课题组在国际著名学术期刊《纳米毒理学(Nanotoxicology)》上发表研究论文,系统阐述了涂抹在皮肤表面的防晒霜添加剂纳米氧化锌如何通过毛囊结构侵入皮肤组织,并对皮肤组织产生消极影响。 “纳米氧化锌具有特殊的物理性质,涂抹到皮肤表面之后可以有效吸收紫外线UVA和UVB,防止皮肤紫外线损伤。而且其涂抹到皮肤上后呈透明状,不会反光,也就是看上去不会油乎乎的,比较符合爱美女性的需求,所以这些特性使纳米氧化锌成为一种常用防晒霜添加剂。”沈伟告诉记者,据统计,世界范围内每年大概有2000吨金属氧化物纳米颗粒被投入到皮肤护理产业中,作为一种防晒霜添加剂使用。而已有研究表明,哺乳动物细胞在体外培养条件下添加纳米氧化锌,会导致细胞发生程序性死亡,造成严重的细胞损伤。 “而涂抹在皮肤表面的纳米氧化锌颗粒能否穿过皮肤屏障对机体造成损伤,此前还不是很清楚。”正因此,沈伟课题组通过小鼠皮肤涂抹纳米氧化锌和毛囊干细胞体外培养实验,系统阐述了涂抹在小鼠皮肤表面的纳米氧化锌通过毛囊结构侵入皮肤组织的损伤途径。研究发现,周期性的涂抹纳米氧化锌会导致这些纳米颗粒积累在小鼠毛囊中,而随着积累浓度的升高,最终导致纳米氧化锌对毛囊中干细胞的分化潜力产生损伤,影响正常的皮肤稳态。 3.三篇Science论文探讨脱发与毛囊干细胞衰老的关系 doi:10.1126/science.aad4395;doi:10.1126/science.aad5440; doi:10.1126/science.aaf1635
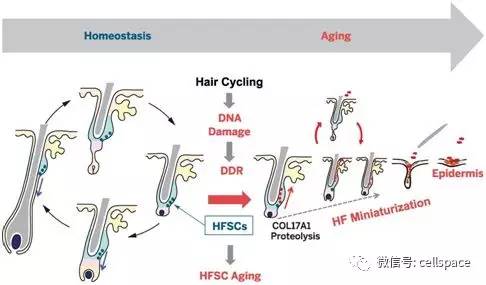
根据两项新的研究,人们头发脱落的原因可能与毛囊干细胞(hair follicle stem cells, HFSCs)衰老相关联。这两项研究同时发表在2016年2月5日那期Science期刊上,文章标题分别为“Hair follicle aging is driven by transepidermal elimination of stem cells via COL17A1 proteolysis”和“Foxc1 reinforces quiescence in self-renewing hair follicle stem cells”。 尽管众所周知,寿命更长的哺乳动物会脱发,但是这种命运背后的机制一直是个谜。HFSCs产生毛囊,而毛囊产生毛发。随着时间的推移,HFSCs重复地维持毛发生长。令人吃惊的是,科学家们已在小鼠实验中证实HFSCs抵抗衰老。为了更好地理解HFSCs可能在衰老相关毛发脱落中所起的作用,日本东京医科牙科大学Hiroyuki Matsumura及其同事们研究了毛发加速脱落(accelerated hair loss)模式小鼠的毛囊。在对18个月大的这些小鼠---它们在此阶段开始毛发脱落---的皮肤进行分析后,他们证实这些动物的毛囊变得小型化,而且毛发数量和厚度下降。 研究人员猜测罪魁祸首是产生毛囊的HFSCs发生变化。进一步的研究---包括参与HFSCs维持的关键性基因---证实了他们的猜测。HFSCs中积累的DNA损伤似乎在促进它们发生变化中发挥着作用。一种在调节HFSCs中发挥着特别重要作用的基因是COL17A1;在剔除这个基因的基因工程小鼠体内,HFSCs被清除了。 在第二项研究中,来自美国科罗拉多大学的Li Wang等人鉴定出一个HFSCs用来启动毛发生长的转录因子,即Foxc1。在成年小鼠的毛发生长周期,HFSCs周期性地在激活阶段和静止阶段之间切换来维持干细胞群体和产生新的毛囊。通过操纵Foxc1在毛发生长周期不同阶段中的表达,研究人员发现这种转录因子促进控制HFSCs静止的两个关键机制---Nfatc1和BMP---之间的信号转导。这些发现表明静止的HFSCs可感知它们的细胞状态变化,并利用短暂的基因激活来维持它们的身份。 归纳在一起,这两项研究有助人们进一步理解毛发生长。与此同时,来自中国重庆大学的Mingxing Lei和来自中国医药大学的Cheng-Ming Chuong在同期的Science期刊上发表了一篇标题为“Aging, alopecia, and stem cells”的观点文章,探讨了衰老、脱发和干细胞之间的关系。 4.Genes & Dev:鉴别出基因brca1可以调节皮肤毛囊干细胞存活 doi:10.1101/gad.206573.112 近日,刊登在国际杂志Genes and Development上的一篇研究报告中,来自布鲁塞尔自由大学的研究者揭开了BRCA1在调节皮肤干细胞存活上的一个新型角色。我们的DNA可以储存遗传信息,但是其会不断受到损伤,如果没有进行合理修复,DNA损伤便会导致细胞死亡,进而会导致组织老化疲惫,诱发基因突变,引发细胞无限增殖和癌症发生。Brca1是一个调解DNA修复的关键基因,其突变后会引发家族性或者散发性的乳腺癌和卵巢癌。 这项研究中,研究者揭示了Brca1在维持毛囊干细胞上所扮演的新角色和发挥的关键作用。研究者Peggy Sotiropoulou和其同事研究揭示,在表皮中剔除乳腺癌相关基因Brca1后,毛囊细胞就会表现出高水平的DNA损伤以及细胞死亡,这将诱导毛囊干细胞增殖过度以及疲惫,从而引发毛囊变性。 相反,位于表皮中其他类型的干细胞,其可以形成皮肤屏障以及皮脂腺,来维护皮肤因基因Brca1缺失后的正常功能,这就揭示了BRCA1在不同类型的成体干细胞中不同需求。研究者表示,我们很惊奇地看到,不同组织中不同类型的细胞可以对于相同的基因剔除表现出不同的效应,就比如是对于DNA修复的关键基因。 5.ASCBAM:陈明冲等预测毛囊干细胞再生机制 根据2011年12月7日在美国丹佛市召开的美国细胞生物学协会年会(American Society for Cell Biology Annual Meeting)新闻,美国南加州大学(University of Southern California)医学博士和哲学博士陈明冲(Cheng-Ming Chuong)说,人头发或者头发丢失是唤醒人身体每个毛囊中干细胞的激活物和让它们休眠的抑制物之间终生拔河的结果。 基于去年四月《科学》(Science)杂志报道的研究,陈明冲和他的同事们与英国牛津大学数学家菲利普-迈尼(Philip Maini)博士和露丝-贝克(Ruth E. Baker)博士合作使用一种“细胞自动机(cellular automaton)”模型来描述毛囊的群体行为。 使用这种预测性模型,研究人员发现,人每个成体毛囊在没有大环境(macro-environment)中附近毛囊的帮助下能够依靠它的内在性促进生长的信号。相反,兔子和小鼠毛囊的生长依赖于来自周围毛囊的信号。 这个细胞自动机模型是由正常的数学自动机网格组成的,其中每个自动机代表着一个毛囊而且该毛囊处于它的四个周期性阶段之一。每个自动机周围是8个自动机,它们都是一个毛囊的邻居。 根据决定人头皮或者动物毛皮上头发是否涉及称作毛发生长阶段(anagen phase)的生长浪潮或者仍然处于毛发休止阶段(telogen phase)的规则,每个细胞自动机状态发生变化。在合适的条件下---冬季或者有机体生命中一个新的生理阶段,如青春期---,一个集体性再生浪潮席卷皮肤,激活单个毛囊中的毛干细胞及其前面成十上千的那些干细胞。 在其他季节或生命阶段,单个毛囊可能被它们大环境中的抑制物一直封锁于静止阶段。抑制物水平部分是由皮下脂肪组织和中央内分泌系统调控的。这些多重调控层次在让毛干细胞保持静止状态的抑制性骨形态发生蛋白(bone morphogenic protein, BMP)信号传导和唤醒它们的激活性Wnt信号传导之间构建平衡。 陈明冲发现生长浪潮在兔子中稳健扩散,在小鼠中逐渐扩散,在人皮肤中则是随机性生长同时伴随着毛囊丢失。这些数据提示着一种新的治疗雄激素源性脱发(androgenic alopecia)---在老年男人中一种最为常见的脱发---的方法:改善它们的环境而不是移植干细胞可能更容易让毛囊在此生长。 6.Nature:研究发现生物钟对毛囊干细胞的控制 doi:10.1038/nature10649
存在于小鼠皮肤中特定小环境中的表皮干细胞,可以确保皮肤的动态平衡得到高效维持。毛囊隆突中的干细胞负责毛囊再生和伤口愈合。它们产生一组异质性细胞——比如说这些细胞在其对内部和外部提示的反应能力方面就是异质性的。 由Salvador Benitah及其同事进行的这项研究表明,生物钟通过调控毛囊隆突干细胞对其微环境的反应能力来控制它们的激发状态和异质性。这意味着,始终都会有一组“准备好了”的细胞来对激发刺激做出反应,同时防止该微环境内的所有干细胞都变得具有响应能力。表皮干细胞若受到扰动,会影响组织的长期平衡,并使组织容易生成肿瘤。 7.JCI:毛囊干细胞缺陷可能是导致脱发的一个主要原因 doi:10.1172/JCI44478 美国宾夕法尼亚大学的研究人员在新一期美国《临床检查杂志》上报告说,毛囊干细胞缺陷使其无法产生让头发生长的源细胞,从而导致脱发。对男性来说,这种现象称为男性秃顶,其症状为头部开始掉发,发际线后退,最终导致全秃;对女性来说,其症状为头发越来越稀,但很少导致全秃。 研究人员分析了54名40岁至65岁男子的头发和头皮组织,结果发现,无论是脱发还是没有脱发的头皮组织中,毛囊干细胞的数量都是相同的,所不同的是,脱发头皮组织中的毛囊干细胞没有产生让头发生长的源细胞,这表明毛囊干细胞产生了缺陷,使头皮无法长出头发。 领导这一研究的乔治·科斯萨利斯说,此前研究以为导致脱发的原因是毛囊干细胞已经不存在了,但最新的研究发现,毛囊干细胞还在,只是出现了缺陷。 8.J. Cell. Biochem.:人类毛囊干细胞可修复神经 doi:10.1002/jcb.22204 AntiCancer公司的一个小组所领导的研究人员已证实,人类毛囊所衍生的干细胞可修复小鼠断裂的神经。来自毛囊的干细胞注射入受损的神经后,可分化为Schwann细胞,这种细胞可促进神经生长,使神经得以续接。修复后的神经可恢复功能,小鼠可正常行走。该研究的协作方是日本神奈川县相模原市的北里大学医学院。 在这之前,AntiCancer公司和北里大学的科学家证实,毛囊干细胞具有多能性,可分化为众多类型的细胞,包括神经元,因此被命名为hfPS (毛囊多能干) 细胞。 AntiCancer公司副总裁兼首席营运官Charlene M. Cooper说:“从开发再生药物角度而言,与胚胎干(ES)细胞和诱导多能干(iPS)细胞相比,hfPS细胞具有重要的优势,因为它们易于从任何患者中换取,不引起免疫问题,不会诱发肿瘤,也无伦理问题。”该项研究已发表在当期的《细胞生物化学杂志》上。 9.Cell Stem Cell:毛囊干细胞在皮肤形成早期功能 doi:10.1016/j.stem.2008.05.009
尽管所有毛囊在小鼠出生时已经开始发育,但是毛囊峡部微环境在出生后3周仍不显著,此时小鼠已经具有完整的表皮毛发覆盖。因此,毛囊干细胞从何而来,它们是如何形成微结构的尚不清楚。此前,科学家认为这些细胞对于胚胎发育并非必需,因为毛囊来自于表皮,而不是峡部微环境。为了研究毛囊干细胞是否在发育早期就已经存在,以及其是否发挥作用,来自美国洛克菲勒大学的一组科学家进行了相关研究,并将结果发表在2008年7月3日出版的《细胞—干细胞》(Cell Stem Cell)上。 毛囊干细胞有多种标记物,这些标记物能帮助研究人员了解干细胞的特征和行为等。其中包括广泛应用的CD34,以及转录因子Lhx2、Sox9、Tcf3、Nfatc1等。与CD34不同的是,这些转录因子的表达开始于毛囊形成时期。在研究中,科学家利用了基因技术、细胞生物技术等对毛囊干细胞进行了分析。结果发现,慢周期细胞(slow-cycling cell)在皮肤发育早期就已经出现,并且表达干细胞标记物,接着形成成年干细胞。为了测试这些早期的慢周期细胞是否起到了干细胞作用,研究小组利用Sox9-Cre作为基因标记,实验结果表明,表达Sox9的细胞最后能形成所有皮肤上皮细胞系,而Sox9对于干细胞分化是必需的。 因此,毛囊干细胞在毛囊形成最早期阶段就发生分化,并且初期的干细胞分化依赖于Sox9。更重要的是,早期的毛囊干细胞对于3种皮肤上皮细胞系形成都有贡献,一旦缺少这些细胞,毛囊和皮脂腺的正常形态发生就会受到阻碍,而同时上皮损伤修复也会被影响。 10.Cardiovascular Research:头发毛囊干细胞可用于血管再生 doi:10.1093/cvr/cvn059 在不远的将来,临床医生不必东找西寻,只需从患者头上拔根头发,就能进行血管再生手术,因为通过生物工程,头发毛囊中富含的干细胞可以发育成新的血管或皮肤组织。美国纽约州立大学水牛城分校的科学家在3月份出版的《心血管研究》(Cardiovascular Research)杂志上发表了他们的最新研究成果。 水牛城分校工程与应用科学院化学和生物工程系副教授斯特里尔斯·安德烈亚第斯博士是该论文的作者之一。他的研究小组从绵羊头发毛囊中分离出干细胞,并利用其中含有的平滑肌细胞,使其发育成新的脉管系统。最近获得的实验数据表明,从人的头发毛囊中提取出的干细胞可以分化成可收缩的平滑肌细胞。安德烈亚第斯称,由头发毛囊中的平滑肌祖细胞制备的工程血管具有扩张和收缩的性能,这使它成为心血管组织再生工程的理想材料。这说明,利用头发毛囊中的干细胞来生成新的血管或皮肤组织的方法是切实可行的。 通过生物工程,头发毛囊中的细胞不仅可以长成新皮肤,用于治疗烧伤患者;也可以再生出心脏组织,用于心脏病患者的血管移植。另外,因为平滑肌细胞存在于包括膀胱、腹腔、肠胃和呼吸道等众多的组织和器官中,所以,这个新的易获得的干细胞源也将有助于对这些器官损害的再生治疗。 11.Nature:毛囊干细胞与毛发再生 doi:10.1038/nature06457 长毛的哺乳动物也许能教给我们关于如何控制干细胞复制的重要知识:它们的皮肤含有数以千计的毛囊,这些毛囊经历着从生长到休息的周期,而且每个毛囊干细胞在程序上就以某种方式决定了它们都能协调细胞分裂。现在,骨形态发生蛋白(BMP)和它们的抑制因子已被识别出在控制毛囊活动周期中起中心作用。对那些剔毛后毛发再生的小鼠来说,BMP2和BMP4都会调控各个毛囊中毛发的生长,并与附近的毛囊进行协调。这对信号分子还符合对“chalone”的描述,后者是50年前就有人假设的分子,用以解释毛发生长的模式。这项工作对于癌症形成和干细胞工程研究有参考意义,因为很多这类研究都假设小鼠皮肤在长时间实验中都是均匀一致的。 来自南加州大学Keck医学院(Keck School of Medicine,生物谷注),英国牛津再生系统生物学中心等处的研究人员发现了毛发再生过程中调控干细胞活 性的新机制,这对于干细胞研究,以及对于理解再生过程中干细胞活性是如何受到调控的意义重大,而且也打开了毛发再生调控,以及最终的器官再生调控的一个新尺度。这一研究成果公布在昨天出版(1月17日)的《Nature》杂志上。 12.重庆大学、第三军医大毛囊干细胞研究新进展 重庆大学生物工程学院院长杨力教授和第三军医大学细胞生物教研室杨恬组成的联合研究组在毛囊干细胞的纯化、诱导分化研究上取得了新成果。 杨力教授的研究组利用免疫磁珠法对大鼠CD34+毛囊干细胞进行了纯化。免疫磁珠分选(mamnetic activated cell sorting, MACS)技术是一种集合了免疫学、细胞生物学、磁力学等知识于一体的高度特异性细胞分选技术,其高度特异性来自抗体对抗原的特异性识别。 该研究组通过对毛囊细胞悬浮进行CD34抗体标记和磁珠标记,使细胞悬浮通过分选柱,然后用缓冲液冲洗分选柱,把所有未标记的细胞被冲洗掉来达到分选的目的。对培养7天的毛囊细胞、毛囊组织细胞和经CD34分选后得到的CD34+细胞和CD34-细胞进行扫描电镜观察,发现这些细胞在形态上并无明显差异,但只有CD34+细胞表面有磁珠颗粒。 荧光显微镜下观察分选得到的细胞,CD34+细胞可见强红色荧光,而CD34-细胞只有很弱的、几乎不可见的荧光。进行细胞培养后发现,CD34+细胞较CD34-细胞活性好,细胞折光性强。免疫组化分别检测CD34+细胞和CD34-细胞β1-integrin、CD34和α6-integrin的表达,Image-Pro Plus5.1软件分析,结果表明CD34+细胞平均光密度(AOD)值大于CD34-细胞平均光密度(AOD)值,差异显著,说明CD34+细胞属于低分化细胞。 另外,杨力教授的研究组还研究了Pax6在毛囊干细胞向着角膜上皮细胞诱导分化中量的变化和功能。 实验中,他们用角膜缘组织匀浆液对培养的毛囊bulge区细胞行诱导培养,并在培养过程中对诱导培养的毛囊bulge区细胞据培养时间进行规律性间断检测核蛋白因子pax6表达量的变化,并协同检测毛囊干细胞标记性因子k15、CD34、α6以及角膜上皮细胞标记物k12的表达及其表达变化。 然后,研究组通过流式细胞法测定诱导转分化的阳性细胞率。免疫组化及免疫荧光结果显示k15、CD34、α6由诱导培养前的阳性表达逐渐转为阴性表达,而k12的表达则由阴性转为阳性。这意味着由毛囊干细胞向角膜上皮细胞的诱导转分化是成功的。而在诱导培养过程中pax6的表达存在量的变化,且其表达逐渐增强。这提示我们pax6这种核蛋白因子在转分化过程中起到了一定的作用。 13.PNAS:科学家用毛囊干细胞治愈神经损伤 doi:10.1073/pnas.0508440102 美国和日本科学家21日报告说,他们成功地使毛囊干细胞分化成神经胶质细胞,并使因坐骨神经损伤而瘫痪的实验鼠能正常行走。科学家说,这一研究成果显示毛囊干细胞有更广泛的医疗应用潜力。 美国麻省理工学院、加州大学圣迭戈分校和日本北里大学的研究人员在新一期美国《国家科学院学报》上发表论文说,他们在实验中成功地诱导毛囊干细胞分化成了许旺氏细胞。许旺氏细胞是末梢神经纤维的鞘细胞,它们排列成串,一个接一个地包裹着神经纤维的轴突。许旺氏细胞形成髓鞘保护神经髓,它外表面还有一层促进神经再生的基膜。 然后,研究人员将毛囊干细胞生成的许旺氏细胞注射到坐骨神经损伤的瘫痪实验鼠体内。一段时间后,他们发现实验鼠已能正常行走。解剖显示,许旺氏细胞已在实验鼠坐骨神经的轴突外围形成了髓鞘。而在新形成的髓鞘内,原先断裂的神经轴突已经修补好了。研究人员推测,这是因为毛囊干细胞分化成的许旺氏细胞刺激了神经轴突的生长,促使神经损伤愈合。 14.美国发现:毛囊干细胞可演变为神经干细胞 doi:10.1073/pnas.0501263102 美国研究人员发现,在毛囊中发现的干细胞可以生长为神经细胞,这项发现可能被用于医疗方面。 研究人员发现,在老鼠胡须的毛囊中采集的干细胞可以生长为神经元以及其他神经细胞,像星形细胞、少突细胞和皮肤细胞、平滑肌细胞以及被称为黑素细胞的色素生成细胞。这项发现已经发表在了美国《国家科学院院刊》上。该发现提供了主细胞的另一潜在源。科学家希望它能提供一个良好的新组织和器官移植源。 已知的最好的干细胞源是骨髓,但研究人员希望能找到更为容易采集干细胞的其他部位。他们想通过实验弄清楚来自不同源的干细胞的质量是否会有所不同。干细胞是人体的主细胞,在人体的周身都可以找到所谓的成体干细胞。一个较为有争议的干细胞源是数天大的胚胎。圣地亚哥抗癌药物研究公司的罗伯特·霍夫曼和他的加州大学及麻省理工学院的同事说,在未来的某个时候有可能将从人体毛囊中采集到的干细胞培养成组织移植物。 此前研究人员在毛囊中发现了干细胞,基于这项发现,这个研究小组又对毛囊中的干细胞进行了深入研究,于是又有了这项新发现。去年9月,由美国哥伦比亚大学霍华德·休斯医学研究所与纽约洛克菲勒大学组成的一个研究小组发现,来自毛囊中的干细胞可以生长为头发、成片的皮肤以及汗腺。 今年3月,宾州大学医学研究所的一个研究小组发现,在老鼠胡须囊中采集的干细胞被移植后可生长为头发以及其他类型的皮肤细胞。研究人员希望这种可用来进行移植的干细胞能对一系列的疾病提供治疗,像摧毁脑细胞的帕金森氏病,导致胰岛素产生细胞死亡的糖尿病或脊索损伤。返回搜狐,查看更多 |
【本文地址】