| 新高一化学丨计算:物质的量、摩尔质量! | 您所在的位置:网站首页 › 摩尔质量m等于什么 › 新高一化学丨计算:物质的量、摩尔质量! |
新高一化学丨计算:物质的量、摩尔质量!
|
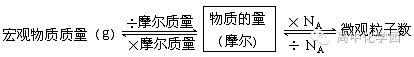
2、相对原子质量 : (1)定义:以12C原子质量的1/12为标准,其它原子的质量跟它相比较所得到的比值,作为这种原子的相对原子质量。(2)两种原子的质量之比与其相对原子质量之比有何关系: 二者相等。因为任何一种原子的相对原子质量,都是以12C质量的1/12为标准所得的比值。所以,任何原子的质量之比,就等于它们的相对原子质量之比。 3、摩尔质量与相对原子质量(或相对分子质量)的关系: 摩尔质量以g·mol―1为单位时,在数值上与物质的相对分子质量或相对原子质量相等。 三、物质的量、阿伏加德罗常数、质量和粒子数目之间的关系
微课:摩尔质量 典型例题 一、物质的量及其单位(摩尔)、阿伏加德罗常数 例1.下列说法正确的是() A、物质的量就是物质的质量 B、阿伏伽德罗常数就是6.02×1023 C、1mol氧含有6.02×1023O2 D、科学上规定含有6.02×1023个粒子的任何粒子集体计量为1mol 【答案】D 例2.下列说法正确的是( ) A.阿伏加德罗常数是人们规定的数,没有单位 B.0.012 kg 12C中所含有的碳原子数的精确值是6.02×1023 C.H2O的相对分子质量为18,1 mol水的质量也是18 D.1.5 mol NaCl晶体中含有Na+数为9.03×1023 【答案】D 【练习】 (1)0.1 mol 碳约含有个碳原子; (2)3 mol 氧气约含有个氧分子,个氧原子; (3)1.5 mol 硫酸约含有个硫酸分子,个氢原子,个氧原子,个硫原子; (4)0.2mol氢氧化钡含有mol钡离子,mol氢氧根离子; (5)1.204×1024个水分子的物质的量。 (6)1 mol H2O 约含个水分子,个氢原子,个氧原子,个质子,个电子; 【答案】(1)0.1NA (2)3NA 6NA(3)1.5NA 3NA 6NA 1.5NA (4)0.2 0.4 (5)2mol (6)NA 2NA NA 10NA 10NA 二、摩尔质量 例3.下列说法正确的是() A.H2的摩尔质量是2 g B.B.1 mol H2O的质量是18 g/mol C.64g氧气的摩尔质量是32 g/mol D.2 g H2含1 mol H 【答案】C 【练习】 1、计算(1)24.5g H2SO4的物质的量是多少? (2)1.50mol Na2CO3的质量是多少? (3)4.9 g H2SO4中含有的氧原子数。 【答案】(1)0.25mol;(2)159g;(3)1.204×1023 【解析】 (1)n(H2SO4)=m/M=24.5g/98g/mol=0.25mol; (2)m(Na2CO3)=n·M=1.50mol×106 g/mol=159g; (3)据n=m / M可求出硫酸的物质的量: n(H2SO4)=4.9 g / 98 g·mol―1=0.05 mol 据n=N/ NA可求出硫酸的分子数: N=n NA=0.05 mol×6.02×1023/ mol=3.01×1022 1个硫酸分子中含有4个氧原子,则4.9 g H2SO4中含氧原子数为1.204×1023。 2、填空 (1)1mol Mg的质量是______ ,Mg的摩尔质量是_________ (2)Na+的摩尔质量是CO32-的摩尔质量是_________ (3)2molFe的质量是_____,1.5molSO2的质量是____。 (4)3.01 ×1022个OH-的物质的量为, 质量为 (5)1个H2O分子中有个电子,1mol H2O中有______ 个电子。 【答案】 (1)1mol Mg 的质量是24g ,Mg的摩尔质量是24g/mol (2)Na+的摩尔质量是23g/mol CO32-的摩尔质量是60g/mol (3)2molFe的质量是_112g____,1.5molSO2的质量是_96g___。 (4)3.01 ×1022个OH-的物质的量为( 0.05mol ), 质量为 ( 0.85g ) (5)1个H2O分子中有10 个电子,1mol H2O中有10NA个电子。返回搜狐,查看更多 |
【本文地址】