| 非小细胞肺癌立体定向体部放疗案例 | 您所在的位置:网站首页 › 复旦肿瘤医院放疗排队久吗 › 非小细胞肺癌立体定向体部放疗案例 |
非小细胞肺癌立体定向体部放疗案例
|
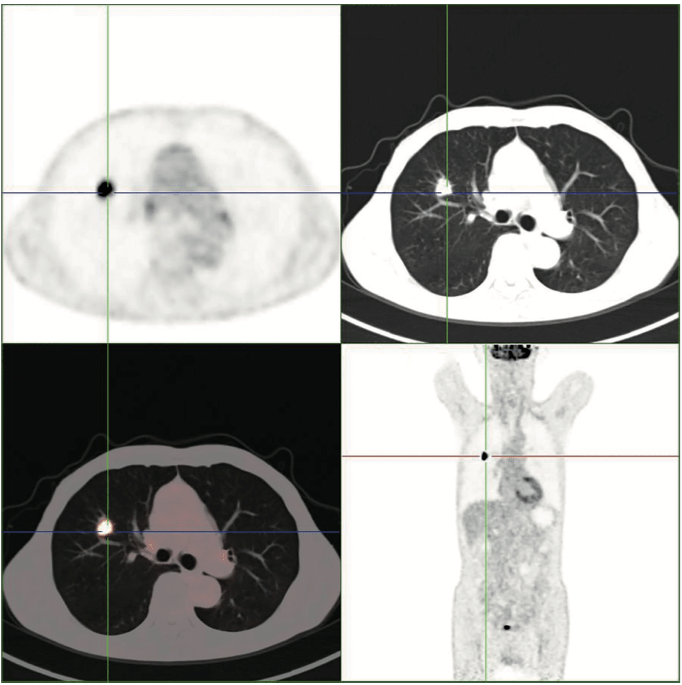
专科检查:胸廓对称,呼吸均匀,呼吸音清,未闻及干湿啰音,心律齐,心率72次/分,未闻及病理性杂音。 正电子发射断层扫描计算机成像技术(PET-CT)检查提示:右肺上叶实性结节影,约1.6 cm×1.5 cm,边缘短毛刺,放射性摄取异常增高(图1)。PET/CT诊断:①右肺上叶恶性肿瘤,氟代脱氧葡萄糖(FDG)高代谢。②左侧基底节区陈旧性脑梗可能;纵隔、两侧肺门淋巴结炎性增生;胰腺多发钙化灶伴胰管扩张,慢性胰腺炎可能;随访,左肾囊肿。
图1 PET-CT图像 右肺上叶实性结节影,约1.6 cm×1.5 cm,边缘短毛刺,放射性摄取异常增高。 (三)病理诊断 外院右上肺结节穿刺组织病理检查,切片邀复旦大学附属肿瘤医院病理会诊:(右肺上叶肿瘤,活检)结合原单位免疫标记,符合鳞状细胞肺癌(图2)。 诊断:右肺上叶鳞状细胞癌[T1bN0M0,ⅠA2期,美国癌症联合会(AJCC)/国际抗癌联盟(UICC)TNM分期第8版]。
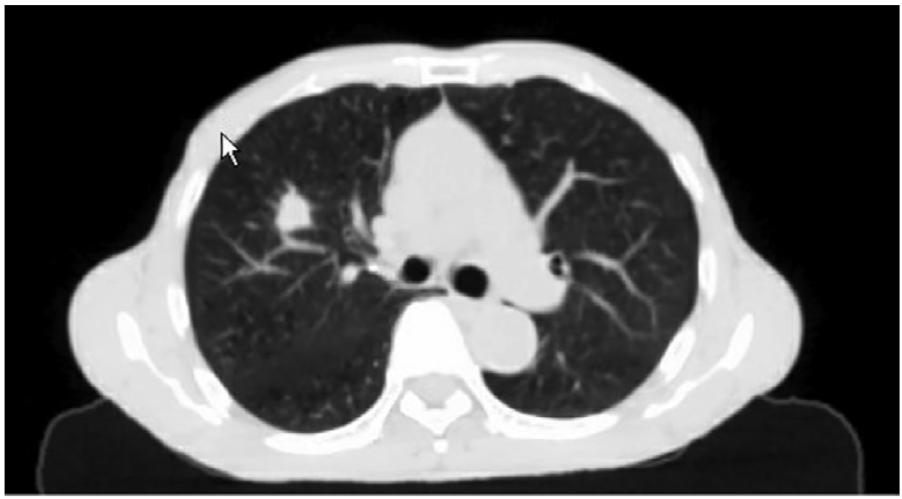
图2 右上肺结节CT影像 将右肺上叶结节活检,符合鳞状细胞癌。 二、治疗前准备 (一)体位与固定 患者仰卧位,双手上举,多功能板+真空垫固定。固定时尽量让患者保持舒适,以保证每次治疗有较好的重复性。 (二)CT模拟定位 (1)有条件的医院建议统一进行4D-CT定位扫描,无条件的医院用慢速CT替代。 (2)层厚≤3 mm。 (3)扫描范围至少应完整包括全肺而非仅仅肿瘤部位。 (4)可以根据肿瘤具体部位进一步上、下适当延伸(例如需要完整勾画臂丛神经)。 (三)参与定位人员 (1)定位CT室技术人员。 (2)参与靶区勾画和治疗实施的医生或至少是同一治疗组内具备立体定向体部放疗(SBRT)相关技术知识或有相关资质的医生。 (3)物理师提供技术咨询。 (四)呼吸运动评估 X线透视或4D-CT下评估该患者肿瘤随呼吸的运动在任意方向上的幅度均不超过5 mm,无须进行呼吸管理。幅度超过5 mm可使用内靶区勾画(internal target volume,ITV)的方法处理。幅度>1.5 cm可以考虑根据各放疗中心条件采取腹部压迫、呼吸门控技术、屏气技术、目标追踪技术等。 三、靶区勾画及剂量 (一)靶区勾画原则 大体肿瘤体积(GTV)根据胸部CT的肺窗进行勾画,软组织窗可用于区分邻近血管或胸壁结构。GTV勾画的准确性应从矢状位、横断位、冠状位分别判断。临床靶体积(CTV)=GTV。 建议窗宽与窗位:W=1 600和L=−600。 可参考增强CT进一步区分肿块与血管以达到肿瘤的进一步精确勾画,但 不建议增强CT上直接进行剂量计算。可以参考PET-CT,但不建议直接使用氟脱氧葡萄糖-正电子发射断层成像 (FDG-PET)图像界定大体肿瘤体积(IGTV)的边界。 IGTV: ①4D-CT重建MIP勾画IGTV。 ②当患者呼吸明显不规律或是肿瘤靠近软组织(如横膈),MIP重建可能 不能准确反映IGTV,需要通过其他时相的CT修改。 PTV:IGTV各个方向上均匀外扩5 mm。 IGTV、PTV、部分危及器官(OAR)勾画如图3所示。
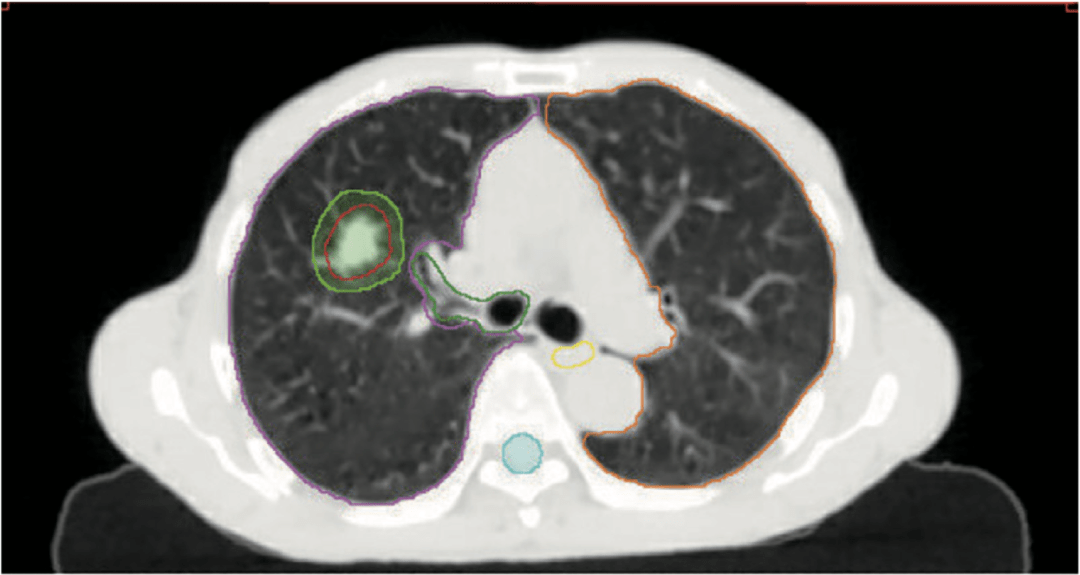
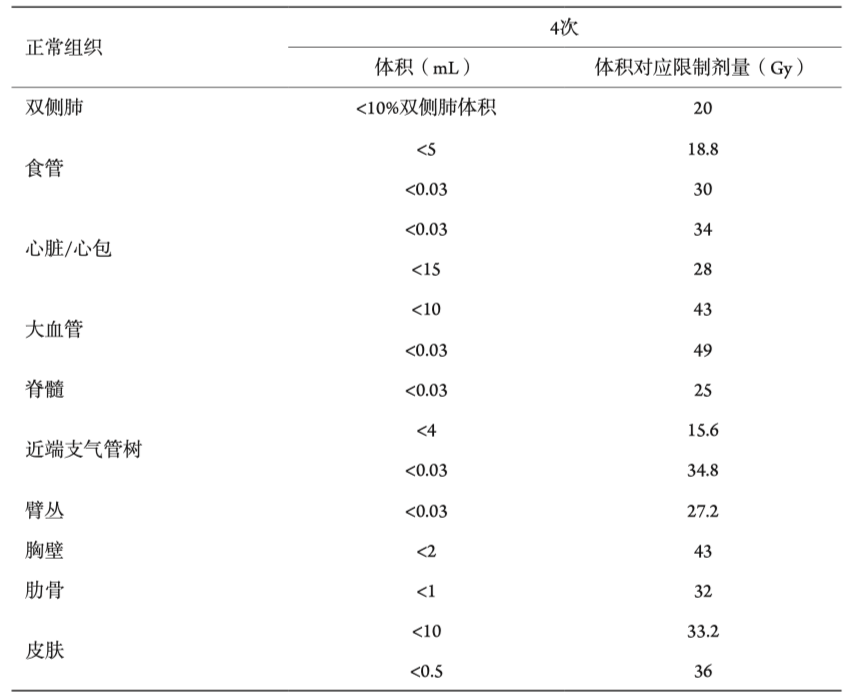
图3 IGTV、PTV、部分OAR勾画示意图 红色,IGTV;绿色,PTV;紫红色,右肺;橘红色,左肺;墨绿色,右侧支气管树;黄色,食管(纵隔窗下勾勒);蓝色,脊髓。 (二)放疗技术及剂量 采用SBRT技术,剂量及分割:Rx 12.5 Gy×4 Fx,TD 50 Gy,BED 10 = 112.5 Gy。 (三)正常组织限量 正常组织限量见表1。该患者正常组织限量参考RTOG 0915。其他分割剂量方案对应的正常组织限量可参考NCCN指南、SBRT正常组织限量英国共识和AAPM TG101号报告等。 表1 正常组织限量
四、讨论 对于一般的Ⅰ期非小细胞肺癌患者而言,除临床试验以外,目前的标准治疗仍然是根治性手术切除。对于手术风险较高的患者,SBRT可作为根治性切除的替代疗法,但对这样的病例仍然建议经包括外科医生在内的多学科医疗团队的讨论,并由主管医生与患者沟通,在患者充分了解利弊的情况下选择治疗方案,并签署知情同意书。对拟进行SBRT治疗的肺内病灶进行活检以获取病理学证据是非常重要的,尤其对于肺内存在多发病灶的情况,仅仅依靠影像学表现往往难以明确诊断和分期。对于无法获得病理证据的病例,需要进行多学科讨论,并结合病灶的大小、位置、肿瘤生长速度、影像学特点、患者吸烟史、既往是否有肺部恶性肿瘤病史等情况进行综合判断。治疗前结合包括PET-CT、脑部MRI、支气管内活检在内的基线评估非常重要,直接决定了分期的准确性。对于剂量分割的选择,需要根据病灶的位置和大小具体判断。因病灶可能毗邻的危及器官不同,因此,对于外周型病灶和中央型病灶需要考虑给予不同的剂量分割模式以期达到毒性和疗效的最佳平衡。 对于中央型早期非小细胞肺癌,增加分割次数有可能降低致命的毒性作用和不良反应。确定剂量时可考虑利用线性二次(linear quadratic,LQ)模型将物理剂量转换为2 Gy等效剂量或生物有效剂量(biological effective dose,BED)。虽然关于LQ模型是否适合大剂量照射存在一定争议,但临床数据显示经典的LQ模型依然可以参考。因此,目前经典模型计算的BED剂量仍在广泛临床应用。足够的BED是达到最佳肿瘤控制的基础,既往研究表明BED≥100 Gy时SBRT能达到更好的肿瘤局部控制率和长期生存率。 关于毒性的考量,目前临床实践中参考的剂量限制多数来源于毒性反应观察、理论推算以及有根据的猜测,而未经过验证。在参考表中信息时需悉知和考虑这一点。对于早期非小细胞肺癌的SBRT治疗,建议对外周型及中央型病灶的正常组织限量分开讨论,由于中央型或超中央型病灶SBRT治疗风险较高,毒性作用和不良反应数据较匮乏,业内对于这类病灶的处方方案及正常组织剂量限制尚未形成共识。针对中央型病灶设计的临床试验RTOG 0813公布了毒性分析结果,发现10 Gy×5次的剂量分割方案较为安全,同时发现基于该方案,近端支气管树(PBT)D0.05 mL |
【本文地址】