| 肿瘤研究中统计学基本考量@MedSci | 您所在的位置:网站首页 › 医学sample评估法 › 肿瘤研究中统计学基本考量@MedSci |
肿瘤研究中统计学基本考量@MedSci
|
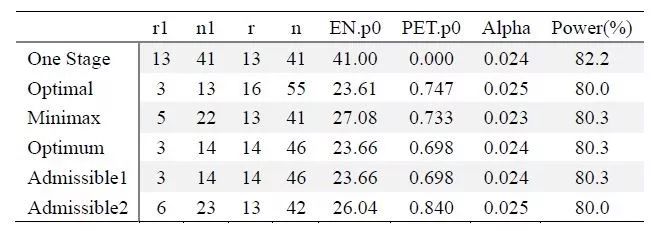
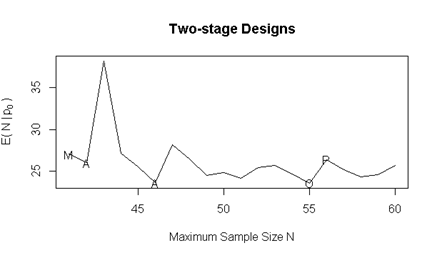
肿瘤研究的显著性水平和检验效能该如何设置? 除非在探索最大耐受剂量(MTD)的基础上扩大研究队列并进行假设检验,否则显著性水平一般不适用于I期研究。针对II期研究,如果考虑使用假设检验,可以对I类和II类错误设定更加宽松的显著性水平,例如α可以超过0.05(双侧),使用0.1(双侧),此外II期研究中也经常考虑使用贝叶斯相关的方法。对于平行对照的III期研究,总体I类错误一般控制在单侧0.025或双侧0.05以内,检验效能一般设为90%。需要注意的是:任何以注册申报为目的的试验,在设计阶段都应该考虑设置适当的I类和II类错误。如果进行多重比较,需要确保总体I类错误控制在单侧0.025或双侧0.05以内。 2肿瘤研究的分析集该如何定义? 全分析集(Full Analysis Set, FAS)通常定义为所有接受随机的受试者(随机试验),或所有入组/使用药物的受试者(非随机试验)。 符合方案集(Per Protocol Analysis Set, PPS)是全分析集的子集,会在FAS基础上剔除一些满足某些条件的受试者,这些条件往往与研究终点、试验设计或入排标准有关,并且需要在SAP中有所定义。安全集(Safety Analysis Set, SS)一般定义为所有至少使用过一次研究药物的受试者。注意,如果1例使用过药物的受试者,其某一安全性指标,如ECG没有基线后数据,或在做相对基线变化时缺少基线数据,那么该受试者会纳入安全集,但是其缺失数据的安全性指标ECG将不会进行统计分析。关于上述情况的处理方法,与现在很多国内申办方方案中的SS定义:所有至少使用过一次研究药物,且至少有一次用药后安全性评价的受试者,两者在数据集上的划分处理方法是不一样的,要注意加以区分,推荐使用本段标记为绿色的定义和做法。其他分析集,包括MTD分析集,PK浓度分析集,PK参数分析集,PD分析集,Biomarker分析集等等,统计师可以和医学讨论根据需要添加分析人群,比如肿瘤试验中对照组进展后会专组接受试验药物,所以可以定义一个交叉治疗分析集,诸如此类。某些疗效终点如PRO(Patient Reported Outcome)由于需要分析相对基线变化,所以可以不基于FAS,而单独定义一个PRO分析集,比如可以定义为:FAS的子集,所有有基线和至少一次随访PRO评估的受试者。 最后介绍一下划分数据集时经常提到的方案偏离。注意区分方案偏离和方案违背,方案违背是严重程度较高的方案偏离。对方案偏离的判断,主要基于入排标准以及其他一些方案中规定的流程标准。所有影响受试者安全性、研究执行或结果评价的方案偏离都需要报告,包括但不限于: 纳入不满足入排标准的受试者并给药 受试者接受错误的治疗或错误的剂量 受试者使用了方案禁止的合并用药 违反GCP 由于关于MTD集的相关介绍文章较少,这里举一个MTD集相关的方案偏离例子,通常MTD集需要剔除在DLT评估期发生重大治疗偏倚的受试者,包括但不限于: DLT评估期真实使用的用药总量比计划使用的总量少x%(假设不是由于出现DLT退出试验造成的) DLT评估期真实使用的用药总量比计划使用的总量多x% 联合治疗中,某种研究药物未使用(设不是由于出现DLT退出试验造成的) 某些方案中规定在给药前需要进行的预防措施未执行 如果受试者给错药,统计分析时该如何处理? 我们可以通过以下三种情况介绍一下通常的做法: 随机后未给药,根据SS的定义,出现该情况的受试者是不会被纳入SS分析的,亦不会被纳入PK分析集,但是根据FAS定义,该受试者会被纳入分析集并按照所随机分配的治疗组进行统计分析。在PPS中,该受试者一般会被剔除。 随机后给药,但是给错了研究药物,除了PPS,出现该情况的受试者一般会被纳入分析集,但是不同分析集统计分析的处理方法不同。对于SS和PK集,受试者一般会按照所随机分配的治疗组进行统计分析,除非是全部或超过xx%的给药给错,具体xx%需要根据不同试验而定。对于FAS,通常会归类到所随机分配的组下。 未随机,但是给予了研究药物,出现该情况的受试者由于未随机,一般不会被纳入到FAS和PPS,但是会按照实际治疗分组,进入SS和PK分析集。 期中分析主要分哪些情况? (1)以反应率为终点指标的II期单臂研究 这类II期研究设计的期中分析,往往用以判断试验药是否无效的,而不是用于判断药物有效而提前终止,但是从开展后续III期研究的角度考虑,也可能会进行事先商议有效性的标准 (这些内容可能不会包含在方案里)。根据不同试验情况,可以进行一次或多次期中分析。以一次期中分析为例,在第一阶段入组结束并达到分析要求(如最后一例受试者完成两次疗效评估)时,将会进行一次正式的期中分析,用以判断药物是否无效,以及试验是否该继续入组第二阶段受试者。如果在进行期中分析前,试验已经满足进入第二阶段的标准,则可以直接入组第二阶段受试者,否则入组进程会在第一阶段入组完成后暂停,等待期中分析结果而决定是否需要继续。如果分析结果不满足继续进行试验的标准,则试验终止。注意,单臂试验往往以反应率为主要终点,如ORR,而不推荐看OS和PFS这类指标。 此类单臂设计,根据研究不同目的,主要有如下几种选择: 目前较多采用的方法为Simon’s Two Stage设计[2],主要包括了Optimal和Minimax两种方法,Optimal平均期望样本量(EN)最小,而Minimax总样本量最小,即Optimal在期中分析时需要的样本量小于Minimax,但是需要的总样本量大于Minimax。从下表可以看到,Minimax第一阶段需要22例受试者,而Optimal只需要13例受试者。但是,Minimax的总样本量和只做一次分析的单阶段设计一致,而Optimal设计的总样本量要多14例,达到55例。所以在两者平均期望样本量相差不大(27.08 VS 23.51)的情况下,Minimax总样本量少很多,但是Optimal能在更少的样本量下给出一个Stage One结论,即如果药物无效,Optimal可以更早的停止试验,以免更多受试者暴露于无效治疗中。 表1. 不同方法二阶段设计样本量比较 (P0=0.2, p1=0.4, Alpha=0.025(单侧),Beta=0.200)
分层分析和亚组分析该怎么做? 在设置分层因素个数、分层因素水平数以及因素和水平的交互个数时,需要考虑样本量的大小。通常情况下,试验中接受随机的受试者例数应该是分层因素和分层水平乘积的50倍以上。依据ICH E9[1],随机分层因素的个数不应该超过4个。 主要统计分析方法应该体现试验设计,比如,试验使用了分层随机,对于时间-事件终点就应该使用分层Log-rank检验,对于二分类终点就应该使用Cochran-Mantel-Haenszel检验。只有在极少的情况下,分层分析可能只包含部分分层因素,或者即便进行了分层随机也不将分层因素纳入主要统计分析模型。 如果随机系统和EDC收集的分层结果不同,分析时该如何选择?分层分析时,应该使用随机系统里面记录的分层因素,而非EDC或CRF表采集的数据,但我们可以通过使用EDC或CRF表的数据进行敏感性分析。 在多中心试验中,如果中心数过多,我们在做主要分析时可以考虑把所有中心合并到一起分析,同时将几个入组较多的中心单独拿出来做亚组分析。或者事先可以提出一些归类标准,按照这些标准将不同地域或中心类型归类进行分层随机或分析,以避免统计分析时中心数过多的问题。 亚组分析的次数不宜过多,并且应针对重要的受试者或疾病特征进行。亚组分析需在SAP中提前定义。由于存在检验效能低和多重性检验等问题,亚组分析的结果往往只能用于探索和产生假设,而不能作为确证性结论,除非该试验是针对亚组分析而设计的。参考文献 [1] ICH E9 Harmonised Tripartite Guideline: Statistical Principles for Clinical Trials, February 1998.[2] Richard Simon, Optimal Two-Stage Designs for Phase II Clinical Trials, Clinical Trial. Control Clin Trials, 1989, 10:1-10.[3]Sin-Ho Jung, SL. George, et.al, Admissible two-stage designs for phase II cancer clinical trials, Statist. Med. 2004; 23:561–569[4] Jung SH, Carey M, Kim KM. Graphical search for two-stage designs for phase II clinical trials. Controlled Clinical Trials 2001; 22:367–372.[5] Ensign LG, Gehan EA, Kamen DS. An optimal three-stage design for phase II clinical trials. Stat Med, 1994, 13: 1727-1736.[6] Chen T.T, Optimal three-stage designs for phase II cancer clinical trials. Stat Med, 1997, 16: 2701-2711.[7] J Jack Lee, Diane D Liu, A predictive probability design for phase II cancer clinical trials, Clinical Trials 2008; 5: 93–106.[8] Y. Lin and W.J. Shih (2004), Adaptive Two-Stage Designs for Single-Arm Phase IIA Cancer Clinical Trials, Biometrics 2004, 60: 482-490.[9] Adrienne Groulx, Kyung-hee (Kelly) Moon, et.al. Using SAS® to Determine Sample Sizes for Traditional 2-Stage and Adaptive 2-Stage Phase II Cancer Clinical Trial Designs, SAS Global Forum 2007, Paper 188.[10] S.G. Thompson, A.P. Mander, Two-stage designs optimal under the alternative hypothesis for phase II cancer clinical trials, Clinical Trials 2010, 31: 572–578[11] Fleming TR. One-sample Multiple Testing Procedure for Phase II Clinical Trials. Biometrics, 1982, 38: 143-151[12] Gehan EA, The determination of the number of patients required in a follow-up trial of a new chemotherapeutic agent. J Chron Dis 1961, 13:346-353[13] Sin-Ho Jung, Minjung Kwak, Optimal two-stage log-rank test for randomized phase II clinical trials, Journal of Biopharmaceutical Statistics 2016: 1-20.[14] Cui L, Hung HMJ, Wang S, et al. Modification of sample size in group-sequential clinical trials. Biometrics. 55: 853-7, 1999.[15] Mehta C R , Pocock S J . Adaptive Increase in Sample Size When Interim Results are Promising: A Practical Guide With Examples[J]. Statistics in Medicine, 2011, 30(28):3267-3284.[16] Huang L , Bai J , Yu H , et al. Sample size re-estimation without un-blinding for time-to-event outcomes in oncology clinical trials[J]. The Journal of Biomedical Research, 2018(1):23-29.[17] Food and Drug Administration (FDA). Draft Guidance for Industry: Adaptive Design Clinical Trials for Drugs and Biologics, 2010.[18] Guidance for Clinical Trial Sponsors Establishment and Operation of Clinical Trial Data Monitoring Committees, 2006[19] Fleming T R , Ellenberg S S , Demets D L . Data Monitoring Committees: Current issues. Clinical Trials, 2018 Aug;15(4):321-328[20] D De Met, The independent statistician model: How well is it working? Clin Trials. 2018 Aug;15(4):329-334 来源:生统百宝箱 版权声明: 本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有,非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。本网所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。同时转载内容不代表本站立场。 在此留言 |
【本文地址】