| 丹参化学成分、药理作用及其质量标志物(Q | 您所在的位置:网站首页 › 丹参的主要功效是 › 丹参化学成分、药理作用及其质量标志物(Q |
丹参化学成分、药理作用及其质量标志物(Q
|
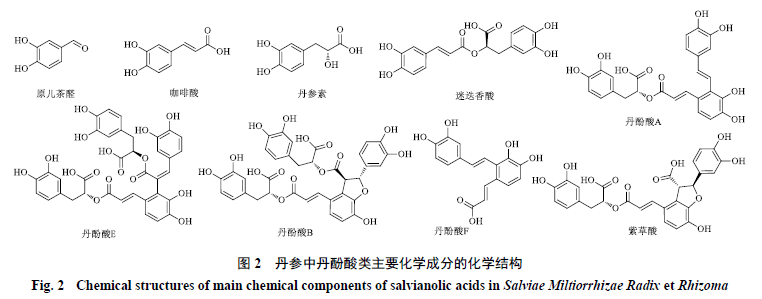
1.2 丹酚酸类 丹参中的丹酚酸类化合物具有水溶性,主要在其根的韧皮部和木质部中合成积累,目前已分离到30余种。主要活性成分为丹酚酸A、丹酚酸B、丹参素、咖啡酸、迷迭香酸、原儿茶醛、紫草酸等[12-13]。其中,大多数丹酚酸类化合物可视为咖啡酸的衍生物,如迷迭香酸为咖啡酸与丹参素的二聚物,丹酚酸B 为迷迭香酸二聚体,丹酚酸A 由1 分子丹参素与2 分子咖啡酸缩合而成[14]。丹酚酸类主要化学成分的化学结构见图2 。
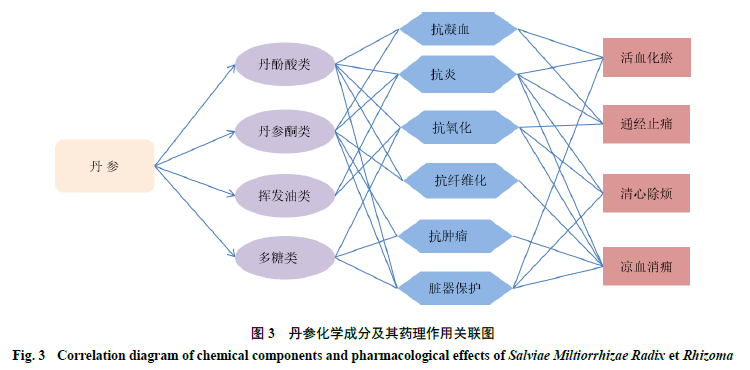
1.3 挥发油类 丹参中挥发油成分含量较低,目前已从丹参挥发油中分离鉴定得到30 余种化合物,主要包括桃 拓酚、铁锈醇、石竹烯、7-异丙基-1,1,4α-三甲基-1,2,3,4,4α,9,10,10α-八氢菲内酯、正十六酸、邻苯二甲酸二异丁酯、大根香叶烯D、油酸和正二十烷等[15-17]。 1.4 多糖类 丹参中的多糖因具有增强免疫、保护肝脏等作用而受到广泛关注[18]。Wang 等[19]从丹参中分离得到多糖SMPA ,其由半乳糖、葡萄糖、鼠李糖、甘露糖和葡萄糖醛酸组成。汪红等[20]通过高流速的离子型琼脂糖凝胶纯化丹参粗多糖后得到多糖SMP1 和SMP0.5 。汤伟[21]从丹参粗多糖中分离得到SMP1 、SMP2 和SMP3 3 个组分并进行相应的活性研究。 1.5 含氮化合物及其他成分 丹参中已分离得到的含氮化合物包括neosalvianen 、salvianen 、salvianan 、salviadione 、5-(methoxymethyl)-1 H -pyr-role-2-carbaldehyde 和环苯内酰胺等[22-23]。此外,丹参中还含有salviamone [24]和丹参螺旋缩酮内酯[25]等内酯类化合物。 2 药理作用 2.1 基于丹参传统功效的药理活性 2.1.1活血祛瘀研究表明,丹参酮IIA 通过扩张动脉,降低血液黏度,修复受损血管内皮细胞从而发挥活血化瘀功效[26]。丹参不同有效部位均能明显改善急性血瘀模型大鼠的血液流变学和凝血功能异常,且丹参总酚酸和丹参总酮配伍的活血化瘀效果 更优[27]。丹酚酸A、丹酚酸B、丹参酮IIA和丹参酮I可作用于凝血酶、纤溶酶原激活物抑制物-1 、过氧 化物酶体增殖物激活受体α、3-羟基3-甲基戊二酰辅酶A还原酶等血瘀关键靶标,发挥活血祛瘀功效[28]。 2.1.2 通经止痛徐勤芳[29]通过临床研究发现,在三阴交穴位注射丹参注射液,不仅能够疏经活血,还能增强药物作用,更好发挥止痛效果。丹参总酮的雌激素样生物活性能够抑制孕酮过多分泌,降低前列腺素F 2 水平,抑制子宫平滑肌强烈收缩,达到治疗原发性痛经的作用[30]。 2.1.3 清心除烦丹参性寒入心经,有清心凉血、除烦安神功效,《本草崇原》谓其“止烦满益气者,治心腹之邪气也。夫止烦而治心邪,止满而治腹邪,益正气所以治邪气也”。《中国药典》2015 年版中用于治疗心悸的中成药有79 个,包含176 味中药,其中丹参的频次最高,为31 次[31]。临床研究表明,安眠穴注射丹参注射液能够有效治疗顽固性失眠[32];丹参注射液直流电离子导入治疗颈性失眠的同时还能够减少安眠药的不良反应[33]。 2.1.4凉血消痈丹参性寒入血分,既能凉血活血,又能散瘀消痈,可用于热毒瘀阻所致的疮痈肿痛。《太平圣惠方》记载丹参以热酒送服主治寒疝,小腹及阴中相引痛,自汗出等;若阴器疼痛或肿胀者,则选丹参散[34]。 2.2 基于丹参拓展功效的药理活性 2.2.1 抗凝血丹参能够抑制血小板聚集、活化,阻止微血栓形成,促进一氧化氮生成,扩张血管,提高血流量,改善血液高凝状态,从而起到抗凝血作用[35]。丹参素通过抑制血小板蛋白质二硫键异构 酶内质网蛋白57和整合素αIIbβ3的相互作用,降低凝血因子活性,达到显著减少凝血酶诱导的血小板聚集[36]。丹酚酸A 在不影响凝血功能的前提下,能增加血小板中环磷酸腺苷的含量,抑制凝血酶、二磷酸腺苷(adenosine diphosphate ,ADP )和花生四烯酸诱导的血小板聚集,具有明显的抗血栓活性[37]。丹参酮IIA 能够诱导分化血管内膜平滑肌细胞凋亡,提高血管平滑肌细胞状态,抑制ADP 和胶原诱导的血小板聚集[38];丹参酮IIA 磺酸钠能够增加冠心病心衰患者的冠脉流量,提高心肌耐缺氧能力,改善心肌代谢紊乱,有效抑制血小板聚集和抗血栓形成[39-40]。隐丹参酮体外的抗血小 板聚集相对效价约为丹酚酸B的40倍,且研究证明了隐丹参酮为丹参中抗血小板聚集的药效物质[41]。 2.2.2 抗炎丹参中的丹酚酸类和丹参酮类成分对各种炎症模型均有一定的治疗作用。丹酚酸A 能够有效降低脂多糖(lipopolysaccharide ,LPS )所致脓毒症模型小鼠脾脏中 肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素-6(interleukin-6,IL-6)的含量,升高IL-10 的含量,有效抑制脾脏炎症[42]。丹参素与TNF-α 靶点具有较强的结合力,能够降低LPS 对小鼠腹腔巨噬细胞刺激,竞争性抑制TNF-α 所介导的炎性反应[43]。丹参酮IIA 通过减少LPS 刺激小鼠单核巨噬细胞产生的炎症细胞因子,并浓度依赖型抑制NIK-IKK 和丝裂原活化蛋白激酶(mitogen-activated protein kinase ,MAPK )等信号通路的激活,从而抑制LPS 诱导的核因子-κB 抑制蛋白-α (inhibitory protein-α of nuclear factor-κB ,IκB-α )降解及核因子-κB (nuclear factor-κB ,NF-κB )激活,以发挥抗炎活性[44]。李园园等[45]通过二甲苯所致的小鼠耳肿胀模型和LPS 刺激的小鼠腹腔巨噬细胞炎症模型研究发现,丹参水溶性成分能够显著抑制小鼠耳肿胀度和IL-6 水平,显著增强小鼠腹腔巨噬细胞吞噬中性红的能力。 2.2.3 抗氧化丹酚酸类成分结构中的酚羟基具有易氧化的特点。李惟滔等[46]研究表明,4 个丹酚酸类成分的抗氧化活性强弱为咖啡酸>丹酚酸B >丹酚酸A >丹参素。丹酚酸B 能够增强超氧化物歧化酶(superoxide dismutase ,SOD )及谷胱甘肽过氧化物酶活性,减少丙二醛(malondialdehyde ,MDA )含量,降低肌酸激酶和乳酸脱氢酶水平,清除体内多余的氧自由基,并抑制其过度生成和积累,其抗氧化作用可能与诱导骨髓间充质干细胞激活核因子E2 相关因子2- 抗氧化反应元件信号通路相关蛋白 的表达有关[47-48]。丹酚酸A能够降低总抗氧化能力,降低MDA、氧化型谷胱甘肽和TNF-α水平,抑制半胱氨酸天冬氨酸蛋白酶-3活性,升高SOD水平[49],上调抗氧化基因SOD、谷胱甘肽过氧化酶1的表达[50]。丹参素能降低H 2O 2诱导损伤的血管内皮细胞中MDA 含量,提高SOD 活性,增强细胞清除氧自由基能力,提高血管内皮细胞活力,对H 2O 2诱导的血管内皮细胞氧化损伤起到保护作用[51]。 2.2.4 抗纤维化丹参通过抑制肌成纤维细胞激活和细胞外基质沉积等,能够有效抵抗多种组织器官的纤维化,并在一定程度上恢复纤维化器官的病理生理状态[52]。丹参酮IIA 在肝纤维化阶段可抑制肝星状细胞活化、分解过量的细胞外基质,保证肝脏微循环畅通,最终逆转肝纤维化[53]。丹参酮VI可以通过减弱胰岛素样生长因子-1 (insulin-like growth factor 1 ,IGF-1 )诱导的磷酸化细胞外信号调节激酶和磷酸化蛋白激酶B ,从而减弱IGF-1 诱导的心肌纤维化[54] 。丹酚酸A 能够降低α 平滑肌肌动蛋白(α-smooth muscle actin ,α-SMA )、 转化生长因子-β1(transforming growth factor-β1 ,TGF-β1 )和Smad3 mRNA 水平,通过抑制TGF-β1/Smad 信号通路来延缓CCl 4 所致的大鼠肝纤维化进展[55] 。丹酚酸B 可以通过激活沉默信号调节因子1 (silent information regulator 1 ,Sirt1 )介导的自噬作用,减弱肾纤维化 过程中的上皮-间质转化(epithelial-mesenchymal transition,EMT)相关蛋白的表达,改善肾功能不全[56]。 2.2.5抗肿瘤丹参多成分通过调控细胞周期、抑制细胞增殖、诱导细胞凋亡等生物过程具有广泛的抗肿瘤作用。丹参酮IIA 能够诱导肺癌细胞发生自噬,使细胞阻滞于G 0/G 1期,导致细胞增殖受到抑制,进而实现治疗肺癌的目的[57]。隐丹参酮可通过诱导肿瘤细胞凋亡,抑制肿瘤细胞的增殖和转移侵袭,抗肿瘤细胞新生血管生成等,发挥抗肿瘤的作用[58]。丹参二萜醌能浓度相关地抑制人肺腺癌细胞PC9 增殖,通过触发细胞内质网应激,激活蛋白激酶R 样内质网激酶- 真核翻译起始因子eIF2 的α 亚基通路,促进细胞凋亡,发挥抗肺癌作用[59]。 2.2.6 脏器保护及其它作用高剂量丹参可以改善肝功能及肝组织病变、抑制IL-1β 表达和核苷酸寡聚化结构域样受体热蛋白结构域相关蛋白3 炎症小体的活化,有效减轻1,4- 二氢-2,4,6- 三甲基-3,5- 吡 啶二甲酸二乙酯诱导的小鼠胆汁瘀积性肝损伤[60]。丹参酮IIA通过抑制心肌细胞中胰岛素样生长因子II受体信号激活的细胞凋亡而具有保护心脏的作用[61]。丹酚酸B通过降低NF-κB p65、p53和B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)相关X蛋白(Bcl-2 associated X protein,Bax)表达,升高Sirt1和Bcl-2表达,对缺氧/富氧诱导的肝细胞损伤起到保护作用[62]。丹参多糖90 ~360 mg/kg 能有效预防小鼠免疫性肝损伤,其机制可能与丹参多糖减少小鼠肝脏中一氧化氮、TNF-α 和IL-1β 的产生有关[63]。丹参酮IIA 可稳定非体外循环冠状动脉旁路移植术患者的血流动力学,提高心脏功能[64]。总丹酚酸可改善缺血再灌注引起的学习记忆障碍,显著提高脑缺血再灌注小鼠的耐缺氧能力[65]。丹参多酚酸亦可维持心肌缺血时线粒体Na +, K +-ATP 酶和Ca 2+-ATP 酶的活性,有效降低缺血再灌注时心肌细胞线粒体的损伤,显著降低心肌梗死面积[66]。 3 Q-Marker的预测分析 丹参的产地、采收加工方法、贮存条件均会影响其化学成分的种类与含量[67-69]。《中国药典》2020 年版规定,丹参药材中丹酚酸B 的含量不得少于3.0% ,丹参酮IIA 、隐丹参酮和丹参酮I的总量不得少于0.25% 。为了更好的、更科学的对丹参质量进行控制,依据刘昌孝院士[70]提出的Q-Marker 概念,结合Q-Marker 科学内涵和研究思路,通过文献综述分析,对丹参的Q-Marker 进行整体分析预测,为丹参质量控制方法体系建立提供科学依据。 3.1 基于植物亲缘学及化学成分特有性的Q-Marker预测分析 唇形科植物在世界范围内共有220 余属,3500 余种,其中,中国有99 个属,约800 种[71]。鼠尾草属植物的化学成分类型主要为二萜类、三萜类、生物碱类和糖苷类等,具有抗炎、降血糖、抑菌、保肝、抗肿瘤、抗氧化等药理活性,其中荔枝草亚属 包含大叶鼠尾草组、丹参组、荔枝草组和多球苏组[72]。南欧丹参主要分布于中国北部,滇丹参主要分布于西南地区,丹参则分布较广;丹参和滇丹参均为根茎部入药,主要成分为丹酚酸类和丹参酮类,而南欧丹参入药部位主要为茎、叶及花序,其主要成分为挥发油类;丹参酮I、丹参酮IIA 、原儿茶醛和丹酚酸A 为丹参和滇丹参的共有成分,但其含量差异较大[73]。杨贵雅等[74]对不同产地的丹参皮部和木部中丹参酮类和丹酚酸类8 个主要活性成分进行含量测定发现,丹参酮类成分(二氢丹参酮I、隐丹参酮、丹参酮I和丹参酮IIA )在皮部的含量明显高于木部,而丹酚酸类成分(丹参素、迷迭香酸、紫草酸、丹酚酸B )在皮部和木部含量差异不大。丹参根、茎、叶、花的成分含量测定结果显示,丹参酮类和水苏糖为根中主要成分,黄酮类和三萜类为地上部分的主要成分,根部和地上部分均含有丹酚酸类成分[75]。张玲等[76]对白花丹参和紫花丹参中的微量元素进行测定发现,白花丹参根部铜、硼、钛和锶的含量及花中镍、硼和铜的含量均显著高于紫花丹参。 3.2基于成分有效性的Q-Marker预测分析 3.2.1 成分与传统功效相关性丹参酮类成分具有活血化瘀、通经止痛、抗凝血、抗纤维化、抗肿瘤等药理作用;丹酚酸类成分具有凉血消痈、清心除烦、抗炎、抗氧化等作用;挥发油及多糖类成分具有抗炎、抗氧化、脏器保护等作用。其主要成分的药理作用均与丹参活血祛瘀、通经止痛、清心除烦、凉血消痈的传统功效相一致,可以作为丹参Q-Marker 的选择参考。 3.2.2 成分与传统药性相关性丹参药材味苦,性微寒,归心、肝经。苦味药大多属寒凉,具有泻下、泻火、降气、坚阴、燥湿等功效,主要归肝、肺、胃经,其化学成分主要包括生物碱、挥发油、苷类、醌类、黄酮类及糖类等[77],其中清热药、抗疟药、祛风湿药、抗肿瘤药、泻下药、麻醉止痛药一般以苦味药为主[78]。在唇形科中药物质成分与药性相关性研究中,丹酚酸类成分丹酚酸A 、丹酚酸B 、紫草酸和丹参酮类成分丹参酮I、丹参酮IIA 等成分与寒性及苦味的关联性最为密切[79]。丹参化学成分及其药理作用关联图见图3 。结合上述丹酚酸类和丹参酮类发挥的相关药理作用,预测其可作为丹参Q-Marker 的选择参考。
3.3 基于化学成分可测性的Q-Marker预测分析 陈嘉慧等[80]采用超高效液相色谱串联四级杆飞行时间质谱(UPLC-Q-TOF-MS/MS)方法从丹参水提液中共检测到72个成分,包括丹参素、咖啡酸、原儿茶醛、丹酚酸A、丹酚酸B、紫草酸、丹参酮IIA、丹参酮IIB、新隐丹参酮、二氢丹参酮I、异隐丹参酮等。杨贵雅等[74]采用HPLC法检测出丹参素、迷迭香酸、紫草酸、丹酚酸B、二氢丹参酮I、隐丹参酮、丹参酮I和丹参酮IIA8种成分,并对丹参药材皮部和木部化学成分的指纹图谱进行分析。张亦琳等[81]利用高分辨质谱和灰色关联度分析法对5个产地丹参质量优劣进行研究,发现11个成分(丹参素、迷迭香酸、丹酚酸A、丹酚酸B、丹酚酸E、丹酚酸F和丹参酮IIA、丹参酮IA、隐丹参酮、二氢丹参酮、丹参酚酮)为不同产地丹参的共有成分。不同研究方法对丹参化学成分的含量测定见表1。
3.4基于可入血成分的Q-Marker预测分析 刘洋等[95]对大鼠ig 丹参水提物后体内原型成分及其代谢产物进行分析,明确了16 种入血成分中丹参素、原儿茶醛、咖啡酸、迷迭香酸以原型成分入血,其余12 种成分均是肠代谢转化后的新成分。冯颖等[96]通过LC-MS/MS 法在大鼠ig 给药丹参酮提取物后的血浆中检测到丹参酮I、丹参酮IIA 和隐丹参酮。Liu 等[97]对丹参素、迷迭香酸、隐丹参酮、二氢丹参酮、丹参酮I和丹参酮IIA 6 种成分进行了分析,研究发现,隐丹参酮在大鼠体内可进一步生物转化为丹参酮IIA ,并且在给药丹参提取物后的大鼠血浆中,丹参酮IIA 的浓度是丹参酮IIA 和隐丹参酮代谢物的累积。王小平等[98]通过HPLC-MS 法对大鼠注射丹红注射液后血浆中3 种丹酚酸类成分(迷迭香酸、紫草酸、丹酚酸B )的含量进行了检测,结果显示丹酚酸B 在大鼠血浆中的含量明显高于迷迭香酸和紫草酸。 3.5基于网络药理学预测的Q-Marker预测分析 目前,已有多位学者将网络药理学和分子对接等技术用于丹参的“成分-靶标-通路-疾病”网络机制研究。研究表明,丹参酮IIA与核心靶蛋白蛋白激酶B(proteinkinase B,Akt)1、IL-6、低聚果糖、血管内皮细胞生长因子A、MAPK1和表皮生长因子受体的结合活性较高,是丹参治疗缺血性脑卒中的主要成分[99];异隐丹参酮、四氢丹参酮I和丹参酮IIA等作用于β2肾上腺素能受体、人类α-阿片类受体基因、前列腺素内过氧化物合酶1、前列腺素内过氧化物合酶2等关键靶点,通过干预活性氧代谢、循环系统血管功能、氧化应激反应等生物过程,发挥治疗慢性肝炎的作用[100];丹参酮IIA和隐丹参酮通过Akt1、IL-6和肿瘤蛋白P53等信号通路的调节发挥治疗骨关节炎的作用[101];二氢丹参酮与降解肝脏内错误折叠蛋白功能的丝氨酸蛋白酶抑制剂A1靶点、与肝脏炎症反应密切相关的干扰素诱导蛋白10靶点、与合成肝纤维蛋白的纤维蛋白原α链靶点及参与抑制肝纤维化早期发作的血小板衍生生长因子靶点具有较强关联性,是防治肝硬化的主要活性成分[102]。 4结语 丹参药用历史悠久、自然资源丰富且分布较广,具有广阔的开发利用前景。在对丹参化学成分和药理作用概述的基础上,对丹参的Q-Marker 进行预测分析发现,丹参中多糖类和挥发油类成分虽有一定的生物活性,但因挥发油类物质易挥发、在丹参中含量少、含量测定的重复性和稳定性不好等因素不适合选作Q-Marker ;多糖类物质因其结构复杂,不易提取纯化等因素也不适合选作Q-Marker ;因此,建议将丹酚酸类和丹参酮类成分作为丹参Q-Marker 筛选的主要大类成分;单一成分建议将丹酚酸类成分丹参素、原儿茶醛、迷迭香酸、紫草酸、丹酚酸B 和丹酚酸A ,以及丹参酮类成分二氢丹参酮I 、隐丹参酮、丹参酮I和丹参酮IIA ,作为丹参Q-Marker 筛选的主要成分。为保证丹参及其相关制剂的临床疗效,建议对以上成分进行深入研究,以期建立科学的质量评价和控制方法。 利益冲突所有作者均声明不存在利益冲突 参考文献(略) 来 源:冯科冉,李伟霞,王晓艳,吴娅丽,张 辉,刘现磊,陈毓龙,李 琨,唐进法.丹参化学成分、药理作用及其质量标志物(Q-Marker)的预测分析 [J]. 中草药, 2022, 53(2): 609-618 .返回搜狐,查看更多 |
【本文地址】