| 【文献阅读】脑卒中康复研究的进展与挑战 | 您所在的位置:网站首页 › 中风患者的康复治疗 › 【文献阅读】脑卒中康复研究的进展与挑战 |
【文献阅读】脑卒中康复研究的进展与挑战
|
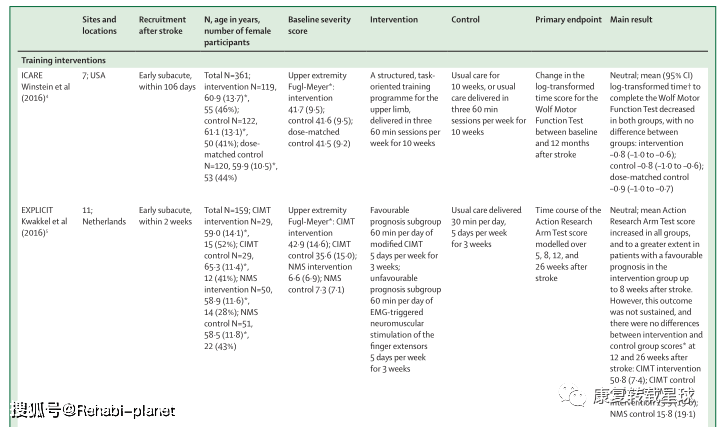
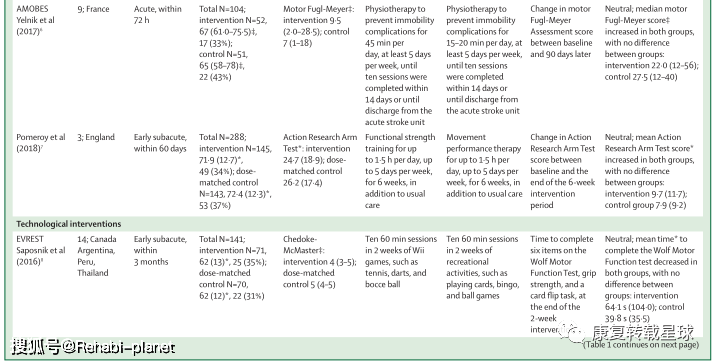
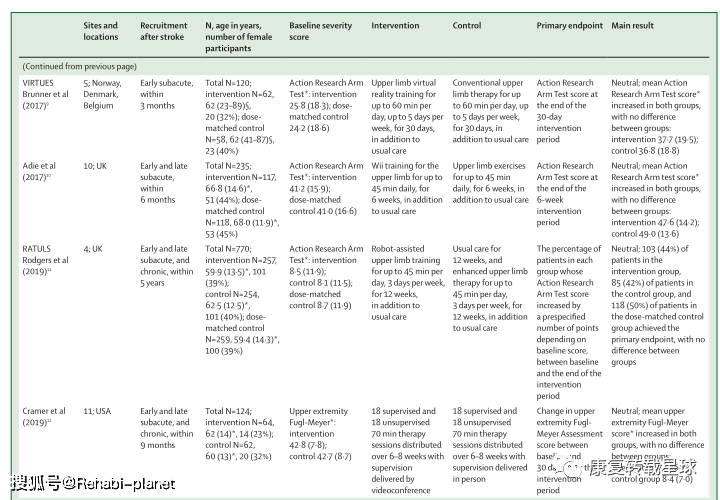
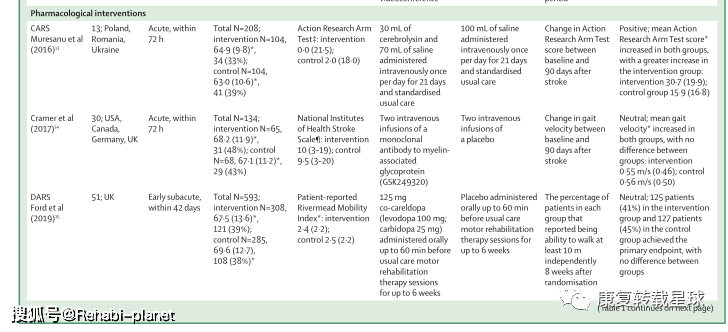
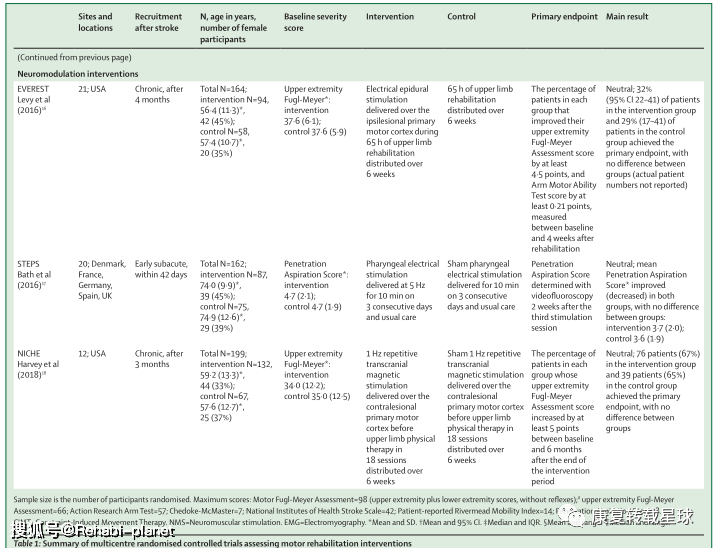
Substantial advances are yet to be made in stroke rehabilitation practice to meet this demand and improve patient outcomes relative to current care. Several large intervention trials targeting motor recovery report that participants’ motor performance improved, but to a similar extent for both the intervention and control groups in most trials. These neutral results might reflect an absence of additional benefit from the tested interventions or the many challenges of designing and doing large stroke rehabilitation trials. Strategies for improving trial quality include new approaches to the selection of patients, control interventions, and endpoint measures. Although stroke rehabilitation research strives for better trials, interventions, and outcomes, rehabilitation practices continue to help patients regain independence after stroke. 简介 中风是导致死亡和残疾的主要原因。1虽然中风死亡率正在下降,但由于人口增长和老龄化,中风患者的患病率有所增加。1中风幸存者人数的增加增加了对康复服务的需求。与康复相关的随机对照试验(RCT)对于改善临床实践至关重要,这样康复服务才能有效地满足这一需求。RCT在过去5年中所做的工作有很多值得我们学习的地方。本综述的目的是对卒中康复试验进行评价,并找出进一步提高卒中康复研究质量的方法。这篇综述集中在中风后的运动康复试验,因为运动障碍是常见的2,3,并且是大多数中风康复试验的目标。这篇综述中包含的试验测试了增强传统疗法的培训、技术、药理学和神经调节方法。 中风后运动康复 表1强调了本综述中讨论的15个试验的主要特征和发现,这些试验根据干预类型分组(第1组)。大多数试验在急性期和亚急性期招募参与者(小组1,表2),所有的干预组和对照组都报告有改善。然而,15项试验中有14项是中性的,因为两组之间在主要终点(第1组)上没有统计上的显著差异。唯一阳性试验,CARS,卒中后72小时内静脉注射脑活素。13脑活素是一种有益于上肢运动能力的猪神经肽制剂(第2组)。治疗组卒中后90天的平均行动研究手臂测试得分高于对照组。虽然随后的类似试验28无法复制这一发现,但荟萃分析报告了脑活素治疗对卒中90天后改良的Rankin评分的有益影响。29这一结果表明,脑活素可能具有改善缺血性卒中后预后的潜力。 四项随机对照试验评估了脑卒中急性和早期亚急性阶段训练干预的效果(表1)。AMOBES试验在急性期招募了参与者,发现旨在减少静止并发症的额外物理疗法对上肢和下肢损伤的益处与较低剂量的物理疗法相似。6其余3名RCT在亚急性早期恢复参与者,发现神经肌肉电刺激、5功能力量训练7和任务导向训练4对上肢能力的益处与常规护理相似。显性试验发现,改良的强制诱导运动疗法在中风后的前12周增加了上肢的能力,但这一益处在26周时并未持续。5由于没有定义主要终点,并且试验结束时治疗组和对照组的改善程度相同,因此保守的解释是,这项试验是中性的。 五项试验检验了技术干预在中风的亚急性和慢性阶段的效果。EVREST,8 Vires,9和Adie及其同事的一项试验10调查了虚拟现实和视频游戏对中风亚急性期上肢运动能力的影响,Cramer及同事12调查了远程康复与门诊治疗对中风亚急性和慢性期上肢损伤的影响。RATULS试验调查了机器人辅助治疗对上肢运动能力的影响,参与者主要处于慢性阶段。11所有这些试验都说明了大规模使用这些技术的可行性,并报告了与匹配剂量的娱乐活动8或传统治疗产生的益处相似的好处(表1)。9-12 三项试验调查了药物在急性和早期亚急性阶段的效果,包括前面提到的CARS试验(表1)。13使用单克隆抗体治疗90天后,步态速度没有进一步提高,超过了安慰剂组患者的改善。14类似地,DARS试验在运动治疗之前测试了卡比多巴-左旋多巴治疗,发现报告行走独立的参与者在治疗组和安慰剂组中的百分比相似。15 三个试验调查了以电咽部刺激(STEPS)形式的神经调节的效果,在中风的早期亚急性和慢性阶段,硬膜外电刺激16和重复经颅磁刺激(NICE)(表1)。18研究中将刺激疗法与物理治疗相结合。16、18虽然这些试验是中性的,但它们表明在多中心研究中使用神经调节干预措施的可行性。在慢性期提供了超过6周的干预,16,18和STEPS在亚急性早期提供了三次刺激。17在亚急性早期进行更长时间干预的可行性应该在未来的试验中探索。除一项试验外,所有试验的中性结果都可能表明,所测试的干预措施与常规护理(在培训或技术干预的情况下)具有类似的益处,或者在添加到常规护理(在神经调节或药物干预的情况下)时没有额外的益处。中性的结果可能也反映了设计和进行卒中康复随机对照试验的挑战。
改善中风康复试验 中风康复随机对照试验的设计、实施和报告面临着重大挑战,而Consensus正在围绕解决这些挑战的最佳方法进行开发。30让患者参与联合设计可能会增加试验及其结果的相关性。31、32关于改进中风康复随机对照试验的进一步建议将在稍后描述,并在小组3中总结。 保真性和隐蔽性 以标准化和盲目的方式提供康复干预是一个复杂和耗时的过程。33培训和技术干预通常需要治疗师个性化和改进干预。以一种标准化的、可重现的方式执行此操作是很困难的。一些试验通过报告治疗和控制干预措施的详细方案以及确保持续完成的治疗师培训方案解决了这一难题,4、5、7、11、12但其他培训和技术干预试验没有现成的方案。6、8-10相对于参与者将物理疗法作为其日常护理的一部分,医学干预面临着定时交付的挑战。虽然这一相对时间可能对某些药理药剂不重要,但对其他药剂可能很重要。例如,在DARS试验中,只有不到10%的参与者有资格进行符合方案的分析,因为治疗时机和治疗剂量的保真度较低,34这可能是导致这项试验的中性结果的原因之一。使用更整齐的检查表35或康复治疗规范系统36将改善实验和对照干预的报告以及试验的重复性。 隐藏组分配也可能很困难。安慰剂药理药物看起来与实验药物相同,假的神经调节干预可以被设计成保持对参与者、治疗师和研究人员的掩饰。但是,由于这些干预的物理性质,通过培训和技术干预几乎不可能隐藏。仅对药理制剂13-15和17,18个非侵入性神经调节能够对参与者隐藏分组。所有15个已回顾的试验都试图向负责收集结果数据的评价员隐瞒分组分配情况。7个报告隐瞒是否成功,4,5,7,8,10,11,18和4个报告,评价员在不同程度上被揭发。4,7,10,11提高和评估干预和分组分配的保真度可以提高试验质量,尽管这些行动可能需要额外的人力资源。4,7,10,11提高和评估干预和分组分配的保真度可以提高试验质量,尽管这些行动可能需要额外的人力资源 对照干预措施和剂量 实验干预措施经常对照所谓的常规、标准或常规护理进行评估。这些描述符代表了一组不同的治疗方法,在不同的国家有不同的定义和描述,37并且很难跨随机对照试验进行比较。由于缺乏对其有效成分的了解,适当的对照干预措施的选择受到阻碍。37-39剂量的实验和对照干预措施也可能受到可用时间和资源的限制。物理治疗的剂量和强度在治疗组和对照组之间可能不同,在试验期间可能会与所谓的常规康复治疗一起进行,从而使结果的解释进一步复杂化。 所有15个回顾试验都报告了实验和对照干预的计划剂量,除了AMOBES、6个EXPLICIT、5个和Pomeroy及同事7之外,所有试验都报告了提供的剂量。令人鼓舞的是,在7个8-12技术试验和4,7个干预训练中,试验组和控制组之间的计划强度是匹配的。三个训练干预试验为实验组计划的强度比为4-6在4-6个训练干预试验中,大多数实验和对照干预的强度低于临床指南推荐的强度(3∙75-10∙00h/周)。40,41个实验和对照干预产生了相似的益处,即使实验干预的强度更高。 大多数试验的参与者除了进行实验或对照干预外,还进行常规治疗,作为他们日常护理的一部分。参与者在试验期间完成的日常护理治疗没有通过三项培训干预试验,6,7,39项技术发明试验,10,11一项药理学试验,13项和两项神经调节试验进行测量或报告。17,18因此,在总体康复经验方面,组间可能存在重要的、未知的差异。其余7个试验报告,控制组有意完成的治疗量与实验组相当,8、9、12、16个有意完成的治疗比实验组少,4个或无意完成的治疗比实验组多15个或更少14个。未知和无意的差异可能会混淆对结果的解释,并限制试验之间的比较,最好避免。 报告参与者在随机对照试验期间完成的干预措施和常规护理疗法的剂量可以提高未来试验的透明度。考虑到剂量有几个变量(例如,重复次数、单位时间内重复的治疗强度、总有效治疗时间和治疗会话频率),决定如何最好地报告物理治疗的剂量是具有挑战性的。要控制和报告的剂量变量将根据干预的活动成分而有所不同(例如,特定任务训练的提供剂量与心肺运动需要不同的变量),必须事先确定。 恢复阶段 大多数运动恢复发生在中风后的前3个月。21、42、43因此,这段时间是实验干预塑造恢复和结果的关键机会之窗。44、45亚急性期恢复的神经生物学机制是复杂的,仍在阐明中。一般说来,缺血性卒中会对基因表达、细胞功能和存活组织的结构产生一连串的影响,其中大部分都能促进康复。这些内源性机制广泛存在,在中风后早期最活跃,43,46,47,并在很大程度上负责从运动损伤中恢复。20,21常规护理疗法和训练干预被认为主要通过补偿来促进运动能力的改善(小组1)。20-22未来的研究可能寻求通过在亚急性早期阶段加强内源性和治疗驱动的过程来改善康复。尽管在自发恢复不受损害的背景下测试干预措施会带来特别的挑战,但这些至少可以是通过选择患者和终点措施部分解决了这一问题。
慢性阶段的试验使干预效果的检测变得更容易,但这些试验还带来了其他挑战。例如,偏瘫上肢的长期不使用和一般身体状况的恶化会影响损伤和能力的基线测量。因此,慢性阶段干预的好处可能与帮助患者恢复到先前最佳状态的恢复有关,而不是特定的神经效应,帮助患者在先前最佳状态的基础上进一步恢复。这一挑战可以通过让所有参与者参与修复计划来解决,然后在基线措施稳定后运行控制。 过去几十年发表的大多数卒中康复随机对照试验都招募了慢性期患者。48在215项随机对照试验中,包括489组和12847名卒中集中开放获取康复数据库的参与者,平均登记时间为中风后509天(中位数141天)。48纳入脑卒中慢性阶段康复试验的患者存在问题,因为大部分恢复和康复服务提供发生在亚急性早期。令人鼓舞的是,15项回顾试验中只有3项是在慢性期进行的(表2)。这一发现表明,在卒中阶段进行多中心试验的能力越来越强,此时干预可能对运动恢复和结果有最大的好处。 病人选择 这15项回顾试验主要使用临床标准选择患者,包括年龄上限,和最小年龄,以及临床最高得分评价量表。两项药理药物试验也使用卒中病灶体积作为选择标准。未来试验可能会考虑明确说明选择标准的理由,以及标准与干预预期作用机制之间的联系。 急性期的试验在卒中后72小时内招募患者,而后期的试验有更宽的招募时间窗口(表1)。对于早期的亚急性试验,最窄的招募时间窗口在卒中后2周内,最宽的时间窗在卒中后106天,4因此包括了自发康复过程的开始、中期和结束的患者。因此,由于自发的生物恢复,患者在试验期间的改善程度可能会有重要的差异,这可能在组之间不匹配,也不能从干预的效果中解脱出来。这个问题不能通过报告各组之间在平均基线得分上没有统计上的显着差异来解决。取而代之的是,自发的生物恢复过程可能导致的改善程度需要在各组之间进行匹配,49,50,这可能至少部分通过在中风后的狭窄时间窗口(如2周)内招募所有参与者来解决。然后,可以根据其假设的或已知的行动机制,在适当的时间开始干预。 使用预后生物标志物(第1组)选择患者可能会改善干预组和对照组的匹配性,并丰富样本,如其他综述。49,51卒中后几天内所做的几项措施与随后的运动恢复和结果相关,包括通过脑电图、经颅磁刺激、结构和功能MRI技术以及基因分析获得的各种措施。49,51然而,这些措施往往与组内随后的运动恢复有关。预后生物标记物需要准确地预测单个患者的运动恢复或结果,以便在试验中用于患者选择或分层。经颅磁刺激评估的皮质脊髓束功能状态是上肢恢复的有力预测因子20、49、50,结果52对于个别患者来说,被认为可以用于临床试验。51该预后生物标志物对于招募中重度初始上肢损伤患者的试验尤其重要,对这些患者来说,基线临床评分不能很好地预测运动恢复。 未来的试验还可以包括预测性生物标志物(第1组),以选择最有可能对干预的作用机制有反应的患者。例如,试验在慢性期患者的患侧运动皮质上进行硬膜外刺激,并报告了一个中性的结果(表1)。16专案后分析发现,与没有功能性皮质脊髓束且该束结构受损较多的患者相比,功能完整、该束结构受损较少的患者更有可能改善上肢功能。53这一发现说明了选择具有从干预中受益所需生物底物的患者的重要性。到目前为止,还没有使用非侵入性刺激来改善运动能力的多中心RCT根据皮质脊髓束存活情况专门选择患者。虽然单一方案不太可能在亚急性或慢性阶段惠及所有患者,但基于皮质脊髓束功能的关键预测生物标志物,可以开发出54,55刺激方案。 基于皮质脊髓束功能状态的患者分层可以更有把握地解释报告上肢运动阳性结果的随机对照试验(RCT)。恢复。例如,CARS试验招募了中风后72小时内有严重上肢损伤的患者(表1)。13名患者的特征和基线临床评分在治疗组和对照组之间保持平衡。然而,尽管基线临床评分相似,但有功能性皮质脊髓束的患者上肢运动恢复明显好于无功能性皮质脊髓束的患者。49与对照组相比,治疗组中可能有更多的有功能性皮质脊髓束的患者,无论治疗如何,他们的恢复都更好,这种差异可能是导致试验阳性结果的原因之一。 未来旨在改善上肢运动恢复的试验可以消除现有证据的歧义,方法是在卒中后的一个狭窄的时间窗口内记录患者,并在选择和分层最初严重上肢瘫痪的患者时使用皮质脊髓束功能完整性的分析。需要为旨在改善下肢运动恢复、语言和吞咽的试验开发生物标记物。 选择最佳主终点和次终点结局指标 卒中康复RCT的另一个挑战是初级和次级终点的选择,无论是在措施上还是在进行这些终点的时间上都是如此。针对运动域的干预试验应该选择特定于运动损伤、能力和性能的终点测量(第2组)。探索性的早期试验可以在所有三个水平上有效地部署措施,而后期试验可以优先考虑容量和性能的测量,以捕捉发明对患者日常活动和行为的影响。在这三个水平上,早期试验可以有效地部署措施,而后期试验可以优先考虑容量和性能的测量,以捕捉发明对患者日常活动和行为的影响。独立或残疾的全球测量,如修正的Rankin量表,不够灵敏,不足以作为针对运动域的干预试验的主要终点测量‘ 主要终点措施的选择应考虑到干预措施的已知或假想的机制和行动的时间进程。例如,神经肌肉电刺激瘫痪腿部肌肉通过增加力量来减少损伤,但对步行能力没有影响,56这需要在初级终点测量的选择中反映出来。患者还可以学习使用代偿性运动策略来克服损伤,如躯干移动来补偿与瘫痪手臂接触时肩和肘部的协同耦合。57,58采用这种策略可能有助于活动改善,但在基于损伤的终点可能无法检测到。早期RCT可能在干预后立即进行主要终点测量以检测受益信号,而后期RCT可能稍后进行主要终点测量以检测持续的有益效果。’ 主要终点可以是结果的绝对度量,例如Action Research ARM测试分数在干预后,或随着时间的推移恢复的度量,例如,在基线和干预后之间的行动研究ARM测试分数的变化。对于在亚急性阶段进行的试验来说,使用评分变化作为主要终点测量可能是有挑战性的,因为在这段时间内,由于自发的生物恢复和日常护理,评分预计会有所改善,而不考虑可能的干预效果。这个问题至少可以通过在早期和狭窄的时间框架内招募所有参与者,并使用预测生物标记物来匹配群体来部分解决。 患者在卒中后的宽时间窗内招募(表2),干预持续时间从3天到3个月不等,主要终点测量在干预结束、干预后或试验结束时进行。这种差异阻碍了试验之间的直接比较。在12个急性和亚急性阶段的回顾试验中,有8个在参与者达到慢性恢复阶段(中风后6个月;表2)之前评估了主要终点措施。在这种情况下,参与者在主要终点测量后可能会继续改善。例如,干预可能会加速亚急性期的恢复,但对照组可能会迎头赶上,在中风后6个月有类似的结果。一旦亚急性阶段完成,可以有效地获得主要终点或后续措施,以检测干预是否产生更长期的好处。纳入患者报告的次要终点措施,最好是与患者协商选择,也将增加试验结果的相关性。 现实挑战 就招募和留住试验参与者的结构性障碍而言,与中风康复随机对照试验相关的实际挑战因国家和卫生保健系统的不同而不同。虽然学术医疗中心是急性中风治疗试验的关键临床基础设施,但康复通常是由分散和独立的组织和系统提供的。参与者通常必须亲自出现在研究现场才能接受干预,干预通常每周提供1-5天,持续2-8周。随着患者从急性护理中心转移到住院、门诊和社区康复环境,试验组织和干预保真度的挑战增加。最初和继续参与康复试验受地理位置、患者中风严重程度、合并症、社会环境、家庭喜好以及交通和照顾者可用性等因素的影响。提供交通工具是一种可以促进参与的实际措施。参与者招募进入回顾试验的速度通常很慢,无论中风后的哪个阶段。在15个试验中,有8个每月每个站点招募的∙5参与者少于0.5。个试验的参与者人数最多7评估计划随机对照试验的可行性和干预措施的可接受性的初步工作有助于确定和解决可能限制招聘的因素。研究人员在急性期和早期亚急性阶段接触患者的机会可能会受到照顾这些患者的卫生保健组织的地点和政策的限制。实验和对照干预可能会与常规护理争夺参与者的时间和精力,而患者或临床团队并不优先考虑研究参与。广泛的纳入和排除标准也可能限制符合参与条件的患者的比例。由于失语症或语言障碍等沟通困难而被排除在外的患者是中风人群中研究不足的一部分。59提供失语症友好的试验信息和必要的口译服务将有助于招募。在临床环境中嵌入投资人,以便能够每天接触患者60,并设计可在常规临床护理的时间限制内获得的干预措施,也将促进在临床实践中招募和吸收有益的干预措施。 在未来的康复试验中,可以考虑纳入缺血性和出血性中风患者。与急性中风治疗或二级预防试验不同,中风类型似乎对运动康复51或结果影响甚微。53如果康复干预的生物目标与中风类型无关,在安全的情况下,包括两种类型的中风都可以增加招募率。在这里回顾的15项试验中,有10项同时包括缺血性和出血性中风患者。剩下的五个试验排除了出血性中风患者,其中三个是唯一不能招募到所需样本量的试验。如果没有残留的运动障碍,纳入有中风病史的7,15,18名患者也可以增加招募 对临床实践的影响 没有明确的证据表明,在大型多中心中风康复试验中测试的干预措施优于目前的治疗。此外,患者在亚急性期和慢性期都从实验和对照干预中受益。这一发现表明,对于大多数患者来说,有意义的运动损伤和能力的改善是可能的(表1)。 中风康复指南在过去5年中增加了推荐的治疗量,40,41,61,但目前最佳治疗量是一个悬而未决的问题。动物实验表明,更多的运动训练与更好的运动恢复有关。62-64此外,基于临床试验数据的荟萃分析的证据表明,在人类中,更高的运动疗法与更好的结果相关。65,66然而,在亚急性67和慢性68测试相同训练干预的不同剂量的随机对照试验(RCT)分期没有显示出常规临床护理中通常剂量的2-3倍的额外益处。69在亚急性早期进行非常大量的运动训练是否能显著改善康复和预后仍然是一个悬而未决的重要问题。 一项对中风慢性期患者进行的前瞻性观察研究发现,每周5天、持续3周的90小时物理治疗可以减少上肢运动损伤。72然而,这项研究受到非盲目评估和缺乏对照组的限制。另一项研究随机将慢性期的患者分为三组进行物理治疗干预,发现每周5天300小时的治疗持续12周,也可以减少上肢运动损伤,没有组别效应。73因此,慢性期的进一步治疗可能是有益的,尽管尚不清楚扭转偏瘫上肢的不使用和全身身体恶化的可能贡献。剂量效应似乎不存在,因为两项研究都报告了上肢Fugl-Meyer评估评分平均改善了约9-10分,尽管治疗剂量存在3倍的差异。74,75总体而言,在RCT s56的背景下以及在临床实践中,一些康复服务似乎比没有康复服务要好 。 一些研究已经测试了新的方法,以增加提供的康复数量,同时将对额外资源的需求降至最低。除了远程康复,12一种方法是培训家庭成员和照顾者提供治疗。75从那时起,在中风后1个月内随机分配1250名参与者的参加试验中,家庭主导的康复治疗能够使住院康复量增加一倍以上(5小时对2小时),并在出院后1个月内每天增加30分钟,持续1个月。76家庭成员提供的额外康复治疗没有产生更好的结果,以改良的Rankin评分衡量。将康复转移到家庭或照顾者可以有效和安全地增加完成的治疗量;然而,在试验中获得的更大的治疗量并没有提供额外的好处。 综上所述,目前可用的传统疗法可以改善卒中后的结果,正如对照组参与者所获得的益处所表明的那样。这些益处主要包括活动能力的改善,这反过来可以减少残疾、照顾者负担和激励并提高参与和生活质量。61需要与自发生物恢复机制相互作用的新干预措施,以减少中风后的运动损伤,并使更多的独立活动和参与成为可能。同时,确保中风患者能够获得康复服务是提高他们日常生活中运动能力和表现的最佳选择。 通过PubMed对2014年1月1日至2019年7月5日发表的文章的搜索,确定了本综述的搜索策略和选择标准参考。 我们使用了术语“中风”、“康复”和“试验”的组合,并且没有语言限制。我们还通过搜索我们自己的文件来识别文章。多中心随机评估RCT,随机分配至少100名参与者,如果他们测试的干预涉及运动康复治疗或主要终点评估自愿运动功能,或两者兼而有之。主要终点测量为一般残疾或独立性的试验,如AVERT试验协作小组的AVERT试验,不在本综述的范围内,因为干预和主要终点测量都不是自愿运动康复所特有的。最终的参考文献列表是根据原创性、影响力和主题相关性由作者一致选出的。 结论与未来方向 亚急性期早期大型多中心随机对照试验的增多是卒中康复研究领域的一个积极进展。到目前为止,大多数试验都是中性的,因为实验干预和对照干预对运动恢复和结果产生了类似的好处。这篇综述建议如何改进未来中风康复试验的设计和实施(小组3)。这些建议包括扩大纳入标准,在必要时包括缺血性和出血性中风类型,有中风病史的患者,以及有沟通困难的患者,以提高招募比率和结果的普适性。这篇综述还包括缩小纳入标准的建议,在卒中后早期在短时间窗口内招募患者,并使用生物标记物选择患者,以减少研究对象间的变异性,丰富样本。未来的试验还将受益于提高治疗的保真度和隐蔽性,使用与干预的作用机制仔细一致的特定领域的主要终点措施,以及减少参与研究的障碍。临床实践可以继续识别和消除限制患者获得适当康复服务的障碍,以便随着更好的治疗的出现,提供这些服务的能力将会提高。 康复转载星球 提了一个问题 留言板: 参与讨论返回搜狐,查看更多 |
【本文地址】