| 2023 ESMO | 您所在的位置:网站首页 › “卡瑞利珠单抗” › 2023 ESMO |
2023 ESMO
|
图2.Ahead-G208研究主要终点 免疫药物用于胃癌围术期治疗的研究近年来正在如火如荼地开展,但并不一帆风顺。ATTRACTION-5研究[7]中探索了免疫联合化疗在中晚期G/GEJ患者术后辅助治疗中的应用,但未达到主要终点-无复发生存时间。KEYNOTE-585研究[8]应用免疫联合化疗达到了主要终点pCR,但在无事件生存上未取得统计学显著差异,总生存期未正式检验。为进一步优化治疗方案,研究者们继续砥砺前行,将目光转向于靶免化方案在胃癌围术期的探索,Ahead-G208研究应运而生。Ahead-G208研究是截至目前为止首个成功的胃癌围术期靶免化方案研究,本次ESMO大会上研究数据的正式发布将有望改变胃癌围术期治疗格局,改写指南,为卡瑞利珠单抗再添新的III期研究证据(图3)。
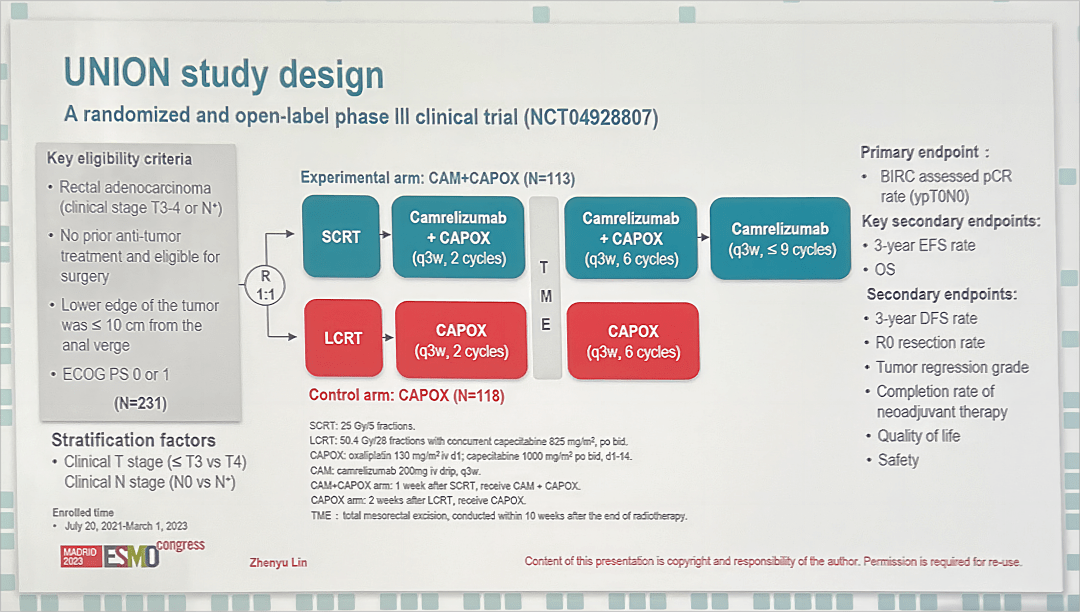
图3.研究者汇报Ahead-G208结果 Ahead-G208研究中卡瑞利珠单抗为胃癌围术期患者提供了新的治疗策略。本届ESMO大会上,卡瑞利珠单抗令人惊喜的亮相远不止于此。在直肠癌领域,卡瑞利珠单抗围术期治疗的UNION研究梅开二度,作为首个直肠癌免疫联合的新辅助III期研究,为肿瘤领域界带来了又一惊喜。 改善LARC远期生存预后任重道远,围术期免疫联合带来全新契机 我国所有恶性肿瘤中,直肠癌位列第七,近年来新发病例数量仍然居高不下,其中LARC(T3~4或N+)患者占比较高[10]。LARC患者直接手术治疗术后复发风险及远处转移风险较高。SCRT或长程放化疗(LCRT)联合化疗已被推荐为LARC的标准新辅助治疗方法之一[11,12]。然而,LARC远处转移风险及长期生存仍待进一步改善。 免疫药物的问世为改善LARC患者远期预后提供了强有力的支持和保障。KEYNOTE-177等多项[13]研究均证实了免疫治疗在LARC中的疗效和价值,但研究对象多为微卫星不稳定(MSI-H/dMMR)患者。MSI-H/dMMR在结直肠癌患者中的占比较低,在直肠癌患者中占比不足5%。一些前瞻性II期研究结果显示了免疫联合放疗在微卫星稳定(MSS/pMMR)型LARC患者中较高的pCR率[12]。但仍待更高级别循证依据、更大样本量的III期研究进一步验证。 更高循证直击全人群,卡瑞利珠单抗+SCRT提供肠癌围术治疗新思路 UNION研究是SCRT序贯卡瑞利珠单抗联合化疗对比LCRT序贯化疗治疗LARC的随机对照、III期临床试验[14](图4)。
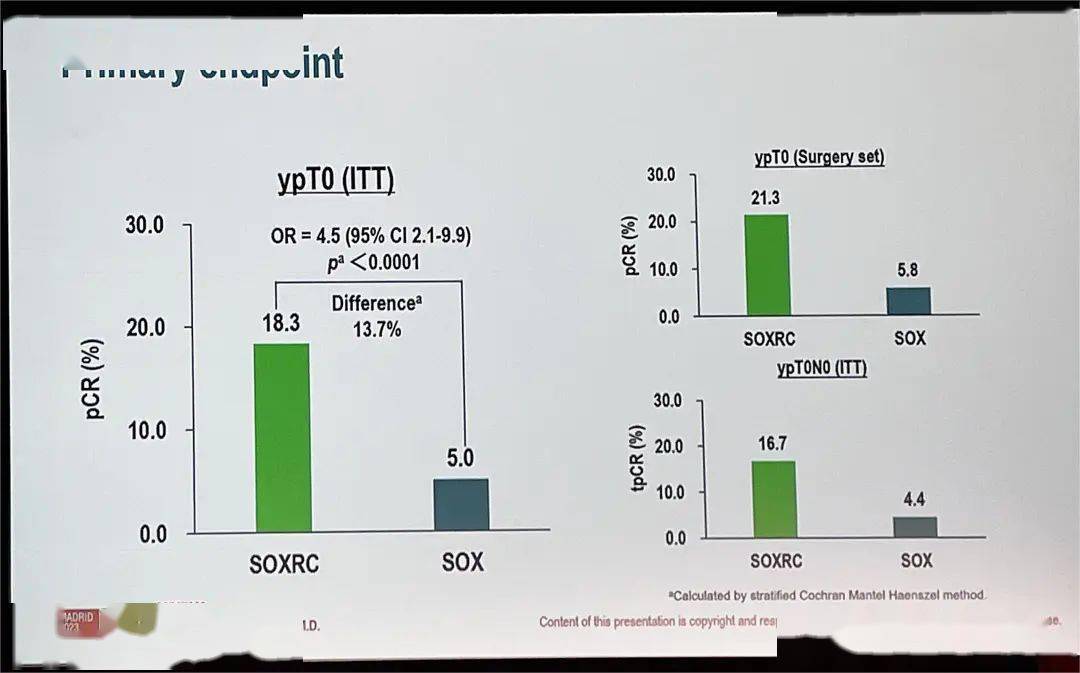
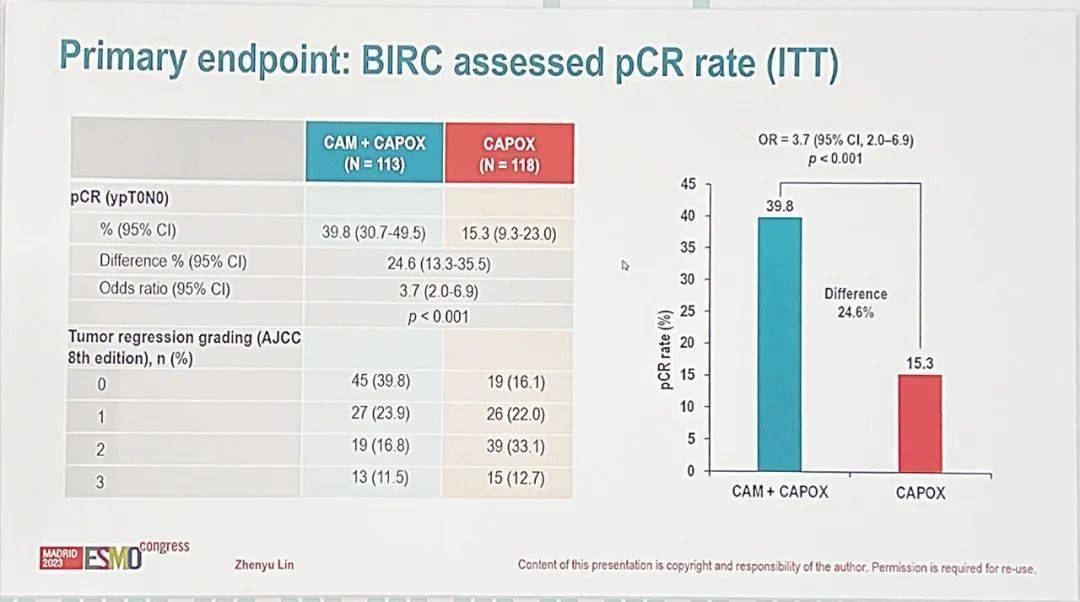
图4.UNION研究设计 研究结果达到主要终点,IRC评估的ITT人群的pCR率在试验组为39.8%,显著高于对照组的15.3%(图5)。亚组分析显示,所有亚组均有一致的阳性结果。两组患者在术后并发症、安全性方面无显著差异。目前正在监测长期生存结果。
图5.UNION研究主要终点 SCRT和LCRT是LARC可选的两种新辅助治疗模式。LCRT因具有更高的降期率和pCR率,是目前指南推荐用于LARC患者围术期的主流治疗方式。但LCRT治疗周期长且获益有限,与SCRT相比复发率、生存率及并发症方面的疗效相当。免疫药物的应用为优化直肠癌新辅助治疗提供了新的思路,但截至目前,免疫药物的应用仍非常局限,仅有dMMR/MSI-H患者获益明确。既往研究均为小样本的II期研究,证据力度有限。 作为首个用于直肠癌新辅助治疗的免疫联合方案,UNION方案疗效突出、安全性良好,即使是高危患者也能取得巨大获益。不仅如此,UNION研究为III期临床试验、证据级别更高,保证疗效同时大大缩短了新辅助治疗时间、提高患者围术期治疗的耐受性及依从性。患者长期获益在基于卡瑞利珠单抗的免疫联合方案下得到保障。UNION方案有望改写诊疗指南、打破现有治疗格局,为治愈直肠癌患者倍增信心(图6)!
图6.研究者汇报UNION结果 精准医疗背景下,胃肠道肿瘤“量体裁衣”式治疗渐入佳境,但局部晚期患者术后风险及生存预后等瓶颈仍然未能显著突破。2023年ESMO大会捷报频传,卡瑞利珠单抗在Ahead-G208及UNION两大III期研究中的表现为胃肠肿瘤的围术期治疗提供了突破性进展,更高的pCR为更多胃肠肿瘤患者带来了治愈希望。免疫治疗不断地深耕前行,相信这一里程碑式的跨越将为胃肠肿瘤患者谱写更加绚烂的生命之歌。 参考文献: 1. Cao W, et al. Changing profiles of cancer burden worldwide and in China: a secondary analysis of the global cancer statistics 2020. Chin Med J (Engl), 2021,134(7):783-791. 2. 中国胃肠肿瘤外科联盟.中国胃肠肿瘤外科联盟数据报告(2014−2016). 中国实用外科杂志,2018,38(1):90-93. 3. Wang FH, et al. The Chinese Society of Clinical Oncology (CSCO): clinical guidelines for the diagnosis and treatment of gastric cancer, 2021. Cancer Commun (Lond),2021,41(8):747-795. 4. Japanese gastric cancer treatment guidelines 2018 (5thedition). Gastric Cancer,2021,24(1):1-21. 5. 朱正纲. 局部进展期胃癌围手术期治疗的现状与展望. 中华胃肠外科杂志, 2021, 24(2): 101-106. 6. Chen Li, et al. Camrelizumab combined with rivoceranib and chemotherapy versus chemotherapy as perioperative treatment for locally advanced resectable gastric or gastroesophageal junction adenocarcinoma: the first interim analysis of a randomized, phase III trial (DRAGON IV/CAP 05), 2023ESMO. 7. Masanori Terashima, et al. ATTRACTION-5: A phase 3 study of nivolumab plus chemotherapy as postoperative adjuvant treatment for pathological stage III gastric or gastroesophageal junction (G/GEJ) cancer. 2023ASCO,Oral Abstract #4000. 8. K. Shitara, et al. Pembrolizumab plus chemotherapy vs chemotherapy as neoadjuvant and adjuvant therapy in locally-advanced gastric and gastroesophageal junction cancer: The Phase 3 KEYNOTE-585 study. 2023ESMO, LBA74. 9. Y. Janjigian, et al. Pathological complete response (pCR) to durvalumab plus 5- fluorouracil, leucovorin, oxaliplatin and docetaxel (FLOT) in resectable gastric and gastroesophageal junction cancer (GC/GEJC): interim results of the global, Phase 3 MATTERHORN study.2023ESMO, LBA73. 10. Siegel RL, et al. Cancer statistics,2016. CA. Cancer J Clin, 2016,66(1):7-30. 11. Bahadoer RR, et al. Short-course radiotherapy followed by chemotherapy before total mesorectal excision (TME) versus preoperative chemoradiotherapy, TME, and optional adjuvant chemotherapy in locally advanced rectal cancer (RAPIDO): a randomised, open-label, phase 3 tria. Lancet Oncol, 2021, 22(1): 29-42. 12. Garcia-Aguilar J, et al. Effect of adding mFOLFOX6 after neoadjuvant chemoradiation in locally advanced rectal cancer: a multicentre, phase 2 trial. Lancet Oncol. 2015;16(8):957-966. 13. Diaz Jr L A, et al. Pembrolizumab versus chemotherapy for microsatellite instability-high or mismatch repair-deficient metastatic colorectal cancer (KEYNOTE-177): Final analysis of a randomised, open-label, phase 3 study. The Lancet Oncology, 2022, 23(5): 659-670. 14. Lin Z , et al.Phase II, single-arm trial of preoperative short-course radiotherapy followed by chemotherapy and camrelizumab in locally advanced rectal cancer.Journal for ImmunoTherapy of Cancer, 2021(11). END返回搜狐,查看更多 |
【本文地址】
| 今日新闻 |
| 推荐新闻 |
| 专题文章 |