| HER2 | 您所在的位置:网站首页 › rc48-adc乳腺癌 › HER2 |
HER2
|
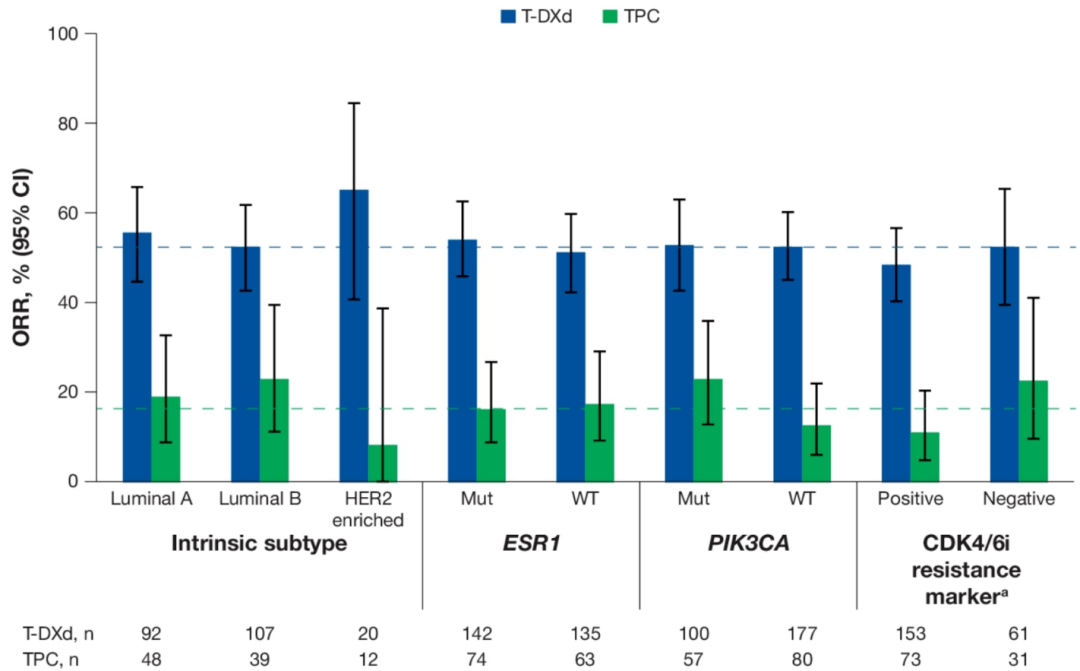
然而,新一代HER2 ADC的药物抗体比(DAR)大大提升,且具有旁观者效应,使其疗效并不完全依赖于HER2抗原性;而ER信号通路以及HER2下游信号通是理论上可以影响新型HER2 ADC的潜在标志物,但需要进一步研究确认。因此,对抗HER2治疗的相关生物标志物探索,包括筛选优势或劣势治疗人群,有助于指导临床实行更加精准的治疗分层。 02 DB-04研究:T-DXd疗效“一视同仁” 上述问题在本次ASCO大会报道的DB-04研究探索性分析 [2] 中可以找到一些答案。 DB-04研究中有高达65%的患者经过CDK4/6抑制剂(CDK4/6i)治疗失败,而且ESR1突变、PIK3CA与患者预后不良相关,对HR+乳腺癌的治疗反应有重要影响;此外,PAM50在CDK4/6i或内分泌治疗中具有预后和预测价值。这项探索性研究,将基线肿瘤组织或血液样本进行RNA-seq或ctDNA检测,以分析PAM50内在亚型、CDK4/6i耐药标志物(CCND1、CCNE1、 CDK6、RB1、PTEN、RAS、AKT1、ERBB2、FAT1突变或FGFR1/2扩增)、ESR1突变、PIK3CA突变对T-DXd疗效的影响。 研究结果显示,在疗效方面,不同PAM50内在亚型(Luminal A、B和HER2富集)、ESR1突变或野生型、PIK3CA突变或野生型、CDK4/6i耐药或非耐药患者的ORR保持一致(见下图)。
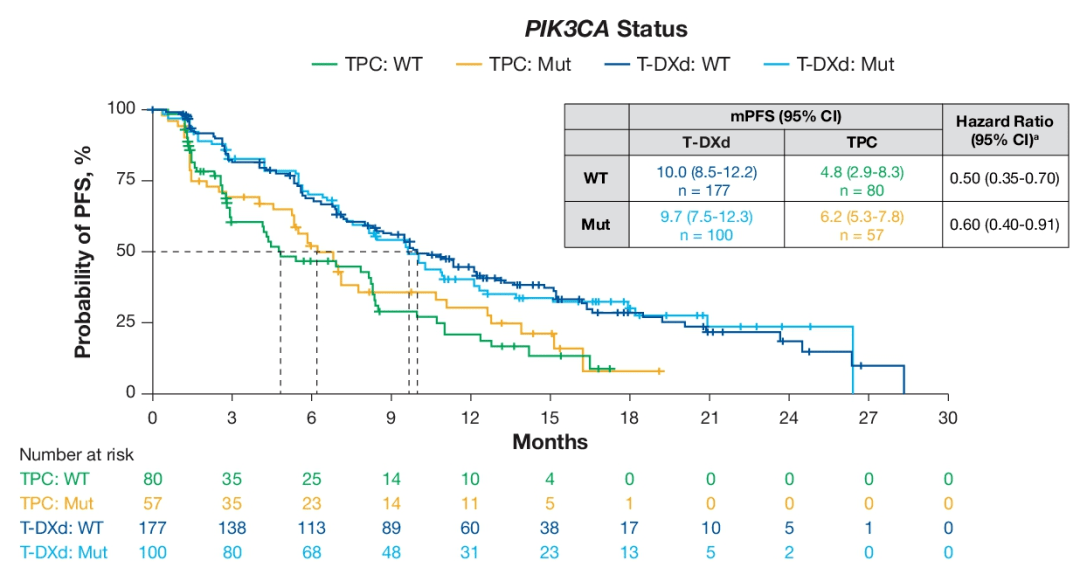
△DB-04研究中:不同内在亚型、ESR1、PIK3CA和CDK4/6i耐药标志物状态患者的ORR PIK3CA突变型(HR 0.50)、野生型(HR 0.60)患者均可从T-DXd治疗中相比TPC(研究者选择的治疗)增加获益;而且T-DXd治疗这两种PIK3CA状态患者的无进展生存期(PFS)相似(10.0 vs 9.7个月)。
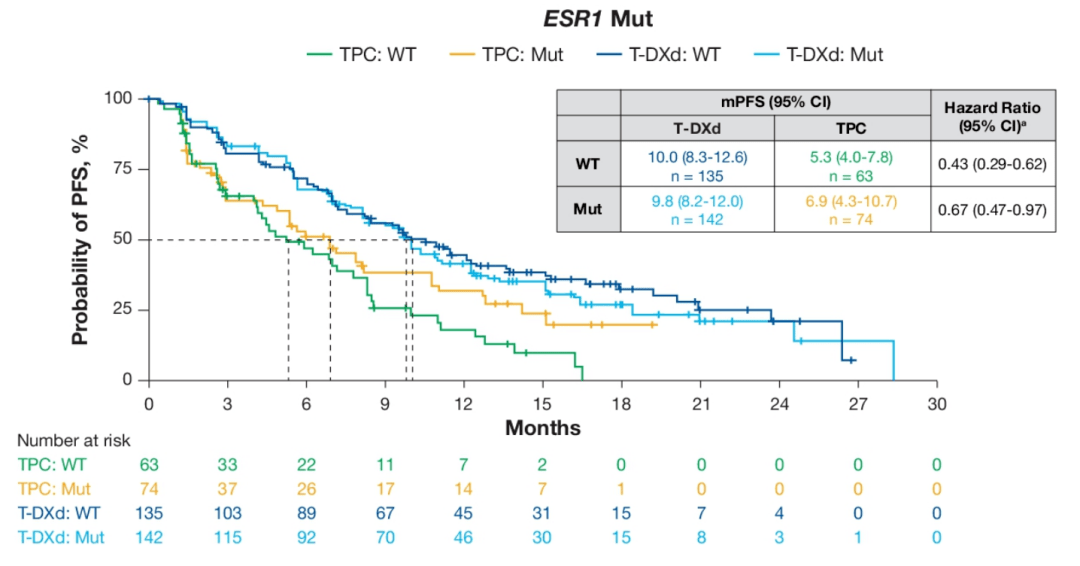
△DB-04研究中:不同PIK3CA状态患者的PFS ESR1野生型(10.0 vs 5.3个月,HR 0.43)、突变型(9.8 vs 6.9个月,HR 0.67)的T-DXd治疗获益也保持一致;T-DXd治疗这两种ESR1状态患者的PFS相似(10.0 vs 9.8个月)。
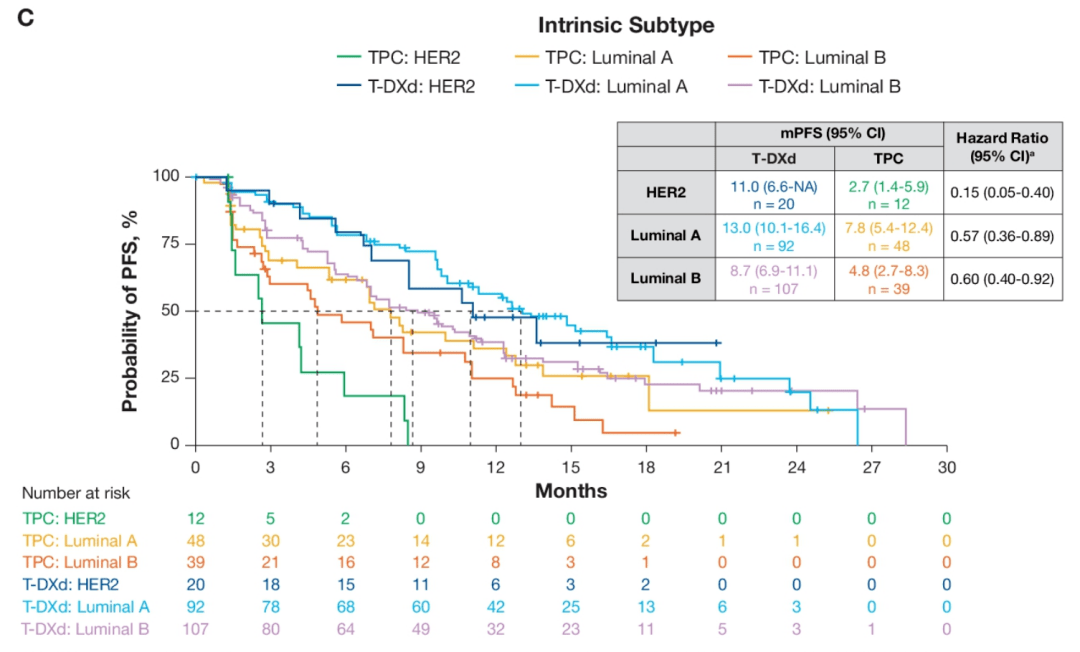
△DB-04研究中:不同ESR1状态患者的PFS 在不同PAM50内在亚型中,HER2富集患者治疗获益程度最大,PFS事件风险降低85%(HR 0.15),Luminal A型(HR 0.57)和Luminal B型(HR 0.60)也有良好的PFS获益。在这三种亚型患者中,Luminal A型的PFS最长(11.0 vs 13.0 vs 8.7个月),这与其本身预后较好是一致的。
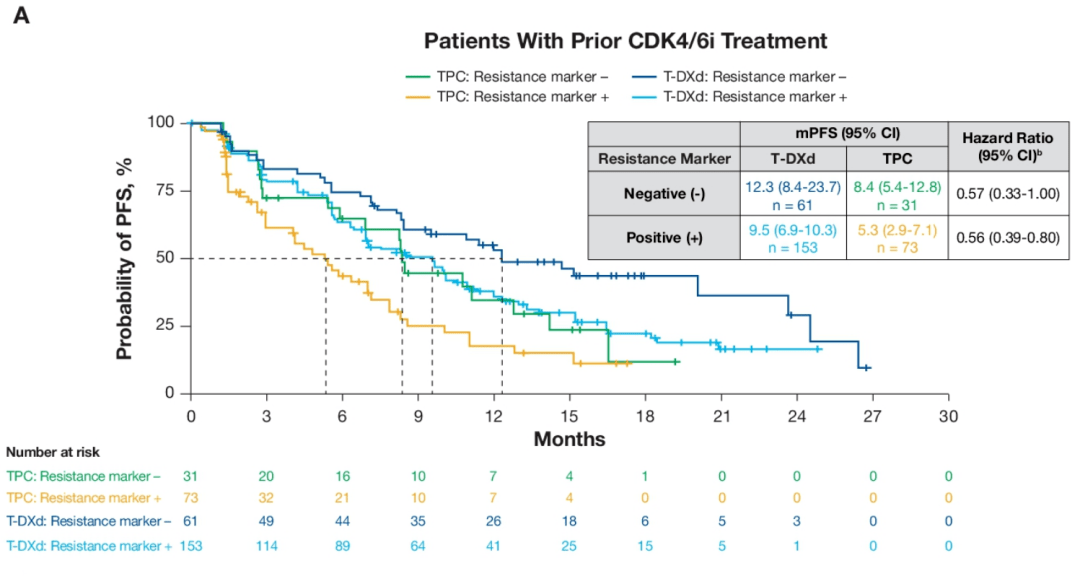
△DB-04研究中:不同内在亚型患者的PFS 在经CDK4/6i治疗的患者中,CDK4/6i耐药标志物阳性(HR 0.57)和阴性(HR 0.56)患者获益程度一致,CDK4/6i耐药标志物阳性患者的PFS比阴性患者更差(12.3 vs 9.5个月)。
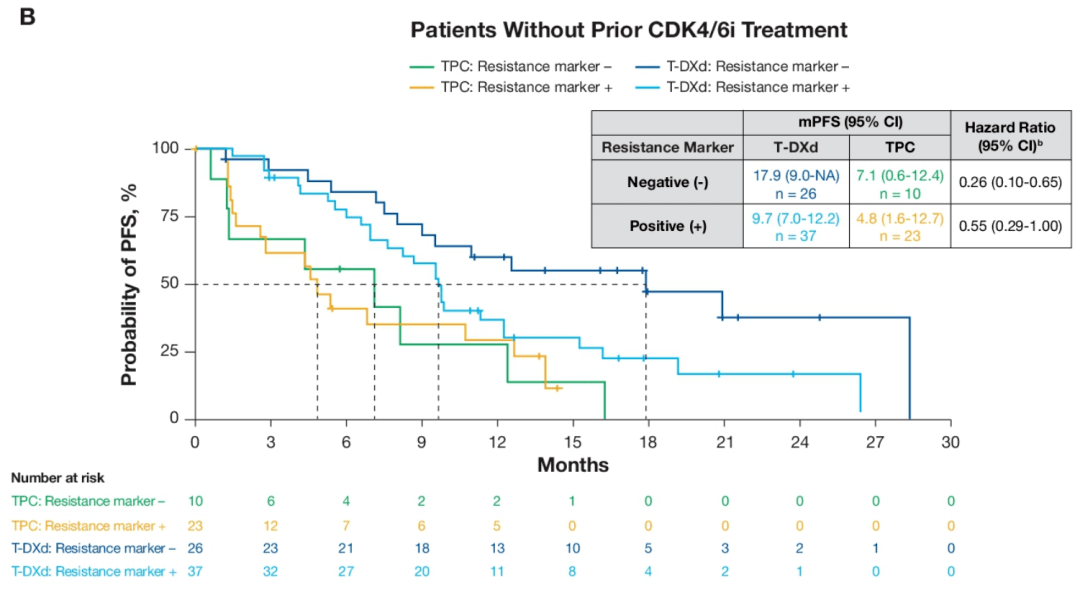
△DB-04研究中:未经CDK4/6i治疗患者中,CDK4/6i耐药标志物阴性或阳性患者的PFS 在未经CDK4/6i治疗的患者中,CDK4/6i耐药标志物阳性患者的PFS事件风险降低74%(HR 0.26),阴性患者(HR 0.55)也有较好的获益。值得注意的是,在未经CDK4/6i而初次接受T-DXd治疗的标志物阴性患者中,PFS长达17.9个月,预示T-DXd在前线治疗中可能有巨大应用潜力。
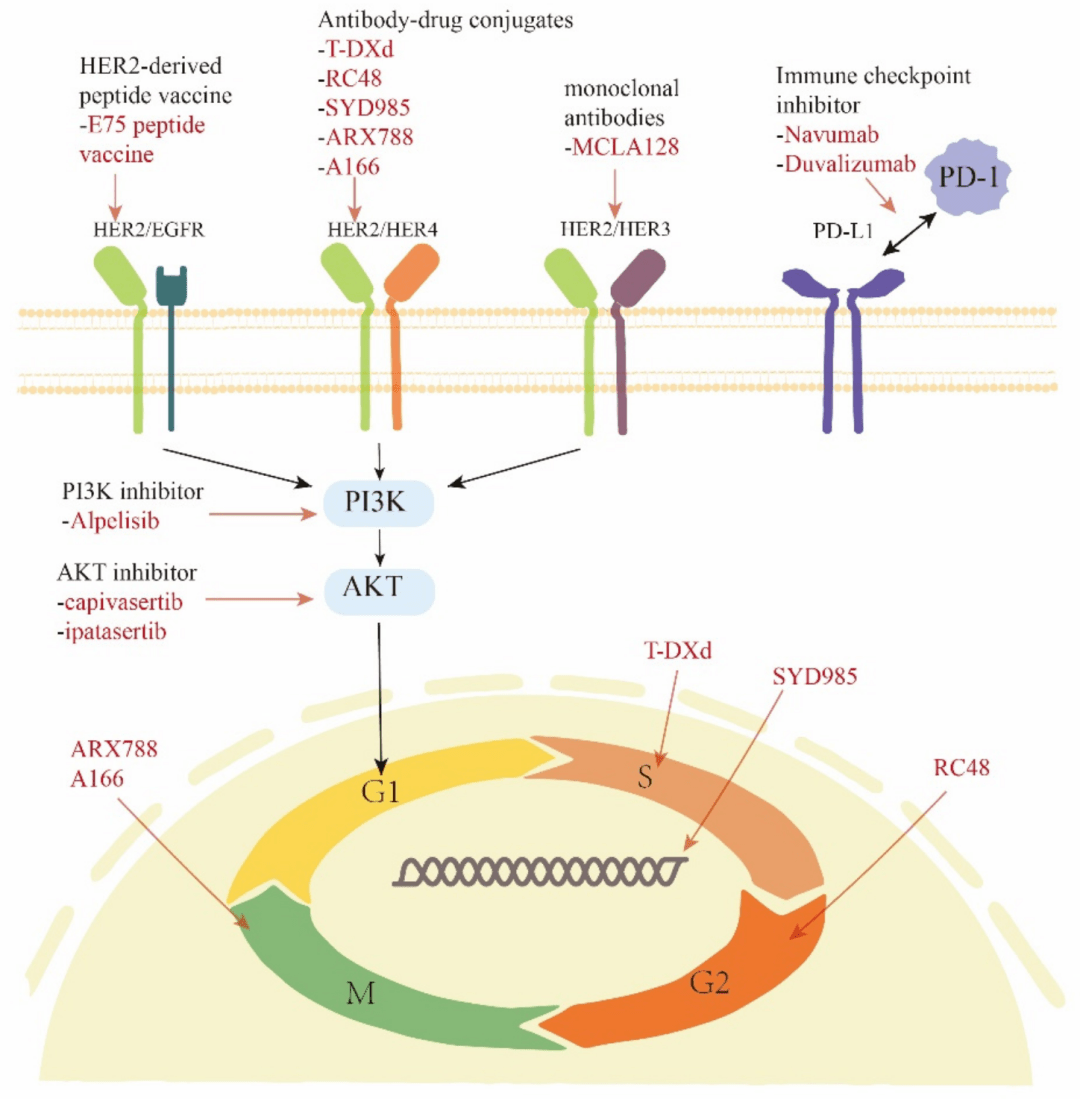
△DB-04研究中:经CDK4/6i治疗患者中,CDK4/6i耐药标志物阴性或阳性患者的PFS 总之,这项探索性研究显示,在不同PAM50内在亚型、CDK4/6i耐药标志物阴性或阳性、ESR1和PIK3CA突变或野生型患者中,T-DXd治疗HER2-L ABC均有生存获益。这些分子对HR+/HER2-乳腺癌内分泌或靶向治疗反应有重要影响,并且在传统抗HER2治疗相关信号通路改变中扮演重要角色;而T-DXd的治疗获益不受到这些标志物的影响。 03 HER2-L:精准治疗“可圈可点” 尽管mAb、TKI以及初代ADC对HER2-L乳腺癌的疗效有限,但HER2-L乳腺癌的精准治疗仍有许多“宝藏”策略值得挖掘,包括新型ADC、双抗/三抗疗法、免疫检查点抑制剂(ICI)、HER2驱动的肽疫苗等;此外,在HER2下游信号通路中,靶向于PI3K/AKT/mTOR的精准治疗也有潜在应用价值 [3] 。目前,除T-DXd以外,大多数药物尚处于临床试验;这些治疗药物的原理和机制各部相同,能否像T-DXd一样突破常见耐药突变、生物标志物的限制,仍待进一步探索。
△当前常见的HER2-L治疗策略 [3] ADCDB-04研究开启了“三元”抗HER2治疗时代,目前已经得到NCCN、ESMO等国际指南推荐,改变了晚期HR+/HER2-和TNBC的治疗格局。T-DXd的成功带动了更多聚焦于HER2-L乳腺癌的新型ADC研发,包括RC48、SYD985、A166等。这些ADC均以HER2作为抗原,连接子具有可裂解性,主要区别在于载药以及药物抗体比(DAR)等(见下表)。1期C001CANCER研究显示RC48治疗HER2-L有较好的ORR(39.6%) [4] ;MRG002的2期研究显示其治疗HER2-L的ORR也达到33% [5] ;SYD985的1期研究同样达到不错的完全缓解(PR)率(HR+和TNBC分别为28%和40%) [6] ;A166的1期研究6例HER-L患者也有75%的疾病控制率(DCR) [7] ,这些新型ADC均展示了积极的抗肿瘤活性,但仍待进一步扩大样本验证。此外,SG(rop-ADC)等其他非HER2靶点的新型ADC,在HER2-L患者中也有效。 双抗或三抗 mAb或TKI 靶向HER2胞内信号通路PI3K/AKT/mTOR信号通路参与细胞周期、细胞增殖和血管生成,还可以调节HER2和ER受体的表达;因此靶向该信号通路是逆转内分泌耐药和抗HER2耐药的重要靶点。但目前的PI3K抑制剂、AKT抑制剂、mTOR抑制剂尚未有关于HER2-L的亚组分析或针对此类人群的临床试验。 靶向免疫微环境这类治疗主要包括HER2驱动的肽疫苗和ICIs。一项2b期研究的亚组分析显示,HER2免疫原性肽nelipepimut-S(NP-S)治疗HER2 IHC 1+或2+的患者有DFS改善趋势(HR 0.62, P =0.18) [8] 。此外,ICIs在HR+/HER2-和TNBC领域已成为重要治疗选择,针对HER2-L患者,也有ICIs联合T-DXd的研究正在开展中。 总之,T-DXd用于治疗HER2-L晚期乳腺癌可以带来显著的生存获益和疗效提升,并且不受CDK4/6i耐药相关突变、ESR1和PIK3CA突变等标志物的限制,是一款可以使广泛人群获益的精准治疗方案;与此同时,T-DXd也带动了更多新型药物聚焦于HER2-L乳腺癌,未来或可为此类患者提供更加丰富、更加精准分层的治疗方案。 参考文献 上下滑动查看更多内容 [2]Shanu Modi, et al. Trastuzumab deruxtecan (T-DXd) vs treatment of physician’s choice (TPC) in patients (pts) with HER2-low, hormone receptor-positive (HR+) unresectable and/or metastatic breast cancer (mBC): Exploratory biomarker analysis of DESTINY-Breast04.J Clin Oncol 41, 2023 (suppl 16; abstr 1020) [6]Banerji U, van Herpen CML, Saura C, et al. Trastuzumab duocarmazine in locally advanced and metastatic solid tumours and HER2-expressing breast cancer: a phase 1 dose-escalation and dose-expansion study. Lancet Oncol. 2019;20(8):1124-1135. doi:10.1016/S1470-2045(19)30328-6
傅芳萌 教授 福建医科大学附属协和医院乳腺外科副主任 主任医师,副教授,医学博士,硕士生导师 约翰霍普金斯肿瘤外科临床博士后 中国临床肿瘤学会(CSCO)青委会(常委) 中华医学会肿瘤学分会乳腺学组青年委员 福建省医学会外科学分会乳腺外科学组秘书 福建省医学会外科学分会转化医学组副组长 主持国自然、福建省重点项目自然科学基金等多个项目 精彩推荐 福建医科大学附属协和医院乳腺外科两项研究成果被2023 ASCO年会收录 ASCO(美国临床肿瘤学会)年会汇聚全球临床肿瘤学研究的精英,是最具影响力的肿瘤学术会议,被誉为国际肿瘤学“奥斯卡盛典”。在2023年ASCO大会上,福建医科大学附属协和医院乳腺外科两项临床转化研究入选ASCO摘要发表!两项研究第一作者分别为乳腺外科科主任王川教授的博士研究生 李燕和硕士研究生 金璇,通讯作者为 傅芳萌副教授和 王川教授。此次入选,彰显该院乳腺外科在世界乳腺肿瘤科研领域的不凡力量与国际影响。该院乳腺外科将不断提升科研、诊疗实力,加强了与医疗同仁之间的交流学习,以期为乳腺癌症患者提供更好的治疗方案和医疗服务。 研究项目一在接受新辅助化疗的三阴性乳腺癌人群中,血浆循环肿瘤DNA独立于病理完全缓解与长期预后相关。 该研究对82例接受新辅助化疗的三阴性乳腺癌患者初次入院的血浆循环肿瘤DNA进行相关耐药基因与驱动基因检测,中位随访22.8月,发现ctDNA存在与否、TP53突变和参与PI3K-Akt信号通路的基因突变与否都是患者独立于包括病理完全缓解和其它临床病理特征的预后因素。基于TP53是否突变联合传统的临床病理因素构建的模型对三年总生存时间预测的ROC高达0.936,相较于传统的临床病理因素构建的模型为优(AUC: 0.751, P = 0.028),提示了血浆循环肿瘤ctDNA中TP53基因检测对接受新辅助化疗的三阴性乳腺癌患者长期生存的潜在应用价值。
同源重组修复缺陷(HRD)状态预测三阴性乳腺癌含铂新辅助化疗的疗效及预后。 该研究研究前瞻性收集了123例在我院接受标准新辅助化疗方案叠加铂类的临床II-III期三阴性乳腺癌患者,最终有104例患者的治疗前肿瘤穿刺标本及配对血标本成功进行了同源重组修复缺陷HRD状态检测并纳入后续统计分析。研究使用更加适合中国人群的HRD检测panel,并对HRD阳性进行了新的判定。结果发现,HRD是早期TNBC含铂新辅助化疗疗效及预后的有力预测生物标志物,并且HRD阳性的患者有更高的病理完全缓解率(pCR)、无事件生存(EFS)、无远处转移生存(DDFS)及总生存(OS);此外,我们探索性地构建了仅包含传统临床参数的模型,及在此基础上加入HRD的模型,比较二者在预测患者3年远期生存中的能力,结果显示,相比于传统临床参数模型,加入HRD的模型预测效能更优,其3年EFS的AUC为0.810(vs 0.668, P =0.017)。
(来源:《肿瘤瞭望》编辑部) 声 明 凡署名原创的文章版权属《肿瘤瞭望》所有,欢迎分享、转载。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。返回搜狐,查看更多 |
【本文地址】